
【題目】燃料電池具有廣闊的發展前途,科學家近年研制出一種微型的燃料電池,采用甲醇取代氫氣做燃料可以簡化電池設計,該電池有望取代傳統電池。某學生在實驗室利用堿性甲醇燃料電池電解Na2SO4溶液。
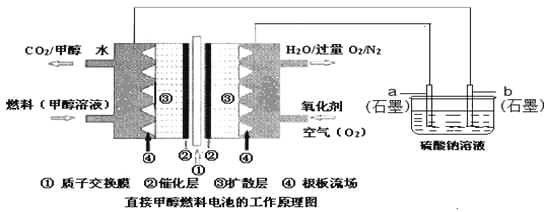
請根據圖示回答下列問題:
(1)圖中a電極是______(填“正極”、“負極”、“陰極”或“陽極”)。該電極上發生的電極反應式為_________________________________________。
(2)堿性條件下,通入甲醇的一極發生的電極反應式為____________________________。
(3)當消耗3.36 L氧氣時(已折合為標準狀況),理論上電解Na2SO4溶液生成氣體的總物質的量是__。
(4)25℃、101kPa時,燃燒16g甲醇生成CO2和H2O(l),放出的熱量為363.26kJ,寫出甲醇燃燒的熱化學方程式:_________________________________________。
【答案】陽極 4OH--4 e-=O2↑+2H2O CH3OH-6e-+8OH-=CO32-+ 6H2O 0.45 CH3OH(l)+ ![]() O2(g ) =CO2(g )+ 2H2O(l) △H=–726.52 kJ/mol
O2(g ) =CO2(g )+ 2H2O(l) △H=–726.52 kJ/mol
【解析】
(1)根據圖示,燃料電池中,甲醇發生氧化反應,通入燃料甲醇的電極是負極,通入氧氣的電極是正極,則和燃料電池負極相連的b極是陰極,和燃料電池正極相連的a極是陽極,石墨為惰性電極,電解硫酸鈉溶液,根據放電順序,在陽極上是氫氧根離子發生失電子的氧化反應,該電極上發生的電極反應式為:4OH--4e-=O2↑+2H2O。
(2)燃料電池的負極上是燃料甲醇發生失電子的氧化反應,在堿性條件下,CH3OH發生氧化反應生成CO32-,則電極反應式為:CH3OH-6e-+8OH-=CO32-+6H2O。
(3)氧氣在燃料電池的正極上通入,當消耗標準狀況下3.36LO2時,電路中轉移電子物質的量為![]() ×4=0.6mol,電解Na2SO4溶液的實質是電解水,根據電解方程式:2H2O
×4=0.6mol,電解Na2SO4溶液的實質是電解水,根據電解方程式:2H2O![]() 2H2↑+O2↑~4e-,生成氣體的物質的量是0.6mol×
2H2↑+O2↑~4e-,生成氣體的物質的量是0.6mol×![]() =0.45mol。
=0.45mol。
(4)在25℃、101kPa下,16g甲醇燃燒生成CO2和液態水時放熱363.26kJ,16g甲醇物質的量為16g÷32g/mol=0.5mol,則1mol甲醇燃燒生成液態水和二氧化碳氣體放熱363.26kJ×2=726.52kJ,因此表示甲醇燃燒的熱化學方程式為:CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) △H=-726.52kJ/mol。
O2(g)=CO2(g)+2H2O(l) △H=-726.52kJ/mol。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】被譽為改變未來世界的十大新科技之一的燃料電池具有無污染、無噪音、高效率的特點。如圖1為氫氧燃料電池的結構示意圖,電解質溶液為KOH溶液,電極材料為疏松多孔的石墨棒。當氧氣和氫氣分別連續不斷地從正、負兩極通入燃料電池時,便可在閉合回路中不斷地產生電流。
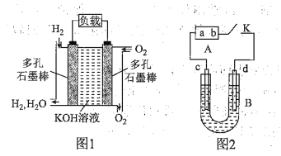
回答下列問題:
![]() 圖1中通過負載的電子流動方向為________
圖1中通過負載的電子流動方向為________![]() 填“向左”或“向右”
填“向左”或“向右”![]() 。
。
![]() 寫出氫氧燃料電池工作時的電極反應式:正極:________,負極:________。
寫出氫氧燃料電池工作時的電極反應式:正極:________,負極:________。
以該燃料電池為電源進行實驗,如圖2所示,B為電解槽,c、d為鐵電極,B中裝有一定濃度的NaOH溶液,閉合K,c電極周圍逐漸析出白色沉淀。
![]() 極是電池的________
極是電池的________![]() 填“正極”或“負極”
填“正極”或“負極”![]() ,c電極的電極反應式為________。
,c電極的電極反應式為________。
![]() 若c、d為石墨電極,B中裝有
若c、d為石墨電極,B中裝有![]() 和
和![]() 的混合溶液,其中
的混合溶液,其中![]() 的物質的量濃度為
的物質的量濃度為![]() ,
,![]() 的物質的量濃度為
的物質的量濃度為![]() 。閉合K,c電極收集到標準狀況下
。閉合K,c電極收集到標準狀況下![]() 的一種氣體甲。在收集氣體甲的過程中電解明顯分為兩個階段,請寫出相應的電解總化學方程式:第一階段:________ ;第二階段:________;d電板理論上收集到的氣體體積是________
的一種氣體甲。在收集氣體甲的過程中電解明顯分為兩個階段,請寫出相應的電解總化學方程式:第一階段:________ ;第二階段:________;d電板理論上收集到的氣體體積是________![]() 標準狀況下
標準狀況下![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】霧霾中含有多種污染物,包括氮氧化物![]() 、CO、
、CO、![]() 等。它們可以通過化學反應得到一定的消除或轉化。
等。它們可以通過化學反應得到一定的消除或轉化。
![]() 氮硫的氧化物的轉化:
氮硫的氧化物的轉化: ![]()
已知:![]()
![]()
![]() ,則
,則![]() _______
_______![]() 。
。
一定條件下,將![]() 與
與![]() 以一定比例置于恒溫恒容的密閉容器中發生上述反應,下列能說明反應達到平衡狀態的有_______。
以一定比例置于恒溫恒容的密閉容器中發生上述反應,下列能說明反應達到平衡狀態的有_______。
![]() 混合氣體的密度不變
混合氣體的密度不變 ![]() 混合氣體的顏色保持不變
混合氣體的顏色保持不變
![]() 和NO的體積比保持不變
和NO的體積比保持不變 ![]() 反應速率
反應速率![]()
![]() 碳氧化物的轉化:
碳氧化物的轉化:
![]() 可用于合成甲醇,反應方程式為:
可用于合成甲醇,反應方程式為:![]() ,在一恒溫恒容密閉容器中充入
,在一恒溫恒容密閉容器中充入![]() 和
和![]() 進行上述反應。測得CO和
進行上述反應。測得CO和![]() 濃度隨時間變化如圖1所示。
濃度隨時間變化如圖1所示。

則![]() 內,氫氣的反應速率為____
內,氫氣的反應速率為____![]() 第
第![]() 后,保持溫度不變,向該密閉容器中再充入
后,保持溫度不變,向該密閉容器中再充入![]() 和
和![]() ,則平衡_______
,則平衡_______![]() 填“正向”、“逆向”或“不”
填“正向”、“逆向”或“不”![]() 移動。
移動。
![]() 通過電解CO制備
通過電解CO制備![]() ,電解液為碳酸鈉溶液,工作原理如圖2所示,寫出陰極的電極反應式_____。若以甲醇燃料電池作為電源,則生成標準狀況下
,電解液為碳酸鈉溶液,工作原理如圖2所示,寫出陰極的電極反應式_____。若以甲醇燃料電池作為電源,則生成標準狀況下![]() 需要消耗
需要消耗![]() 的質量為_______。
的質量為_______。

![]() 硫氧化物的轉化:硫的氧化物與一定量氨氣、空氣反應,可生成硫酸銨。硫酸銨水溶液呈酸性的原因是________________
硫氧化物的轉化:硫的氧化物與一定量氨氣、空氣反應,可生成硫酸銨。硫酸銨水溶液呈酸性的原因是________________![]() 用離子方程式表示
用離子方程式表示![]() 室溫時,向
室溫時,向![]() 溶液中滴入NaOH溶液至溶液呈中性,則所得溶液中微粒濃度大小關系:
溶液中滴入NaOH溶液至溶液呈中性,則所得溶液中微粒濃度大小關系:![]() ____
____![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】①~⑤五種元素在元素周期表中的位置如下圖所示:
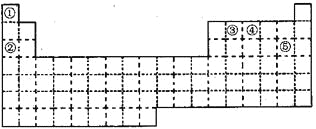
回答下列問題:
(1)①~⑤五種元素中,非金屬性最強的元素在周期表中的位置是___________;
(2)②③④元素原子中,半徑最小的是_________(填元素符號);
(3)元素①和③可以形成眾成多的化合物,其中最簡單的是_____(化學式)。該化合物中,化學鍵的類型為_________(選填“極性共價鍵”、 “非極性共價鍵”或“離子鍵”);
(4)元素④的最高價氧化物對應水化物能與其最低價的氣態氫化物發生反應,產物是________(化學式);
(5)元素⑤單質與水反應的離子方程式:________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下反應4NH3(g)+5O2(g)=4NO(g)+6H2O(g)開始進行時,c(NH3)=0.04mol/L,經5min后,c(NH3)=0.03mol/L,則v(H2O)為( )
A.0.003mol/(Lmin)B.0.002mol/(Lmin)
C.0.0045mol/(Lmin)D.0.003mol/(Ls)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活、環境密切相關,下列有關說法正確的是![]()
![]()
A.我國在南海成功開采的可燃冰![]() 可能會帶來酸雨等環境污染
可能會帶來酸雨等環境污染
B.大量使用含丙烷、二甲醚等輔助成分的“空氣清新劑”,會對環境造成新的污染
C.在人體內酶的作用下,纖維素可以發生水解反應生成葡萄糖
D.我國全面啟動的北斗導航系統的信號傳輸與硅有關
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列根據實驗及現象得出的結論不正確的是
實驗 | 現象 | 結論 | |
A |
| 試管(1)中紫色消失,試管(2)中紫色沒有消失 | 甲苯中苯環使甲基的活性增強 |
B |
| 試管內壁有銀鏡生成 | X具有還原性,一定含有醛基 |
C |
| 先生成白色沉淀,滴加FeCl3溶液后,生成紅褐色沉淀 | Fe(OH)3 是比Mg(OH)2 更難溶的電解質 |
D |
| 試管b比試管a中溶液的紅色深 | 增大反應物濃度,平衡向正反應方向移動 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述不正確的是 ( )
A.通常狀況下,氯氣是一種黃綠色有毒的氣體,在加壓條件下轉化為液態,可儲存在鋼瓶中,便于運輸和使用
B.通常狀況下,碘單質是紫黑色的固體,易升華,遇淀粉溶液,溶液會變藍色
C.鎂是一種活潑的金屬,一旦失火,若用泡沫滅火器滅火反而會燃燒得更旺
D.![]() 是一種白色晶體,溶于水,溶液呈弱堿性,所以是醫學上治療胃酸過多的一種試劑
是一種白色晶體,溶于水,溶液呈弱堿性,所以是醫學上治療胃酸過多的一種試劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物種類多種多樣,具有廣泛的應用價值。回答下列問題。
(1)用乙烯、己烷、乙酸乙酯、甲酸、葡萄糖、麥芽糖6種物質名稱回答下列問題。
①作為衡量國家石油工業水平標志的物質是______________。
②能因為萃取而使溴水褪色的是____________________。
③能發生水解反應的是_____________________。
④加熱條件下,能與新制Cu(OH)2懸濁液反應生成磚紅色沉淀的是____________。
(2)已知:RCHO+R′CH2CHO![]()
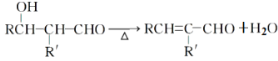 ,請寫出苯甲醛與丙醛在上述條件下反應,得到有機產物的結構簡式____________。
,請寫出苯甲醛與丙醛在上述條件下反應,得到有機產物的結構簡式____________。
(3)已知:![]()
Nomex纖維是一種新型阻燃性纖維。可由間苯二甲酸(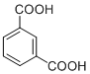 )和間苯二胺(
)和間苯二胺(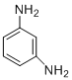 )在一定條件下以等物質的量縮聚合成得到。則Nomex纖維結構簡式為____________。
)在一定條件下以等物質的量縮聚合成得到。則Nomex纖維結構簡式為____________。
(4)下列物質的反應,不屬于取代反應的是____________。(填序號)
A.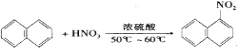 +H2O
+H2O
B.CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
C.CH3COOH+CH3OH![]() CH3COOCH3+H2O
CH3COOCH3+H2O
D. [式中R為CH3(CH2)15CH2—]
[式中R為CH3(CH2)15CH2—]
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com