
【題目】設阿伏加德羅常數的值為![]() 。下列說法正確的是
。下列說法正確的是
A.![]() 氧氣與
氧氣與![]() 金屬鈉充分反應,轉移的電子數為
金屬鈉充分反應,轉移的電子數為![]()
B.加熱時,![]() 銅粉與足量濃硫酸反應,轉移的電子數為
銅粉與足量濃硫酸反應,轉移的電子數為![]()
C.將![]() 乙烷和
乙烷和![]() 混合光照,生成一氯乙烷的分子數為
混合光照,生成一氯乙烷的分子數為![]()
D.![]() 的
的![]() 溶液中
溶液中![]() 的數目小于
的數目小于![]()
科目:高中化學 來源: 題型:
【題目】某研究性學習小組查閱資料:“氯氣與硫在加熱條件下生成二氯化硫(S2Cl2),該物質遇水迅速反應,他們利用如下儀器和藥品制取純凈的氯氣與硫反應來制備S2Cl2
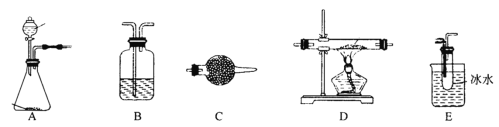
實驗過程所提供的藥品有:濃鹽酸、濃H2SO4、MnO2、KMnO4(H+)、飽和NaHCO3溶液、堿石灰、硫磺、NaOH溶液、冰水、飽和食鹽水。
回答下列問題:
(1)利用所提供的設備和藥品,寫出制備Cl2的離子方程式:________________
(2)在該實驗過程中兩次用到儀器B,第一次裝置B中的藥品是____________,第二次裝置B的作用是____________________________________________________。
(3)能否省略裝置C________(填“能”或“否”),原因是_________________________________。
(4)實驗開始后,當_______________________________________________,(填現象)點燃D處的酒精燈。
(5)某學生利用裝置A制備一定量的Cl2,他收集到的Cl2的體積總比預期的要多,他經過認真分析后,認為應對裝置A略作改進,你認為怎樣改進:_____________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種碳納米管能夠吸附氫氣,用這種材料制備的二次電池原理如下圖所示,該電池的電解質為6 mol·L-1KOH溶液,下列說法中正確

A. 放電時K+移向負極
B. 放電時電池負極的電極反應為H2-2e-===2H+
C. 放電時電池正極的電極反應為NiO(OH)+H2O+e-===Ni(OH)2+OH-
D. 該電池充電時將碳電極與電源的正極相連
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 表示阿伏加德羅常數,下列說法正確的是
表示阿伏加德羅常數,下列說法正確的是
A.1mol硝基![]() 與46g二氧化氮
與46g二氧化氮![]() 所含的電子數均為
所含的電子數均為![]()
B.![]() 液與
液與![]() 溶液中的
溶液中的![]() 數目相同
數目相同
C.標準狀況下,![]() 三氯甲烷中含碳氯共價鍵的數目為
三氯甲烷中含碳氯共價鍵的數目為![]()
D.向FeI2溶液中通入適量![]() ,當有
,當有![]() 被氧化時,轉移的電子數為
被氧化時,轉移的電子數為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】弱電解質的電離平衡、鹽類的水解平衡和難溶物的溶解平衡均屬于化學平衡。
(1)在25℃時,將c mol·L-1的醋酸溶液與0.02 mol·L-1 NaOH溶液等體積混合后溶液剛好呈中性,用含c的代數式表示CH3COOH的電離常數Ka=________。
(2)25℃時,H2SO3![]() HSO3-+H+的電離常數Ka=1×10-2 mol·L-1,則該溫度下NaHSO3水解反應的平衡常數Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,則溶液中
HSO3-+H+的電離常數Ka=1×10-2 mol·L-1,則該溫度下NaHSO3水解反應的平衡常數Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,則溶液中 將________(填“增大”、“減小”或“不變”)。
將________(填“增大”、“減小”或“不變”)。
(3)已知H2A在水中存在以下平衡:H2A=H++HA-,HA-![]() H++A2-。常溫下H2A的鈣鹽(CaA)的飽和溶液中存在以下平衡:CaA(s)
H++A2-。常溫下H2A的鈣鹽(CaA)的飽和溶液中存在以下平衡:CaA(s)![]() Ca2+(aq)+A2-(aq) △H>0。若要使該溶液中Ca2+濃度變小,可采取的措施有________。
Ca2+(aq)+A2-(aq) △H>0。若要使該溶液中Ca2+濃度變小,可采取的措施有________。
A.升高溫度 B.降低溫度 C.加入NH4Cl晶體 D.加入Na2A固體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若NA表示阿伏加德羅常數,下列敘述中正確的是 ( )
A.標準狀況下,22.4L SO3含NA個分子
B.含0.4mol HCl的濃鹽酸與足量二氧化錳反應轉移電子數為0.2NA
C.32gCu與足量硫完全反應,轉移的電子數為0.5NA
D.在200mL 5mol·L-1 AlCl3溶液中,Al3+數目為NA,等于Cl-數目的1/3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 為阿伏加德羅常數,下列敘述正確的是
為阿伏加德羅常數,下列敘述正確的是![]()
![]()
A.過氧化鈉與水反應時,生成![]() 轉移的電子數為
轉移的電子數為![]()
B.![]() 用NaOH溶液充分吸收,轉移的電子數目為
用NaOH溶液充分吸收,轉移的電子數目為![]()
C.常溫常壓下,![]() 和
和![]() 混合,生成氣體分子數目為
混合,生成氣體分子數目為![]()
D.常溫常壓下,![]() 與足量的鐵屑反應轉移電子數目為
與足量的鐵屑反應轉移電子數目為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎢是熔點最高的金屬,是重要的戰略物資。自然界中鎢主要存在于黑鎢礦中,其主要成分是鐵和錳的鎢酸鹽(FeWO4、MnWO4),還含少量Si、As的化合物。由黑鎢礦冶煉鎢的工藝流程如圖1:
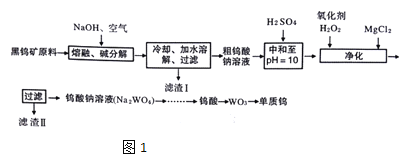
已知:
①濾渣I的主要成份是Fe2O3、MnO2
②上述流程中,鎢的化合價只有在最后一步發生改變。
③常溫下鎢酸難溶于水。
(1)鎢酸鹽(FeWO4、MnWO4)中鎢元素的化合價為___,請寫出MnWO4在熔融條件下發生堿分解反應生成Fe2O3的化學方程式___
(2)上述流程中向粗鎢酸鈉溶液中加硫酸中和至pH=10后,溶液中的雜質陰離子確SiO32-、HAsO32-、HAsO42-等,則“凈化”過程中,加入H2O2時發生反應的離子方程式為___,濾渣Ⅱ的主要成分是___
(3)已知氫氧化鈣和鎢酸鈣(CaWO4)都是微溶電解質,兩者的溶解度均隨溫度升高而減小。圖2為不同溫度下Ca(OH)2、CaWO4的沉淀溶解平衡曲線,則:
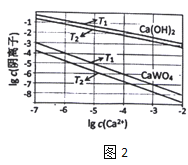
①T1___T2(填“>”或“<”)T1時Ksp(CaWO4)=___
②將鎢酸鈉溶液加入石灰乳得到大量鎢酸鈣,發生反應的離子方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物 X(C4H6O5)廣泛存在于許多水果內,尤以葡萄、西瓜、山渣內為多,X 的碳鏈結構無支鏈,分子式為 C4H6O5;1.34gX 與足量的鈉溶液反應,生成標準狀況下的氣體 0.336L。X與醇或羧酸在濃 H2SO4 和加熱的條件下均生成有香味的產物。X 在一定條件下可發生反應生成A,A![]() B
B![]() C(X、A、B、C 分子中碳原子數目相同)。下列有關說法中不正確的是( )
C(X、A、B、C 分子中碳原子數目相同)。下列有關說法中不正確的是( )
A.X 的結構簡式為 HOOC—CHOH—CH2—COOH
B.A 的分子式為 C4H4O4
C.與 X的官能團種類、數量完全相同的同分異構體還有 3 種
D.C 物質能溶于水
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com