
【題目】海水是巨大的資源寶庫,從海水中提取食鹽和溴的過程如圖所示;下列描述錯誤的是:

A. 淡化海水的方法主要有蒸餾法、電滲析法、離子交換法
B. 以NaCl為原料可以生產燒堿、純堿、金屬鈉、氯氣、鹽酸等化工產品
C. 步驟Ⅱ中鼓入熱空氣吹出溴,是因為溴蒸氣的密度比空氣的密度小
D. 用SO2水溶液吸收Br2的離子反應方程式為:Br2+SO2+2H2O═4H++SO42﹣+2Br﹣
科目:高中化學 來源: 題型:
【題目】下列關于能量轉換的認識中不正確的是
A. 電解水生成氫氣和氧氣時,電能轉化成化學能
B. 白熾燈工作時電能全部轉變成光能
C. 電池將化學能轉化為電能
D. 煤燃燒時化學能主要轉變成熱能
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用反應6NO2+8NH3===7N2+12H2O構成電池的裝置如圖所示。此方法既能實現有效清除氮氧化物的排放,減輕環境污染,又能充分利用化學能。下列說法正確的是()

A. 電流從左側電極經過負載后流向右側電極
B. 為使電池持續放電,離子交換膜需選用陰離子交換膜
C. 電極A極反應式為2NH3-6e-===N2+6H+
D. 當有4.48 L NO2被處理時,轉移電子數為0.8NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現用0.1000 mol·L-1KMnO4酸性溶液滴定未知濃度的無色H2C2O4溶液,反應離子方程式是:2MnO4-+5H2C2O4+6H+ = 2Mn2++10CO2↑+8H2O
填空完成問題:
(1)該滴定實驗所需的玻璃儀器有______________。(填字母)
A.酸式滴定管B.堿式滴定管 C.量筒 D.錐形瓶 E.鐵架臺F.滴定管夾G.燒杯H.白紙 I.漏斗
(2)不用________(填“酸”或“堿”)式滴定管盛放高錳酸鉀溶液。試分析原因___________________________________________。
(3)滴定終點的現象為___________________________________。
(4)若滴定開始和結束時,滴定管中的液面如圖所示,則起始讀數為________mL,終點讀數為________mL。
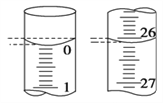
(5)某學生根據3次實驗分別記錄有關數據如下表:
滴定 次數 | 待測H2C2O4溶液的體積/mL | 0.1000 mol/L KMnO4的體積(mL) | ||
滴定前刻度 | 滴定后刻度 | 溶液體積/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依據上表數據列式計算該H2C2O4溶液的物質的量濃度為_______________。
(6)下列操作中可能使測定結果偏低的是___________(填字母)。
A.酸式滴定管未用標準液潤洗就直接注入KMnO4標準液
B.滴定前盛放草酸溶液的錐形瓶用蒸餾水洗凈后沒有干燥
C.酸式滴定管尖嘴部分在滴定前沒有氣泡,滴定后有氣泡
D.讀取KMnO4標準液時,開始仰視讀數,滴定結束時俯視讀數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.物質的量是描述微觀離子集合的一個物理量
B.摩爾可以把物質的量、體積等宏觀量與原子、分子或離子等微觀離子聯系起來
C.阿伏加德羅常數可近似表示為6.02×1023
D.摩爾是國際單位制的七個基本物理量之一
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T℃,分別向10ml濃度均為1mol/L的兩種弱酸HA、HB中不斷加水稀釋,并用pH傳感器測定溶液pH。所得溶液pH的兩倍(2pH)與溶液濃度的對數(1gc)的關系如圖所示。下列敘述正確的是
己知:(1)HA的電離平衡常數Ka=[c(H+)·c(A-)]/[c(HA)-c(A-)]≈c2(H+)/c(HA);(2)pKa=-lgKa

A. 弱酸的Ka隨溶液濃度的降低而增大
B. a點對應的溶液中c(HA)=0.1mol/L,pH=4
C. 酸性:HA<HB
D. 弱酸HB的pKa=5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】結合下表回答下列問題(均為常溫下的數據):
酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
請回答下列問題:
(1) 同濃度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中結合H+的能力最弱的是_________。
(2) 0.1mo1/L的H2C2O4溶液與0.1mo1/L的KOH的溶液等體積混合后所得溶液呈酸性,該溶液中各離子濃度由大到小的順序為________________。
(3)pH相同的NaC1O和CH3COOK溶液中,[c(Na+)-c(C1O-)]______[c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mo1/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此時溶液pH=_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】正丁醚常用作有機反應的溶劑。實驗室制備正丁醚的反應和主要實驗裝置如下:2CH3CH2CH2CH2OH![]() (CH3CH2CH2CH2)2O+H2O,反應物和產物的相關數據如下表:
(CH3CH2CH2CH2)2O+H2O,反應物和產物的相關數據如下表:
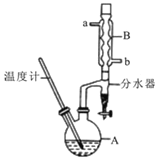

①將6 mL濃硫酸和37 g正丁醇,按一定順序添加到A中,并加幾粒沸石。
②加熱A中反應液,迅速升溫至135℃,維持反應一段時間。
③分離提純:待A中液體冷卻后將其緩慢倒入盛有70 mL水的溫度分液漏斗中,振搖后靜置,分液得粗產物。
④粗產物依次用40 mL水、20 mL NaOH溶液和40 mL水洗滌,分液后加入約3g無水氯化鈣顆粒,靜置一段時間后棄去氯化鈣。
⑤將上述處理過的粗產物進行蒸餾,收集餾分,得純凈正丁醚11g。請回答:
(1)步驟①中濃硫酸和正丁醇的添加順序為:應先加 。
(2)加熱A前,需先從 (填“a”或“b”)口向B中通入水。
(3)步驟③的目的是初步洗去 ,振搖后靜置,粗產物應 (填“上”或“下”)口倒出。
(4)步驟⑤中,加熱蒸餾時應收集 (填選項字母)左右的餾分。
A.100℃ B.117℃ C.135℃ D.142℃
(5)反應過程中會觀察到分水器中收集到液體物質,且分為上下兩層,隨著反應的進行,分水器中液體逐漸增多至充滿時,上層液體會從左側支管自動流回A。分水器中上層液體的主要成分為 ,下層液體的主要成分為 。
(6)本實驗中,正丁醚的產率為 (精確到1%)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com