
【題目】(1)有甲、乙兩種物質:甲![]() 、乙
、乙![]() 。由甲轉化為乙需經下列過程
。由甲轉化為乙需經下列過程![]() 已略去各步反應的無關產物,下同
已略去各步反應的無關產物,下同![]()
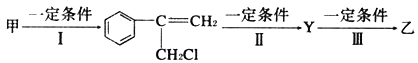
①反應I的反應類型是__________,反應II的條件是___________,反應III的化學方程式為_________________________
②下列物質不能與乙反應的是_________![]() 填序號
填序號![]() 。
。
![]() 金屬鈉
金屬鈉 ![]() 溴水
溴水 ![]() 氫氧化鈉溶液
氫氧化鈉溶液 ![]() 乙酸
乙酸
(2)寫出苯酚和碳酸鈉溶液反應的離子方程式__________________。
(3)寫出乙醛和銀氨溶液反應的化學方程式____________________。
(4)寫出乙二酸和鈉反應的化學方程式______________________。
【答案】取代反應 氫氧化鈉水溶液、加熱 ![]() +HCl→
+HCl→![]() b
b ![]() +CO32-→
+CO32-→![]() +HCO3- CH3CHO+2Ag(NH3)2OH
+HCO3- CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O HOOCCOOH+2Na→NaOOCCOONa+H2↑
CH3COONH4+2Ag↓+3NH3+H2O HOOCCOOH+2Na→NaOOCCOONa+H2↑
【解析】
(1)①根據流程圖可知,反應I為光照條件下,發生烷基氫原子的取代反應,反應II為鹵代烴在NaOH水溶液條件下的水解生成醇,反應III為碳碳雙鍵與HCl的加成反應,據此分析解答;
②根據乙中含有醇羥基和鹵素原子,結合醇和鹵代烴的性質分析解答;
(2)苯酚能跟碳酸鈉溶液反應,生成苯酚鈉和碳酸氫鈉;
(3)乙醛與銀氨溶液發生銀鏡反應生成醋酸銨、Ag、氨氣、水;
(4)乙二酸和鈉反應生成NaOOCCOONa和氫氣。
(1)①由甲轉化為乙過程可知,反應I為光照條件下,發生烷基氫原子的取代反應,反應II為NaOH水溶液、加熱條件下的水解生成醇,反應III為碳碳雙鍵與HCl的加成反應,其中反應III的化學方程式為:![]() +HCl→
+HCl→![]() ,故答案為:取代反應;氫氧化鈉水溶液、加熱;
,故答案為:取代反應;氫氧化鈉水溶液、加熱;![]() +HCl→
+HCl→![]() ;
;
②乙(![]() )中含有醇羥基,能與鈉反應,能與乙酸發生酯化反應,含有氯原子,在氫氧化鈉水溶液、加熱條件下可以發生水解反應,乙不能與溴水反應,故答案為:b;
)中含有醇羥基,能與鈉反應,能與乙酸發生酯化反應,含有氯原子,在氫氧化鈉水溶液、加熱條件下可以發生水解反應,乙不能與溴水反應,故答案為:b;
(2)苯酚能跟碳酸鈉溶液反應,生成苯酚鈉和碳酸氫鈉,反應的離子方程式為![]() +CO32-→
+CO32-→![]() +HCO3-,故答案為:
+HCO3-,故答案為:![]() +CO32-→
+CO32-→![]() +HCO3-;
+HCO3-;
(3)乙醛與銀氨溶液發生銀鏡反應生成乙酸銨、Ag、氨氣、水,反應的化學方程式為CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O,故答案為:CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag↓+3NH3+H2O,故答案為:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3+H2O;
CH3COONH4+2Ag↓+3NH3+H2O;
(4)乙二酸和鈉反應的化學方程式為HOOCCOOH+2Na→NaOOCCOONa+H2↑,故答案為:HOOCCOOH+2Na→NaOOCCOONa+H2↑。


科目:高中化學 來源: 題型:
【題目】Fenton法常用于處理含難降解有機物的工業廢水,往調節好pH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物。現運用該方法降解有機污染物p﹣CP,控制p﹣CP的初始濃度相同,恒定實驗溫度在298K或313K進行實驗。實驗測得p﹣CP的濃度隨時間變化的關系如圖所示,下列說法不正確的是( )

A.由①可得,降解反應在50~150s內的反應速率:v(pCP)=8.0×10﹣6molL﹣1s﹣1
B.升高溫度,有利于加快降解反應速率,但溫度過高反應速率又會變慢
C.③目的為探究溶液的pH對降解反應速率的影響
D.298K下,有機物p﹣CP降解速率pH=10時比pH=3快
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在兩個容積均為![]() 的恒容密閉容器中,起始時均充入
的恒容密閉容器中,起始時均充入![]() ,以溫度、
,以溫度、![]() 催化劑為實驗條件變量,進行
催化劑為實驗條件變量,進行![]() 的分解實驗
的分解實驗![]() 反應為
反應為![]() 。測得的結果如圖所示。
。測得的結果如圖所示。![]() 曲線Ⅱ、Ⅲ表示經過相同時間且未達到化學平衡時
曲線Ⅱ、Ⅲ表示經過相同時間且未達到化學平衡時![]() 的轉化率
的轉化率![]()
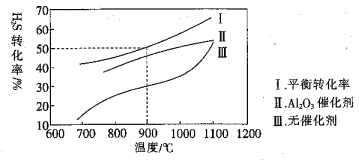
下列說法正確的是( )
A.溫度升高,![]() 分解的速率增大,
分解的速率增大,![]() 的含量減少
的含量減少
B.由曲線Ⅱ、Ⅲ可知,加入![]() 可提高
可提高![]() 的平衡轉化率
的平衡轉化率
C.![]() 時,ts后達到平衡,則
時,ts后達到平衡,則![]() 的生成速率為
的生成速率為![]()
D.約![]() 時,曲線Ⅱ、Ⅲ幾乎重合,說明
時,曲線Ⅱ、Ⅲ幾乎重合,說明![]() 可能幾乎失去催化活性
可能幾乎失去催化活性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以肉桂酸乙酯 M 為原料,經過相關化學反應合成的抗癌藥對治療乳腺癌有著顯著的療效。已知 M 能發生如下轉化:

已知:C的結構簡式為![]() ,請回答下列問題:
,請回答下列問題:
(1)A 的結構簡式為_____,E 中官能團的名稱是_____。
(2)寫出反應③和⑥的化學方程式: _____。
(3)在合適的催化劑作用下,由 E 可以制備高分子化合物 H,H 的結構簡式為_____,由 E 到 H的反應類型為_____。
(4)Ⅰ是 B 的同分異構體,且核磁共振氫譜中只有一組吸收峰,Ⅰ的結構簡式為_____。
(5)A 的同分異構體有多種,其中屬于芳香族化合物,既能使溴的四氯化碳溶液褪色,又能與碳酸氫鈉溶液反應的同分異構體有_____種(不包含 A)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20mL某一元酸(HA)溶液中逐滴加入0.1mol·L-1的NaOH溶液,測得混合溶液中由水電離出的c(H+)隨加入NaOH溶液的體積變化關系圖如下。下列說法不正確的是

A. Ka(HA)的數量級為10-5
B. d點溶液的pH最大
C. b點溶液顯酸性,c(A-)>c(Na+)>c(H+)>c(OH-)
D. d點溶液中,c(Na+)+c(H+)=c(A-)+c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有五種化合物是分別由以下原子![]() 團
團![]() 中的兩種不同的原子
中的兩種不同的原子![]() 團
團![]() 組成的:
組成的:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。已知A是一種能發生銀鏡反應的酸,它跟B在一定條件下可生成C和
。已知A是一種能發生銀鏡反應的酸,它跟B在一定條件下可生成C和![]() ,C是D的同分異構體,E可在堿性條件下和
,C是D的同分異構體,E可在堿性條件下和![]() 反應生成B。按要求回答問題
反應生成B。按要求回答問題![]() 提示:所有物質所含碳原子均不超過兩個,以上基團可以重復使用
提示:所有物質所含碳原子均不超過兩個,以上基團可以重復使用![]()
(1)C的結構簡式__________;
(2)A與D的關系______________________![]() 填序號
填序號![]() ;
;
①同系物 ②同分異構體 ③同種物質 ④同位素 ⑤同素異形體
(3)請寫出相對分子質量與D相等且屬于飽和一元醇的所有同分異構體的結構簡式______;
(4)請寫出下列反應的方程式:![]() 轉化的離子方程式:_____________;C與氫氧化鈉水溶液反應的化學方程式:_________。
轉化的離子方程式:_____________;C與氫氧化鈉水溶液反應的化學方程式:_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】測定0.1 mol·L-1 Na2SO3溶液先升溫再降溫過程中的pH,數據如下。
時刻 | ① | ② | ③ | ④ |
溫度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
實驗過程中,取①④時刻的溶液,加入鹽酸酸化的BaCl2溶液做對比實驗,④產生白色沉淀多。
下列說法不正確的是
A. Na2SO3溶液中存在水解平衡:![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ④的pH與①不同,是由于![]() 濃度減小造成的
濃度減小造成的
C. ①→③的過程中,溫度和濃度對水解平衡移動方向的影響一致
D. ①與④的Kw值相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖表示溶液中c(H+)和c(OH-)的關系,下列判斷錯誤的是
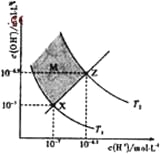
A. 兩條曲線間任意點均有c(H+)×c(OH-)=Kw
B. M區域內任意點均有c(H+)<c(OH-)
C. 圖中T1<T2
D. XZ線上任意點均有pH=7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A~G是短周期主族元素,原子序數依次增大,部分元素的部分信息如下表所示:
A | B | C | D | E | F | |
原子半徑/nm | 0.077 | 0.075 | 0.074 | 0.099 | ||
主要 化合價 | +4 -4 | +5 -3 | -2 | +6 -2 | ||
其他 | 一種同位素原子無中子 | 所有有機物中一定含有的元素 | 簡單氫化物常用作制冷劑 | 短周期主族元素中原子半徑最大 |
回答下列問題(用相應化學用語):
(1)G在周期表中的位置是___,F的簡單離子結構示意圖是___。
(2)由A、C、G三種元素形成的原子個數比為4:1:1的化合物的電子式為___,該化合物所含的化學鍵有___。(填化學鍵類型)
(3)D、E、F、G簡單離子半徑由小到大順序___。
(4)用電子式表示BD2的形成過程___。
(5)C、D、F的簡單氫化物中沸點由高到低的順序是___。
(6)寫出E2D2和A2D反應的化學方程式___,該反應每消耗1molE2D2電子轉移數目為___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com