
【題目】下列各組微粒在指定溶液中能大量共存的是( )
A.pH=1的溶液中:CH3CH2OH、Cr2O![]() 、K+、SO
、K+、SO![]()
B.c(Ca2+)=0.1molL-1的溶液中:NH![]() 、C2O
、C2O![]() 、Cl-、Br-
、Cl-、Br-
C.加入鋁粉放出大量H2的溶液:Fe2+、Na+、Cl-、NO![]()
D.含大量HCO![]() 的溶液中:C6H5O-、CO
的溶液中:C6H5O-、CO![]() 、Br-、K+
、Br-、K+
 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源: 題型:
【題目】已知室溫時,0.1mol·L-1某一元酸HA的電離平衡常數約為1×10-7,下列敘述錯誤的是( )
A. 該溶液的pH=4
B. 此溶液中,HA約有0.1%發生電離
C. 加水稀釋,HA的電離平衡向右移動,HA的電離平衡常數增大
D. 由HA電離出的c(H+)約為水電離出的c(H+)的106倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A~G是幾種烴的分子球棍模型,據此回答下列問題:
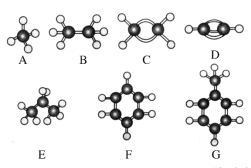
(1)常溫下含碳量最高的氣態烴是___(填對應字母);
(2)A分子的空間構型是___;
(3)G的一氯代物有___種;E的二氯代物有___種;
(4)寫出C與溴的四氯化碳溶液反應的化學方程式__,反應類型為___。
(5)寫出F與濃硝酸和濃硫酸反應的化學方程式___,反應類型為___。
現有上面A、B、C三種有機化合物:(以下均用結構簡式作答)
(6)同狀況、同體積的以上三種物質完全燃燒時耗去O2的量最多的是___。
(7)等質量的以上三種物質燃燒時,生成二氧化碳最多的是___,生成水最多的是___。
(8)在120℃、1.01×105Pa時,有兩種氣態烴和足量的氧氣混合點燃,相同條件下測得反應前后氣體體積沒有發生變化,這兩種氣體是__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】MnCO3是信息產業和機電工業的重要基礎功能材料,某地有含錳礦石(主要成分是MnO2還含CaO、Al2O3、FeS等雜質),由此礦石生產MnCO3的工藝流程如下:
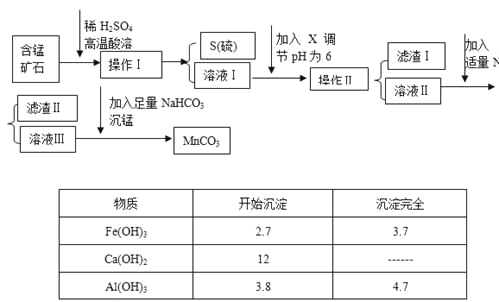
回答下列問題:
(1)操作Ⅰ為:___________。
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血紅色,試寫出酸溶過程中FeS發生反應的離子方程式:
(3)調節溶液pH所用物質X最好為(_______)
A.NaOH溶液 | B.氨水 | C.MnCO3固體 | D.鹽酸 |
(4)濾渣Ⅰ為___________,濾渣Ⅱ為___________。
(5)沉錳的化學方程式為:______________________。
(6)MnCO3也是制造鋰離子電池的重要原料,在此電池的正極,充放電過程中發生LiMn2O4與Li1-xMn2O4之間的轉化,寫出該電池充電時正極發生的反應式:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】己烯雌酚是一種激素類藥物,其結構簡式如圖所示。下列有關敘述中不正確的是( )
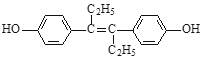
A. 己烯雌酚的分子式為C18H20O2
B. 己烯雌酚分子中一定有16個碳原子共平面
C. 己烯雌酚為芳香族化合物
D. 己烯雌酚可發生加成、取代、氧化、加聚、酯化、硝化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下反應![]() 在一密閉容器中進行,測得平均反應速率v(C)=2v(B)。若該反應過程中氣體的物質的量一直保持不變,則m、n、p、q可能依次是( )
在一密閉容器中進行,測得平均反應速率v(C)=2v(B)。若該反應過程中氣體的物質的量一直保持不變,則m、n、p、q可能依次是( )
A.2、6、3、5B.3、1、2、2C.2、1、2、1D.1、3、2、2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在室溫下,向Cu(IO3)2飽和溶液中加入足量的經稀硫酸酸化的KI溶液,產生CuI沉淀,溶液由藍色變為棕黃色,反應前加入淀粉溶液不變藍,反應后加入淀粉溶液變為藍色。
(1)該反應中氧化劑是 ______ ;
(2)該反應的還原產物是 ______ ;
(3)1 mol氧化劑在反應中得到電子的物質的量為 ______ ;
(4)某反應體系中有物質:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4請將NaBiO3之外的反應物與生成物分別填入以下空格內,配平化學計量數,并在氧化劑與還原劑之間標出電子轉移的方向和數目。
_________NaBiO3+_____ ________ + _____ ________→_____ _______ + ______ ________+ ______ _______+ ______ _______。
_____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】E、G、M、Q、T是五種原子序數依次增大的前四周期元素。E、G、M是位于p區的同一周期的元素,M的價層電子排布為ns2np2n,E與M原子核外的未成對電子數相等;QM2與GM2具有相等的價電子總數;T為過渡元素,其原子核外沒有未成對電子。請回答下列問題:
(1)T元素原子的價電子排布式是___。
(2)E、G、M三種元素的第一電離能由大到小的順序為___(用元素符號表示),其原因為___。
(3)G的最簡單氫化物的分子立體構型名稱為___,M的最簡單氫化物的分子中中心原子的雜化類型為___。M和Q的最簡單氫化物的沸點大小順序為___(寫化學式)。
(4)TQ在熒光體、光導體材料、涂料、顏料等行業中應用廣泛。立方TQ晶體結構如圖所示,該晶體的密度為pg·cm3。如果TQ的摩爾質量為Mg·mol1,阿伏加德羅常數為NAmol1,則a、b之間的距離為___cm。
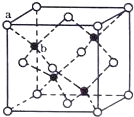
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知氫氣和碳燃燒的熱化學方程式為:
①2H2(g)+O2(g)=2H2O(l) △H1=-akJ·mol-1
②H2(g)+1/2O2(g)=H2O(g) △H2=-bkJ·mol-1
③C(s)+1/2O2(g)=CO(g) △H3=-ckJ·mol-1
④C(s)+O2(g)=CO2(g) △H4=-dkJ·mol-1
下列說法錯誤的是
A. 氫氣的燃燒熱為△H=-akJ·mol-1
B. c<d
C. 一氧化碳的燃燒熱為△H=-(d-c)kJ·mol-1
D. 0.5a>b
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com