
34ĪóÅ═┴ĢĢrŻ¼šn╠├╔Ž└ŽÄ¤ę²ī¦╬ęéā╗žŅÖ┴╦Č■éĆ╠ĮŠ┐īŹ“ׯ«
╠ĮŠ┐1Ż║į┌īŹ“×╩ęū÷╦ß║═ēA┼cųĖ╩Šä®Ę┤æ¬Ą─īŹ“ׯ¼╦∙ė├įćä®╚ńłD╦∙╩ŠŻ¼īŹ“×║¾░čÅUę║╝»ųąĄ╣╚ļÅUę║ĖūųąŻ«
Ż©1Ż®ÅUę║│╩╝t╔½Ż¼šf├„ÅUę║’@
╦ß
ąįŻ╗
Ż©2Ż®īæ│÷ÅUę║ųą╦∙║¼╚▄┘|Ą─╗»īW╩Į
NaClĪóCaCl2ĪóHCl
Ż«
╠ĮŠ┐2Ż║─│īW┴ĢąĪĮMĄ─╚²╬╗═¼īW×ķ┴╦£yČ©H
2SO
4┼cNaOH░l╔·ųą║═Ę┤æ¬ĢrĘ┼│÷Ą─¤ß┴┐Ż¼╦¹éāį┌Ž┬łD╦∙╩ŠĄ─ąĪ¤²▒Łųąčb╚ļę╗Č©┴┐Ą─NaOH╚▄ę║Ż¼£yŲõ£žČ╚Ż╗┴Ē╚Īę╗Č©┴┐Ą─┴“╦ß╚▄ę║Ż¼£yŲõ£žČ╚║¾Ż¼į┘ŠÅŠÅĄžāA╚ļąĪ¤²▒ŁųąŻ¼▓ó▀ģ╝ė▀ģė├Łhą╬▓Ż┴¦░¶╔ŽŽ┬ęŲäėöć░ĶŻ¼ėøõø╚▄ę║£žČ╚Ą─ūā╗»Ż«╝ūĪóęęĪó▒¹╚²╬╗
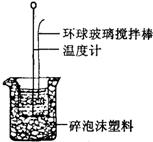
═¼īWīŹ“×Ģr▀xō±Ą─įćä®ŪķøręŖ▒ĒŻ║
|
|
╩╣ė├Ą─NaOHŪķør |
╩╣ė├Ą─H2SO 4Ūķør |
|
╝ū |
NaOH╣╠¾w |
ŽĪH 2SO 4 |
|
ęę |
NaOHŽĪ╚▄ę║ |
ØŌH2SO4 |
|
▒¹ |
NaOHŽĪ╚▄ę║ |
ŽĪH2SO4 |
Ż©1Ż®║å┤Ž┬┴ąå¢Ņ}Ż║
ó┘▓Ż┴¦░¶Ž┬Č╦×ķ╩▓├┤ę¬ū÷│╔Łhą╬Ż┐
▒Ńė┌▓Ż┴¦░¶╔ŽŽ┬ęŲäėŠ═─▄öć░Ķ╚▄ę║Ż¼Ę└ų╣ŲŲē─£žČ╚ėŗ
Ż╗
ó┌╦ķ┼▌─Ł╦▄┴ŽĄ─ū„ė├╩Ū╩▓├┤Ż┐
Ė¶¤ßŻ¼Ę└ų╣¤ß┴┐╔ó╩¦
Ż«
Ż©2Ż®╝ūĪóęęĪó▒¹╚²╬╗═¼īWųąŻ¼ėąā╔╬╗═¼īW▀xō±Ą─įćä®ėąÕeš`Ż«Å─╚▄ę║£žČ╚Ė─ūāĄ─ę“╦ž
┐╝æ]Ż¼ųĖ│÷Õeš`Ą─įŁę“╩ŪŻ║
ó┘═¼īWÕeš`Ą─įŁę“╩Ū
NaOH╣╠¾w╚▄ė┌╦«Ģ■Ę┼¤ßŻ¼ė░ĒæĘ┤æ¬¤ßĄ─£yČ©
Ż╗
ó┌═¼īWÕeš`Ą─įŁę“╩Ū
ØŌH2SO4╚▄ė┌╦«Ģ■Ę┼¤ßŻ¼ė░ĒæĘ┤æ¬¤ßĄ─£yČ©
Ż«
Ż©3Ż®┴Ēę╗╬╗╗žīW▀xō±Ą─įć䮚²┤_Ż¼Ą½ė├╔Ž╩÷īŹ“×ĘĮĘ©£yĄ├Ą─ųą║═¤ßöĄųĄČ╝Ģ■Ų½ąĪŻ¼įćĘų╬÷┐╔─▄įņ│╔š`▓ŅĄ─įŁę“Ż║
ąĪ¤²▒Ł╬┤╝ė╔wŻ¼¤ß┴┐╔ó╩¦╗“Ę┤æ¬╬’┴┐╠½╔┘Ż©Ųõ╦¹║Ž└Ē┤░ĖŠ∙┐╔Ż®
Ż«


 Ż¼šłå¢į┌╗»īWĘ┤æ¬ųąŌcįŁūėęū
Ż¼šłå¢į┌╗»īWĘ┤æ¬ųąŌcįŁūėęū




 34ĪóÅ═┴ĢĢrŻ¼šn╠├╔Ž└ŽÄ¤ę²ī¦╬ęéā╗žŅÖ┴╦Č■éĆ╠ĮŠ┐īŹ“ׯ«
34ĪóÅ═┴ĢĢrŻ¼šn╠├╔Ž└ŽÄ¤ę²ī¦╬ęéā╗žŅÖ┴╦Č■éĆ╠ĮŠ┐īŹ“ׯ« ═¼īWīŹ“×Ģr▀xō±Ą─įćä®ŪķøręŖ▒ĒŻ║
═¼īWīŹ“×Ģr▀xō±Ą─įćä®ŪķøręŖ▒ĒŻ║