
【題目】(1)NA表示阿伏加德羅常數的數值.46g NO2和N2O4的混合氣體中含有_____NA個氧原子;2L0.6 mol·L1 Fe(NO3)3溶液中含_____NA個NO3—離子.
(2)三氟化氮(NF3)是一種氣體,它是微電子工業技術的關鍵原料之一,三氟化氮在潮濕的空氣中與水蒸氣能發生氧化還原反應,其反應的產物有:HF、NO和HNO3。
①寫出該反應的化學方程式_________________________________
②三氟化氮可由氨氣和氟氣反應得到:4NH3+3F2NF3+3NH4F;據題意推測NF3,F2,NO三種氣體中,氧化性由強到弱的順序為________________________
(3)H2C2O4溶液和KMnO4酸性溶液可發生反應:___H2C2O4+___MnO4﹣+___H+→___CO2↑+___Mn2++___H2O,反應中每生成標況下4.48L CO2氣體,外電路中通過的電子的物質的量為___________mol.
(4)氨和聯氨(N2H4)是氮的兩種常見化合物,制備聯氨可用丙酮為催化劑,將次氯酸鈉與氨氣反應,該反應中還原劑與氧化劑的物質的量之比為2∶1,寫出該反應的化學方程式_______。
【答案】23.63NF3+5H2O===2NO+HNO3+9HFF2、NF3、NO52610280.2NaClO+2NH3===N2H4+H2O+NaCl
【解析】
(1)NO2和N2O4的最簡式相同,NA表示阿伏加德羅常數的數值,46g NO2和N2O4的混合氣體中含有氧原子=![]() ×2×NA/mol=2NA,2L 0.6mol/L Fe(NO3)3溶液中含硝酸根離子=2L×0.6mol/L×3×NA/mol=3.6NA,故答案為:2;3.6;(2)①三氟化氮在潮濕的空氣中與水蒸氣能發生氧化還原反應,其反應的產物有:HF、NO和HNO3,N元素化合價由+3價變為+2價、+5價,由電子、原子守恒可知反應為:3NF3+5H2O═2NO+HNO3+9HF;②4NH3+3F2=NF3+3NH4F中,F元素的化合價降低,F2為氧化劑,氧化劑的氧化性大于氧化產物的氧化性,則氧化性為F2>NF3,結合①中分析可知,氧化性由強弱的順序為F2、NF3、NO;(3)H2C2O4中C元素的化合價為+3價,二氧化碳分子中C的化合價為+4價,化合價至少升高2價;MnO4﹣中Mn元素的化合價為+7,反應后變為+2價的Mn2+,化合價降低5價,化合價變化的最小公倍數為10,則MnO4﹣的系數為2,H2C2O4的系數為5,然后利用觀察法配平為:5H2C2O4+2MnO4﹣+6H+=10CO2+2Mn2++8H2O;標準狀況下4.48L二氧化碳的物質的量為:
×2×NA/mol=2NA,2L 0.6mol/L Fe(NO3)3溶液中含硝酸根離子=2L×0.6mol/L×3×NA/mol=3.6NA,故答案為:2;3.6;(2)①三氟化氮在潮濕的空氣中與水蒸氣能發生氧化還原反應,其反應的產物有:HF、NO和HNO3,N元素化合價由+3價變為+2價、+5價,由電子、原子守恒可知反應為:3NF3+5H2O═2NO+HNO3+9HF;②4NH3+3F2=NF3+3NH4F中,F元素的化合價降低,F2為氧化劑,氧化劑的氧化性大于氧化產物的氧化性,則氧化性為F2>NF3,結合①中分析可知,氧化性由強弱的順序為F2、NF3、NO;(3)H2C2O4中C元素的化合價為+3價,二氧化碳分子中C的化合價為+4價,化合價至少升高2價;MnO4﹣中Mn元素的化合價為+7,反應后變為+2價的Mn2+,化合價降低5價,化合價變化的最小公倍數為10,則MnO4﹣的系數為2,H2C2O4的系數為5,然后利用觀察法配平為:5H2C2O4+2MnO4﹣+6H+=10CO2+2Mn2++8H2O;標準狀況下4.48L二氧化碳的物質的量為:![]() =0.2mol,H2C2O4中C元素的化合價為+3價,二氧化碳分子中C的化合價為+4價,則生成0.2mol二氧化碳轉移的電子的物質的量為:0.2mol×(4﹣3)=0.2mol,故答案為:5;2;6;10;2;8;0.2;
=0.2mol,H2C2O4中C元素的化合價為+3價,二氧化碳分子中C的化合價為+4價,則生成0.2mol二氧化碳轉移的電子的物質的量為:0.2mol×(4﹣3)=0.2mol,故答案為:5;2;6;10;2;8;0.2;
(4)制備肼的方法,是以NaClO氧化NH3,反應中還原劑與氧化劑的物質的量之比為2:1,制得肼的稀溶液,反應方程式為:NaClO+2NH3═N2H4+H2O+NaCl。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】甲是一種常見的單質,乙、丙為中學常見的化合物,甲、乙、丙均含有元素 X 。它們有如下的轉化關系(部分產物及反應條件已略去),下列判斷正確的是:
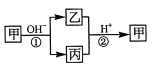
A. X元素可能為Al B. X 元素不一定為非金屬元素
C.反應①和②互為可逆反應 D.反應①和②一定為氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是
A. 碳酸鈣與鹽酸反應:CO32-+2H+![]() CO2↑+H2O
CO2↑+H2O
B. 氯化鋁溶液中加入過量氨水:Al3++3NH3·H2O![]() Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+
C. 硫酸和氫氧化鋇溶液反應:Ba2++SO42-![]() BaSO4↓
BaSO4↓
D. 鐵釘放入硫酸銅溶液中:2Fe+3Cu2+![]() 2Fe3++3Cu
2Fe3++3Cu
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某新型電池,以NaBH4(B的化合價為+3價)和H2O2作原料,負極材料采用Pt,正極材料采用MnO2(既作電極材料又對該極的電極反應具有催化作用),該電池可用作衛星、深水勘探等無空氣環境電源,其工作原理如圖所示。下列說法不正確的是

A. 每消耗3mol H2O2,轉移6mol e﹣
B. 電池工作時Na+從b極區移向a極區
C. a極上的電極反應式為:BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2O
D. b極材料是MnO2,該電池總反應方程式:NaBH4 + 4H2O2===NaBO2 + 6H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現用98%濃硫酸(密度1.84 g·cm3)配制濃度為0.5 mol·L1稀硫酸500mL.
(1)選用的主要儀器有:_________、________、__________、_______、
__________;
(2)請將下列操作按照正確的序號填在橫線上___
A.用量筒量取濃硫酸
B.反復顛倒搖勻
C.用膠體滴管加水至刻度
D.洗凈燒杯內壁和玻璃棒,并將洗液轉至容量瓶
E.稀釋濃硫酸
F.將溶液轉入容量瓶
(3)所需濃硫酸的體積為______mL.
(4)將濃硫酸沿著燒杯內壁慢慢注入盛水的燒杯中,不斷攪拌的目的是______;若攪拌過程中有液體濺出,會使最終結果______(填偏高、偏低或無影響)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在某無色溶液中緩慢地滴入NaOH溶液直至過量,產生沉淀的質量與加入的NaOH溶液體積的關系如右圖所示,由此確定,原溶液中含有的陽離子是
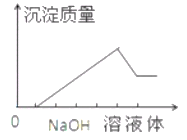
A. Mg2+、Al3+、Fe3+ B. H+、Mg2+、Al3+
C. H+、Ba2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列分離物質的方法正確的是( )
A.用萃取的方法除去花生油中的水分
B.用過濾的方法除去NaCl溶液中含有的少量KNO3
C.用酒精萃取碘水中的碘
D.用蒸餾的方法除去水中的不揮發性雜質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下有關焊錫(錫和鉛)的結論正確的是( )
A.焊錫的熔點比錫和鉛的熔點低
B.焊錫的熔點比錫和鎘的熔點低
C.焊錫的熔點比錫和鉍熔點低
D.焊錫的熔點比鉛、錫的熔點都高
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com