
【題目】化學與生活密切相關。下列生活中常見物質的俗名與化學式相對應的是
A.純堿— NaOHB.漂白粉— NaClO
C.大理石— CaCO3D.燒堿— Na2CO3
 智趣寒假作業云南科技出版社系列答案
智趣寒假作業云南科技出版社系列答案科目:高中化學 來源: 題型:
【題目】一碳化學是指以分子中只含一個碳原子的化合物(如一氧化碳、二氧化碳、甲烷、甲醇等)為原料,用化工的方法制造產品的化學體系的總稱。我國能源比較豐富,煤的探明儲量6000億噸,居世界第三位,因此,發展一碳化學有著優越的條件和光明的前途。請回答下列有關問題。
(1)已知在一定溫度下有如下反應:
I.C(s)+CO2(g)![]() 2CO(g)H1=akJ/mol
2CO(g)H1=akJ/mol
II.CO(g)+H2O(g)![]() H2(g)+CO2(g)△H2=bkJ/mol
H2(g)+CO2(g)△H2=bkJ/mol
III.C(s)+H2O(g)![]() CO(g)+H2(g)△H3________。
CO(g)+H2(g)△H3________。
(2)在一恒容的密閉容器中,加入lmolCO(g)、2molH2O(g),發生反應CO(g)+H2O(g)![]() H2(g)+CO2(g) △H ,CO的平衡轉化率隨溫度的變化如圖所示:
H2(g)+CO2(g) △H ,CO的平衡轉化率隨溫度的變化如圖所示:

①該反應的△H__0(填“<”或“>”。)
②在某溫度下,能判斷該反應是否達到化學平衡狀態的依據是________。
a.混合氣體中c(CO)不變 b.c(CO)=c(CO2)
c.υ正(H2O)=υ逆(H2) d.混合氣體的平均相對分子質量不變
③A點時H2O(g)的轉化率為__________。
④在體積不變時,要增大該反應的正反應速率可采取的措施是_______(寫兩條)。
⑤A點時該反應的平衡常數為________(保留到小數點后兩位)。
⑥若在該容器中充入2molCO和3mol水蒸氣進行反應,達到平衡時水蒸氣的體積分數與H2的體積分數相等,則平衡后CO的體積分數為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近年科學家提出“綠色自由”構想。把含有大量CO2的空氣吹入K2CO3溶液中,再把CO2從溶液中提取出來,并使之與H2反應生成可再生能源甲醇。其工藝流程如下圖所示:
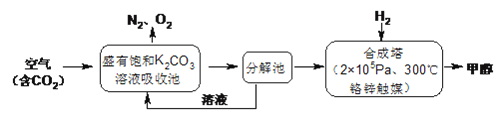
回答下列問題:
(1)進入分解池中主要物質是______;在合成塔中,若足量的H2與CO2反應,消耗4.4gCO2,生成氣態的H2O和CH3OH,可放出5370J的熱量,寫出該反應的熱化學方程式________。
(2)該工藝在哪些方面體現了“綠色自由”構想中的“綠色”: ①_______;②_______。
(3)一定條件下,往2L恒容密閉容器中充入1.0molCO2和3.0mol H2,在不同催化劑作用下,相同時間內CO2的轉化率隨溫度變化如圖所示:
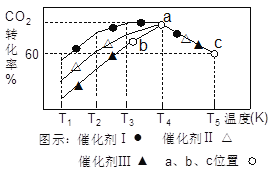
①催化劑效果最佳的是_______(填“催化劑I”.“催化劑Ⅱ”,“催化劑Ⅲ”)。b點v(正)______v(逆)(填“>”,“<”,“=”)。
②此反應在a點時已達平衡狀態,a點的轉化率比c點高的原因是_________。c點時該反應的平衡常數K=___________(保留一位小數)。
(4)科學家還研究了利用溫室氣體制造充電電池,下圖為正在研究的Na—CO2可充電電池示意圖,該裝置放電時的總反應方程式為_________。
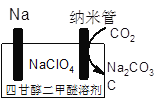
(5)己知25℃時H2CO3的電離平衡常數為:Kal =4.4×10-7、Ka2 =4.7×l0-ll,則反應:HCO3-+H2O![]() H2CO3+ OH-的平衡常數K=________。
H2CO3+ OH-的平衡常數K=________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( ) 
A.圖①中△H1=△H2+△H3
B.圖②可用于證明實驗中生成了乙烯
C.圖③表示醋酸溶液滴定NaOH和氨水混合溶液的電導率變化曲線
D.圖④可表示由CO(g)生成CO2(g)的過程中要放出566kJ 熱量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】聚對苯二甲酸二烯丙酯(PDAP)是一種優良的熱固性樹脂,這種材料可以采取下列路線合成:

已知:

(1)F的分子式是________;C的化學名稱是_________。
(2)反應④的類型是________;反應條件是________。
(3)寫出反應③的化學方程式________________。
(4)D的結構簡式是________。
(5)G是E的同分異構體,G具有如下性質:①能發生銀鏡反應,且1 mol G與銀氨溶液反應時最多可得到4 mol Ag;②遇FeCl3溶液呈紫色;③在稀硫酸中能發生水解反應。則符合上述條件的G最多有________種,這些不同結構的物質,它們的核磁共振氫譜峰的數目有何特點?__________________。
(5)試仿照題目中合成流程圖的形式,完成![]() 這一合成流程_______________________。
這一合成流程_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】燃料電池利用原電池的工作原理將燃料和氧化劑(如O2)反應所放出的化學能直接轉化為電能:能有效提高能源利用率,具有廣泛的應用前景。某種燃料電池的總反應式是:CH4+2O2+2OH-=CO32-+ 3H2O,裝置如下圖所示,該電池用金屬鉑片作電極在兩極上分別通甲烷和氧氣。請思考回答以下問題:
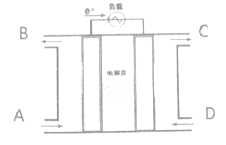
(1)電解質溶液可能是_________________;陽離子的移動方向:___________。(“左→右”、“右→左”)
(2)D氣體通入的電池的_________極,發生的電極反應式:__________________;A通入的是______________,發生的電極反應式:_________________。
(3)當該電子流經導線的電子為4mol時,A入口至少需要通入_______L的氣體(標準狀態下)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com