
【題目】地球上的海水中蘊藏了大約40萬億噸氘。從1升海水里提取的氘,在聚變反應中所釋放的能量,相當于燃燒300升汽油。如果把自然界的氘和氚全部用于聚變反應,釋放出來的能量足夠人類使用100億年。與核裂變相比,氘和氚的聚變能是一種安全、不產生放射性物質、原料成本低廉的能源。同溫同壓下有等質量的H2、D2、T2三種氣體,下列敘述正確的是
①密度之比為1∶2∶3 ②質子數之比為6∶3∶2 ③中子數之比為0∶6∶8 ④體積之比為6∶3∶2
A.①②③④B.只有①②C.只有③④D.只有②④
【答案】A
【解析】
同質量的H2、D2、T2的的物質的之比為:![]() :
:![]() :
:![]() ,即6:3:2,則:
,即6:3:2,則:
①根據阿伏加德羅定律及其推論可知,在相同條件下,氣體的密度之比等于相應的相對分子質量之比,H2、D2、T2的相對分子質量之比為1:2:3,則它們的密度之比為1:2:3,①正確;
②H2、D2、T2分子的質子數分別為2、2、2,則等質量的情況下,它們的質子數比為6:3:2,②正確;
③H2、D2、T2分子的中子數分別為0、2、4,則等質量的情況下,它們的質子數比為0:6:8,③正確;
④在相同條件下,氣體的體積之比等于其物質的量之比,故它們的體積之比為6:3:2,④正確;
綜上所述,①②③④正確,故選A。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】將一定量純凈的氨基甲酸銨置于密閉真空恒容容器中(固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡: ![]() ,
,![]() 。然后在恒定溫度下縮小容器體積,重新達到平衡。下列分析正確的是
。然后在恒定溫度下縮小容器體積,重新達到平衡。下列分析正確的是
A. 若![]() ,則該反應達到平衡狀態
,則該反應達到平衡狀態
B. 兩次平衡時,后一次平衡時![]() 的濃度大
的濃度大
C. 重新達到平衡,密閉容器中氨氣的體積分數不變
D. 若開始時向容器中加人2molNH3和1molCO2,則達到平衡時放出akJ熱量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用如下圖所示裝置探究碳酸和苯酚的酸性強弱,下列敘述不正確的是(部分夾持儀器省略)
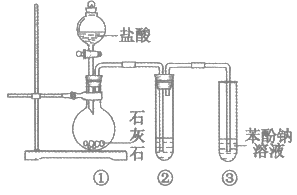
A. 打開分液漏斗旋塞,①中產生無色氣泡,③中出現白色渾濁
B. ②中試劑為飽和NaHCO3溶液
C. ③中發生反應的化學方程式是![]()
D. 苯酚有弱酸性,是由于苯基影響了與其相連的羥基的活性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某固體A在一定條件下加熱分解,產物都是氣體。分解的方程式為:2A=B↑+2C↑+2D↑。測得生成的混合氣體對H2的相對密度為d,則A的相對分子質量為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素R、T、Q、W在元素周期表中的相對位置如圖所示,其中T所處的周期序數與族序數相等。下列判斷不正確的是
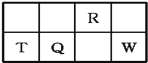
A.最簡單氣態氫化物的熱穩定性:R>Q
B.最高價氧化物對應水化物的酸性:Q<W
C.原子半徑:T>Q>R
D.T、Q、W最高價氧化物對應的水化物均能與R的最高價氧化物對應的水化物發生反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,①pH=3的醋酸和②0.01mol·L-1NaOH溶液兩種溶液中,由水電離產生的氫離子濃度之比(①∶②)是( )
A.1∶10B.1∶4C.10∶1D.無法計算
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素X的某價態離子Xn+中所有電子正好充滿K、L、M三個電子層,它與N3-形成晶體的晶胞結構如圖所示。下列說法錯誤的是( )
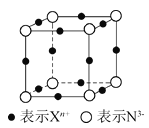
A.X元素的原子序數是19
B.該晶體中陽離子與陰離子個數比為3∶1
C.Xn+中n=1
D.晶體中每個Xn+周圍有2個等距離且最近的N3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Na2O2可用作漂白劑和呼吸面具中的供氧劑
(1)某學習小組發現:在盛有Na2O2的試管中加入足量水,固體完全溶解,并立即產生大量氣泡,當氣泡消失后,向其中滴入1~2滴酚酞溶液。此時再向試管中加入少量MnO2粉末,又有氣泡產生,該氣體能使帶火星的木條復燃。
①寫出Na2O2在呼吸面具中作供氧劑的兩個化學反應方程式__________,__________;
②滴入酚酞溶液后看到的現象是________;
③已知MnO2作為催化劑,則加入MnO2反應的化學方程式為_____;
(2)Na2O2有強氧化性,H2具有還原性,有同學猜想Na2O2與H2能反應。為了驗證此猜想,該小組同學進行如下實驗,實驗步驟和現象如下:
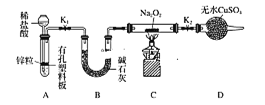
步驟1:按如圖組裝儀器(圖中夾持儀器省略),裝入藥品。
步驟2:打開K1、K2,產生的氣體流經裝有Na2O2的硬質玻璃管,一段時間后沒有任何現象。
步驟3:開始加熱,觀察到硬質玻璃管內Na2O2開始熔化,淡黃色的粉末變成了白色固體,干燥管內硫酸銅未變藍色。
步驟4:反應后撤去酒精燈,待硬質玻璃管冷卻后關閉K1。
(提示:B裝置的作用是吸收A裝置中揮發的HCl氣體和水蒸氣。)
①步驟1組裝好儀器之后,裝入藥品之前,應________。
②A裝置中添加稀鹽酸的儀器名稱是_____,A裝置中發生反應的離子方程式為______。
③步驟3在點燃C處酒精燈前必須進行的操作是________;④你得到的結論是______ (若能反應請用化學方程式表示);
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:①1mol晶體硅中含有2molSi—Si鍵。
②Si(s)+O2(g)===SiO2(g) ΔH,其反應過程與能量變化如圖所示。
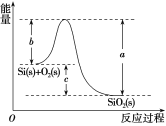
③
化學鍵 | Si—O | O=O | Si—Si |
斷開1 mol共價鍵所需能量/kJ | 460 | 500 | 176 |
下列說法中正確的是( )
A.晶體硅光伏發電是將化學能轉化為電能B.二氧化硅穩定性小于硅的穩定性
C.ΔH=-988kJ·mol-1D.ΔH=(a-c)kJ·mol-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com