
【題目】如圖是用0.1 mol·L-1 NaOH溶液分別滴定20 mL濃度均為0.1 mol·L-1的不同一元酸的滴定曲線(圖中曲線由上向下依次是氫氰酸、醋酸、氫氟酸、鹽酸),下列說法錯誤的是
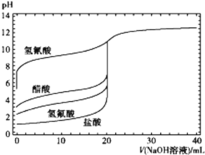
A.酸性:HF>CH3COOH>HCN
B.當加入10 mL NaOH溶液時,c(CN-)>c(CH3COO-)
C.用NaOH溶液滴定醋酸時,應用酚酞作指示劑不能使用甲基橙
D.隨NaOH溶液滴入,CH3COOH溶液中水的電離程度先變大后變小
【答案】B
【解析】
A. 相同條件下,相同濃度的三種酸,溶液的pH:HF<CH3COOH<HCN,pH越小,酸性越強,所以酸性:HF>CH3COOH>HCN,故A正確;
B. HCN的酸性小于CH3COOH,相同濃度時,HCN的電離程度小,溶液中CN-的濃度小,所以溶液中c(CN-)<c(CH3COO-),故B錯誤;
C. NaOH與醋酸反應生成CH3COONa,溶液顯堿性,應該選擇在堿性條件下變色的指示劑,所以選擇酚酞,故C正確;
D. 隨NaOH溶液的滴入,CH3COOH溶液中氫離子濃度減小,對水的抑制程度減小,當氫氧化鈉過量,NaOH會抑制水的電離,水的電離程度減小,所以CH3COOH溶液中水的電離程度先變大后變小,故D正確。
故答案為B。


 孟建平錯題本系列答案
孟建平錯題本系列答案 超能學典應用題題卡系列答案
超能學典應用題題卡系列答案科目:高中化學 來源: 題型:
【題目】藥物中間體M的合成路線流程圖如圖:

已知:

 (R、R’、R”為H或烴基)
(R、R’、R”為H或烴基)
請回答下列問題:
(1)A為芳香烴,名稱為___。
(2)化合物C含有的官能團名稱為__。
(3)下列說法中正確的是__。
A.化合物A只有1種結構可以證明苯環不是單雙鍵交替的結構
B.可利用酸性KMnO4溶液實現A→B的轉化
C.化合物C具有弱堿性
D.步驟④、⑤、⑥所屬的有機反應類型各不相同
(4)步驟⑥可得到一種與G分子式相同的有機副產物,其結構簡式是__。
(5)有機物H與氫氣加成的產物J存在多種同分異構體。寫出一種同時符合下列條件的同分異構體的結構簡式__。
①能與FeCl3溶液發生顯色反應;
②核磁共振氫譜檢測表明分子中有4種化學環境不同的氫原子。
(6)寫出I+G→M的化學方程式(可用字母G和M分別代替物質G和M的結構簡式)__。
(7)設計以![]() 和CH3CH2OH為原料制備
和CH3CH2OH為原料制備![]() 的合成路線流程圖_____(無機試劑任選)。
的合成路線流程圖_____(無機試劑任選)。
合成路線流程圖示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列與金屬腐蝕有關的說法,正確的是


A.圖1中,插入海水中的鐵棒,越靠近底端腐蝕越嚴重
B.圖2中,插入溶液中的鐵棒容易溶解,主要是發生電化學腐蝕
C.圖3中,燃氣灶的中心部位容易生銹,主要是由于高溫下鐵發生電化學腐蝕
D.圖4中,用犧牲鎂塊的方法來防止地下鋼鐵管道的腐蝕,鎂塊相當于原電池的負極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在有機物的分子中,當碳原子連有4個不同的原子或原子團時,這種碳原子稱為“手性碳原子”,在其旁邊標有*號。凡具有一個手性碳原子的化合物一定具有光學活性。如圖有機物含有一個手性碳原子,具有光學活性,當發生下列化學反應,生成的新有機物無光學活性的是( )
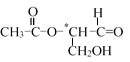
A.與氫氧化鈉水溶液共熱反應B.與新制銀氨溶液共熱反應
C.與甲酸在一定條件下發生酯化反應D.與H2發生加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對已達化學平衡的反應 2X(g)+Y(g)![]() 2Z(g) ΔH<0 下列說法正確的是
2Z(g) ΔH<0 下列說法正確的是
A.減小壓強,逆反應速率增大,正反應速率減小,平衡向逆方向移動
B.升高溫度,正、逆反應速率均增大,平衡向逆方向移動
C.除去部分的Z,正反應速率增大,逆反應速率減小,平衡向正方向移動
D.加入正催化劑,正、逆反應速率均增大,平衡向正方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組物質中,不能按![]() (“→”表示一步完成)的關系相互轉化的是 ( )
(“→”表示一步完成)的關系相互轉化的是 ( )
選項 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | Cl2 | NaClO | NaCl |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】天津是我國研發和生產鋰離子電池的重要基地。鋰離子電池正極材料是含鋰的二氧化鈷(LiCoO2),充電時LiCoO2![]() 中Li被氧化,Li+遷移并以原子形式嵌入電池負極材料碳(C6)中,以LiC6表示。電池反應LiCoO2+C6
中Li被氧化,Li+遷移并以原子形式嵌入電池負極材料碳(C6)中,以LiC6表示。電池反應LiCoO2+C6![]() CoO2+LiC6,下列說法正確的是 ( )
CoO2+LiC6,下列說法正確的是 ( )
A.充電時,電池的負極反應為LiC6-e-=Li+C6
B.放電時,電池的正極反應為CoO2+Li2++e-=LiCoO2
C.羧酸、醇等含活潑氫的有機物可用作鋰離子電池的電解質
D.鋰離子電池的比能量(單位質量釋放的能量)低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,H2(g)+CO2(g)![]() H2O(g)+CO2(g)的平衡常數
H2O(g)+CO2(g)的平衡常數![]() 。該溫度下在甲、乙、丙三個恒容密閉容器中,
。該溫度下在甲、乙、丙三個恒容密閉容器中,
起始濃度 | 甲 | 乙 | 丙 |
c(H2)/mol | 0.010 | 0.020 | 0.020 |
c(CO2)/mol | 0.010 | 0.010 | 0.020 |
投入H2(g)和CO2(g),其起始濃度如表所示。下列判斷不正確的是( )
A.平衡時,乙中CO2的轉化率大于60%
B.平衡時,甲中和丙中H2的轉化率均是60%
C.平衡時,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反應開始時,丙中的反應速率最快,甲中的反應速率最慢
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在溶液中可以發生反應:X+2Y3+=2Y2++X2+,則下列敘述①X被氧化;②X是氧化劑;③X具有還原性;④Y2+是氧化產物;⑤Y2+具有還原性;⑥Y3+的氧化性比X2+的氧化性強。以下敘述中正確的是( )
A.②④⑥B.①③④C.①③⑤⑥D.②⑤
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com