
【題目】以氯化鈉和硫酸銨為原料制備氯化銨及副產品硫酸鈉的工藝流程如圖: 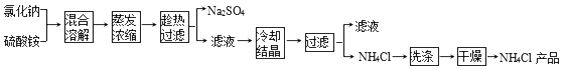
【查閱資料】
①上述流程所示物質中只有NH4Cl受熱易分解:NH4Cl ![]() NH3↑+HCl↑
NH3↑+HCl↑
②氯化銨和硫酸鈉的溶解度隨溫度變化曲線如圖所示: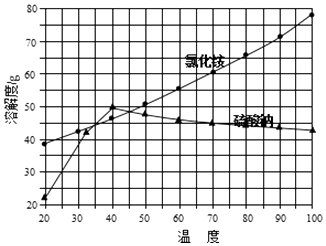
請回答下列問題:
(1)寫出氯化鈉和硫酸銨溶液混合得到硫酸鈉晶體的化學方程式: .
(2)欲制備10.7g NH4Cl,理論上需NaCl質量為g.
(3)實驗室進行蒸發結晶用到的主要儀器除鐵架臺、鐵圈、酒精燈外,還要有 .
(4)“冷卻結晶”過程中,析出NH4Cl晶體的合適溫度為 .
(5)不用其它試劑,檢查NH4Cl產品是否純凈的方法:
操作步驟 | 現象 | 結論 |
取少量氯化銨產品于試管底部, | 表明氯化銨產品純凈 |
【答案】
(1)(NH4)2SO4+2NaCl═2NH4Cl↓+Na2SO4
(2)11.7
(3)玻璃棒、燒杯、蒸發皿
(4)35℃
(5)加熱;如果試管底部沒有固體剩余
【解析】解:將氯化鈉和硫酸銨混合溶解,蒸發濃縮,根據溶解度曲線可知,在溫度較高時,硫酸鈉溶解度較小,所以趁熱過濾可得硫酸鈉固體,溶液中則主要為氯化銨,過濾得氯化銨溶液,將氯化銨溶液冷卻結晶,過濾得氯化銨固體,經洗滌干燥得氯化銨產品,(1)硫酸銨和氯化鈉相互交換離子生成硫酸鈉和氯化銨,反應方程式為(NH4)2SO4+2NaCl═2NH4Cl↓+Na2SO4,
故答案為:(NH4)2SO4+2NaCl═2NH4Cl↓+Na2SO4;(2)10.7g NH4Cl的物質的量為 ![]() =0.2mol,根據Cl元素守恒,需要NaCl的物質的量也為0.2mol,質量為0.2mol×58.5g/mol=11.7g,
=0.2mol,根據Cl元素守恒,需要NaCl的物質的量也為0.2mol,質量為0.2mol×58.5g/mol=11.7g,
故答案為:11.7;(3)實驗室進行蒸發結晶用到的主要儀器除鐵架臺、鐵圈、酒精燈外,還需要蒸發溶液的蒸發皿、盛放晶體的燒杯、攪拌用的玻璃棒,
故答案為:蒸發皿、燒杯、玻璃棒;(4)根據硫酸鈉的溶解度曲線不難看出,在低于40℃時,硫酸鈉的溶解度隨溫度的升高而增大,高于40℃時硫酸鈉的溶解度隨溫度的升高而減小;由兩物質的溶解度曲線不難看出,只有在35~45℃時,氯化銨的溶解度小于硫酸鈉的溶解度,
故答案為:35℃;(5)加熱條件下氯化銨分解生成氨氣和氯化氫,如果固體完全是氯化銨,則加熱后沒有固體剩余,如果有固體剩余就證明氯化銨不純凈,所以其檢驗方法為:取少量氯化銨產品于試管底部,加熱,如果試管底部沒有固體剩余,就說明氯化銨純凈,
故答案為:加熱;如果試管底部沒有固體剩余.
將氯化鈉和硫酸銨混合溶解,蒸發濃縮,根據溶解度曲線可知,在溫度較高時,硫酸鈉溶解度較小,所以趁熱過濾可得硫酸鈉固體,溶液中則主要為氯化銨,過濾得氯化銨溶液,將氯化銨溶液冷卻結晶,過濾得氯化銨固體,經洗滌干燥得氯化銨產品,(1)硫酸銨和氯化鈉相互交換離子生成硫酸鈉和氯化銨;(2)根據Cl元素守恒計算NaCl的質量;(3)實驗室進行蒸發結晶用到的主要儀器除鐵架臺、鐵圈、酒精燈外,還需要蒸發皿、玻璃棒、燒杯;(4)從溶解度曲線判斷硫酸鈉和氯化銨的溶解度變化特點分析,在35﹣45℃時,氯化銨的溶解度小于硫酸鈉的溶解度;(5)氯化銨分解生成氯化氫和氨氣,根據固體加熱是否有剩余固體確定氯化銨是否除凈.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下列關于有機物的說法正確的是( )
A.淀粉和油脂的水解都是高分子生成小分子的過程
B.2﹣甲基丙烷和異丁烷互為同系物
C.![]() 屬于取代反應
屬于取代反應
D.C3H4Cl2的鏈狀有機物的同分異構體有5種(不考慮立體異構)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】構造原理揭示的電子排布能級順序,實質是各能級能量高低。若以E(nl)表示某能級的能量,以下各式中正確的是( )
A. E(5s)>E(4f)>E(4s)>E(3d)
B. E(3d)>E(4s)>E(3p)>E(3s)
C. E(4s)<E(3s)<E(2s)<E(1s)
D. E(5s)>E(4s)>E(4f)>E(3d)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若將海水淡化作飲用水使用,下列方法在原理上完全不可行的是
A. 利用太陽能使海水蒸餾淡化
B. 加明礬使海水中的鹽分沉淀而淡化
C. 利用電滲析法可以獲取淡化的飲用水
D. 將海水通過離子交換樹脂,以除去所含離子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于苯乙烯(結構如圖)的下列敘述中:①能使酸性KMnO4溶液褪色;②可發生加聚反應;③可溶于水;④可溶于苯中;⑤能與濃硝酸發生取代反應;⑥所有的原子可能共平面,其中正確的是( ) ![]()
A.僅①②④⑤
B.僅①②⑤⑥
C.僅①②④⑤⑥
D.全部正確
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知甲、乙、丙、X是中學化學中四種常見的物質,其轉化關系如圖所示.則甲和X不可能是( ) 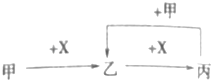
A.甲為CO2 , X為NaOH溶液
B.甲為NH3 , X為O2
C.甲為Si,X為O2
D.甲為NaAlO2 , X為HCl溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯氣是一種黃綠色氣體.1974年,瑞典化學家舍勒發現軟錳礦(主要成分是MnO2)和濃鹽酸混合加熱能制取氯氣:MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O;通常也可用高錳酸鉀和濃鹽酸混合來制取氯氣:2KMnO4+16HCl(濃)═2MnCl2+5Cl2↑+2KCl+8H2O;
MnCl2+Cl2↑+2H2O;通常也可用高錳酸鉀和濃鹽酸混合來制取氯氣:2KMnO4+16HCl(濃)═2MnCl2+5Cl2↑+2KCl+8H2O;
(1)若用這兩種方法制氯氣,請比較,它們的發生裝置使用的不同儀器是 .
(2)現將29g純度為60%的軟錳礦(主要成分MnO2)與足量的濃鹽酸充分反應(雜質不參加反應),把反應后所得溶液稀釋到200mL.計算: ①生成的Cl2在標準狀況下的體積.
②稀釋后溶液中MnCl2的物質的量濃度.
查看答案和解析>>
科目:高中化學 來源: 題型:
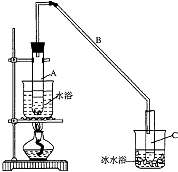
【題目】某化學小組采用類似制乙酸乙酯的裝置(如圖),以環己醇制備環己烯 已知: 
密度(g/cm3) | 熔點 (℃) | 沸點 (℃) | 溶解性 | |
環已醇 | 0.96 | 25 | 161 | 能溶于水 |
環已烯 | 0.81 | ﹣103 | 83 | 難溶于水 |
(1)制備粗品 將12.5mL環己醇加入試管A中,再加入1mL濃硫酸,搖勻后放入碎瓷片,緩慢加熱至反應完全,在試管C內得到環己烯粗品.
①A中碎瓷片的作用是 , 導管B除了導氣外還具有的作用是 .
②試管C置于冰水浴中的目的是 .
(2)制備精品 ①環己烯粗品中含有環己醇和少量酸性雜質等.加入飽和食鹽水,振蕩、靜置、分層,環己烯在層(填上或下),分液后用(填入編號)洗滌.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再將環己烯蒸餾即可得到精品.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】完成實驗Fe與水蒸氣反應,如圖所示. 
(1)裝置A的作用是 .
(2)B中反應的化學方程式: .
(3)堿石灰的作用是 .
(4)在D處玻璃管口點燃生成的氣體前,必須對該氣體進行 , 這一操作的目的是 .
(5)當有16.8g 鐵粉參加反應時,生成的氣體在標準狀況下的體積是 L.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com