
【題目】青蒿揮發油是青蒿的活性成分(幾乎不溶于水,可溶于乙醚,熔點156-157℃,對熱不穩定,乙醚的沸點34.6℃),有抗菌、解熱、止咳等作用。實驗室從青蒿中提取青蒿揮發油的流程如圖所示。
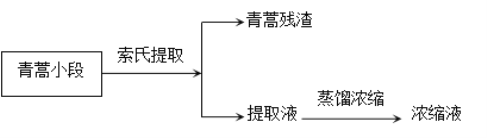
索氏提取裝置如圖所示,實驗時燒瓶中溶劑受熱蒸發,蒸汽沿蒸汽導管2上升至球形冷凝管,冷凝后滴入濾紙套筒1中,與青蒿小段接觸,進行萃取。萃取液液面達到虹吸管3頂端時,經虹吸管3返回燒瓶,從而實現對青蒿小段的連續萃取。回答下列問題:
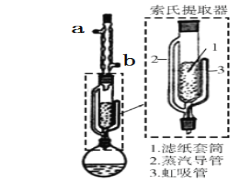
(1)實驗時需將青蒿剪成1-2cm小段,放入濾紙套筒1中,剪成小段的目的是___,圓底燒瓶中加入乙醚為溶劑時,應不超過燒瓶容積的___。
(2)索氏提取器中濾紙套筒的高度(x)、套管內青蒿小段的高度(y)及虹吸管的高度(z)由大到小的順序是___(用x、y、z回答),與常規的萃取相比,采用索氏提取器的優點是___。
(3)提取時球形冷凝管中冷水應從__(填“a”或“b”)管導入,提取液需經___(“常壓”或“減壓”)蒸餾法除去大部分溶劑,下列儀器在該蒸餾中需要用到的有___(填字母標號)。
A.直形冷凝管 B.球形冷凝管 C.錐形瓶 D.燒杯 E.溫度計
【答案】增加固液接觸面積,提取更充分 ![]() x>z>y 使用溶劑少,可連續萃取(或萃取效率高) b 減壓 ACE
x>z>y 使用溶劑少,可連續萃取(或萃取效率高) b 減壓 ACE
【解析】
根據索氏提取法的流程可知,對青蒿進行干燥破碎,可以增大青蒿與溶劑的接觸面積,提高青蒿素的浸取率,用溶劑對青蒿素進行浸取后,過濾,可得濾液和濾渣,提取液經過蒸餾后可得青蒿素的粗品,對粗品加95%的乙醇,濃縮、結晶、過濾可得精品。
(1)實驗時需將青蒿剪成1-2cm小段,放入濾紙套筒1中,剪成小段的目的是增加固液接觸面積,提取更充分,圓底燒瓶中加入乙醚為溶劑時,應不超過燒瓶容積的![]() 。
。
(2)蒸汽沿蒸汽導管2上升至球形冷凝管,冷凝后滴入濾紙套筒1中,與青蒿小段接觸,進行萃取。萃取液液面達到虹吸管3頂端時,經虹吸管3返回燒瓶,即套管內青蒿小段的高度小于虹吸管的高度,由圖可知:索氏提取器中濾紙套筒的高度(x)、套管內青蒿小段的高度(y)及虹吸管的高度(z)由大到小的順序是x>z>y,與常規的萃取相比,采用索氏提取器的優點是使用溶劑少,可連續萃取(或萃取效率高)。
(3)減少水資源浪費,使冷凝水更充分被利用,提取時球形冷凝管中冷水應從b管導入;減壓環境沸點下降,提取液需經減壓蒸餾法除去大部分溶劑,在該蒸餾中需要用到的有直形冷凝管、錐形瓶、溫度計。


科目:高中化學 來源: 題型:
【題目】短周期主族元素W、X、Y、Z的原子序數依次增加。A是元素Y的單質。常溫下,甲的濃溶液和A發生鈍化。丙、丁、戊是由這些元素組成的二元化合物,且丙是無色氣體。上述物質的轉化關系如圖所示。下列說法正確的是
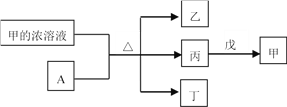
A. 丁和戊中所含元素種類相同
B. 簡單離子半徑大小:X<Y
C. 氣態氫化物的還原性:X>Z
D. Y的簡單離子與Z的簡單離子在水溶液中可大量共存
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D四種物質之間有下圖所示的轉化關系。
已知:A是氣體單質,C 是紅棕色氣體。
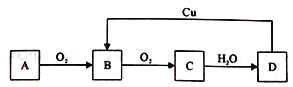
回答下列問題:
(1)寫出C的化學式:________;
(2)在上圖D→B的過程中,D表現出強_____(填“氧化性”或“還原性”);
(3)寫出C→D轉化的化學方程式__________________________________
(4)D→B的離子方程式_____________________________________________
(5)C 是紅棕色氣體,若A是氣態氫化物,則A的電子式為___________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組在實驗室從海帶中提取碘,設計實驗流程如下:
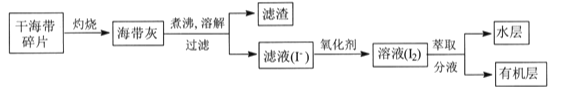
下列說法錯誤的是
A.過濾操作主要除去海帶灰中難溶于水的固體,它們主要是無機物
B.氧化劑參加反應的離子方程式為2I-+H2O2+2H+=I2+2H2O
C.萃取過程所用有機溶劑可以是酒精或四氯化碳
D.因I2易升華,I2的有機溶液難以通過蒸餾法徹底分離
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】C、N、P、S、Fe、Cu是與人類生產、生活息息相關的化學元素,利用所學知識回答下列問題:
(1)基態Cu原子核外電子排布式為___,則高溫下的穩定性CuO___Cu2O(填“>”或“<”);
(2)經研究Cu的某種化合物能催化氧化CO(NH2)2,其中C、N的雜化方式分別為___,___;
(3)Si、P、S元素的第一電離能由大到小的順序是___;
(4)OF2的空間構型是___,分子極性:H2O___OF2(填“>”或“<”),理由是___;
(5)[Fe(CN)6]3-中配位鍵和π鍵的個數之比為___;
(6)鄰羥基苯甲醛的沸點低于對羥基苯甲醛的沸點,原因是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是![]()
![]()
A.鹽酸的導電能力一定比醋酸的導電能力強
B.一定量的鋅粒與足量稀硫酸反應,向反應混合液中加入醋酸鈉固體,產生![]() 速率減小,
速率減小,![]() 體積減小
體積減小
C.相同溫度下![]() 氨水
氨水![]() 的濃度比
的濃度比![]() 溶液
溶液![]() 的濃度小
的濃度小
D.![]() 氨水可以使酚酞試液變紅,證明
氨水可以使酚酞試液變紅,證明![]() 是弱堿
是弱堿
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Y是合成香料、醫藥、農藥及染料的重要中間體,可由X在酸性條件下反應得到:
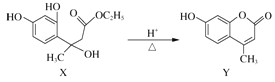
下列說法正確的是( )
A.X分子中所有碳原子可能共平面
B.X、Y分別與足量H2加成后的分子中均含有手性碳原子
C.Y可以發生顯色、氧化和還原反應,還可以與甲醛發生縮聚反應
D.1mol的X、Y分別與NaOH溶液反應,最多消耗NaOH的物質的量之比為4∶3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 時,濃度均為
時,濃度均為![]() 的HA溶液和BOH溶液的pH分別是1和11。下列說法中正確的是
的HA溶液和BOH溶液的pH分別是1和11。下列說法中正確的是 ![]()
![]()
A.BOH的電離方程式為![]()
B.將一定體積的上述兩種溶液混合后得到中性溶液,則![]()
C.在![]() 溶液中:
溶液中:![]()
D.若將![]() 溶液稀釋至
溶液稀釋至![]() ,則溶液的
,則溶液的![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三氯氧磷![]() 廣泛用于農藥、醫藥等生產。工業制備三氯氧磷的過程中會產生副產品亞磷酸
廣泛用于農藥、醫藥等生產。工業制備三氯氧磷的過程中會產生副產品亞磷酸![]() 。請回答下列問題:
。請回答下列問題:
![]() 已知亞磷酸
已知亞磷酸![]() 為二元弱酸,則
為二元弱酸,則![]() 溶液中,各離子濃度的大小關系為________。
溶液中,各離子濃度的大小關系為________。
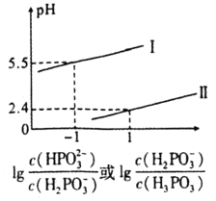
![]() 常溫下,將NaOH溶液滴加到亞磷酸
常溫下,將NaOH溶液滴加到亞磷酸![]() 溶液中,混合溶液pH與離子濃度變化的關系如圖所示。則表示
溶液中,混合溶液pH與離子濃度變化的關系如圖所示。則表示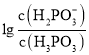 的是曲線________
的是曲線________![]() 填“Ⅰ”或“Ⅱ”
填“Ⅰ”或“Ⅱ”![]() ,亞磷酸
,亞磷酸![]() 的
的![]() ________,反應
________,反應![]() 的平衡常數值是________。
的平衡常數值是________。
![]() 工業上生產三氯氧磷的同時會產生含磷廢水
工業上生產三氯氧磷的同時會產生含磷廢水![]() 主要成分為
主要成分為![]() 、
、![]() 。向廢水中先加入適量漂白粉,再加入生石灰調節pH,將磷元素轉化為磷酸的鈣鹽沉淀并回收。若處理后的廢水中
。向廢水中先加入適量漂白粉,再加入生石灰調節pH,將磷元素轉化為磷酸的鈣鹽沉淀并回收。若處理后的廢水中![]() ,則溶液中
,則溶液中![]() ________
________![]() 。
。![]() 已知
已知![]() )
)![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com