
堿金屬元素在科學研究與生產生活中有著非常廣泛的用途。
(1)鋰是最輕的金屬,如果用鋰做一架飛機,兩個人就可以抬動。鋰在元素周期表中的表示如圖所示,填寫以下空格。
①Li在元素周期表中的位置: 。
②6.941的意義: __________________________。
(2)光電管是利用堿金屬銫受到光照射時能形成電流這一光電效應的性質制成的。
①完成銫的原子結構示意圖: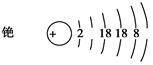
②下列有關銫的說法正確的是________。
| A.其單質在常溫下與水反應不如鈉劇烈, | B.其原子半徑比鉀原子半徑小 |
| C.其氫氧化物的水溶液不能使氫氧化鋁溶解, | D.其碳酸鹽易溶于水 |
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:單選題
鹵族元素隨著原子序數的增大,下列遞變規律正確的是( )
| A.原子半徑逐漸增大 | B.單質的氧化性逐漸增強 |
| C.單質熔、沸點逐漸降低 | D.氣態氫化物穩定性逐漸增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E五種短周期元素,它們的原子序數依次增大。A是元素周期表中原子半徑最小的元素,B元素原子L層上的電子數為K層電子數的2倍;元素D的2價陰離子的核外電子排布與氖原子相同;E與A同主族;A和E這兩種元素與D都能形成X2Y、X2Y2型化合物。請回答:
(1)寫出元素的符號:C ;E 。
(2)化合物A2D的電子式為 。
(3)元素B的一種同位素可測定文物年代,這種同位素的符號是 。
(4)B的最高價氧化物的結構式 。
(5)寫出符合X2Y2的物質在MnO2催化作用下生成D單質的方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(8分)下表是元素周期表的短周期部分,表中字母分別表示一種元素。請回答下列問題:
| a | | | |||||
| | | | b | c | d | | |
| e | | f | | | g | | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
元素周期表與元素周期律在學習、研究和生產實踐中有很重要的作用。下表列出了①~⑨九種元素在周期表中的位置。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑤ | | ⑥ | | |
| 3 | ① | ③ | ④ | | | | ⑦ | ⑨ |
| 4 | ② | | | | | | ⑧ | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
短周期元素Q、R、T、W在元素周期表中的位置如下圖所示,其中T所處的周期序數與主族序數相等,請回答下列問題: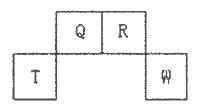
(l)W在周期表中的位置是___________,Q、R、T三種元素原予的半徑從大到小排列順序為 (用元素符號表示),Q的最高價氧化物的電子式___________,R氣態氫化物分子的結構式為___________;
(2)元素的原子得電子能力:Q_____W(填“強于”或“弱于”);
(3)原子序數比R多8的元素形成的一種常見氣態氫化物的沸點___________(填“高”或“低”)于R的的常見氣態氫化物;
(4)T、Q、R、W的單質中,固態時屬于原子晶體的是___________(填名稱);
(5)現有8種屬于短周期的元素,它們的性質、數據如下表所列。請指出R元素在下表中的對應編號___________,與T同周期且最高價氧化物的水化物堿性最強的元素在下表中的對應編號___________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(9分)A、B、C三種元素的原子具有相同的電子層數,而B的核電荷數比A大1,C原子的電子總數比B原子的電子總數多4; 1molA的單質跟足量鹽酸反應,可置換出標準狀況下22.4L的H2,這時A轉變為與氖原子具有相同電子層結構的離子。試請回答:
(1)用電子式表示A和C組成的化合物的形成過程為______________________;
(2)B離子的電子式是 ,與B的離子具有相同電子數的分子中,有一種分子可與鹽酸化合生成鹽,該分子的電子式是 ;
(3)周期表中與C上下相鄰的同族元素形成的氣態氫化物中,沸點最高的是 ,(填氫化物化學式),原因是 ;
(4)寫出B最高價氧化物的水化物和C最高價氧化物的水化物之間反應的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
[物質結構與性質]
磁性材料氮化鐵鎳合金可用Fe(NO3)3、Ni(NO3)2、丁二酮肟、氨氣、氮氣、氫氧化鈉、鹽酸等物質在一定條件下反應制得。
(1) 基態Ni原子的價電子排布式是________。
(2) 丁二酮肟(結構簡式如右圖所示)中碳原子的雜化方式為________。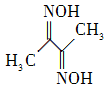
(3) NH3的沸點高于PH3,其主要原因是____。
(4) 與N3-離子具有相同電子數的三原子分子的空間構型是________。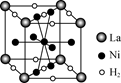
(5) 向Ni(NO3)2溶液中滴加氨水,剛開始時生成綠色Ni(OH)2沉淀,當氨水過量時,沉淀會溶解,生成[Ni(NH3)6]2+的藍色溶液,則1 mol[Ni(NH3)6]2+含有的σ鍵為________mol。
(6) 右圖是一種鎳基合金儲氫后的晶胞結構示意圖。該合金儲氫后,含1 mol La的合金可吸附H2的數目為________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(15分) 已知A、B、C、D、E都是元素周期表中的前四周期元素,它們原子序數的大小關系為A<C<B<D<E。又知A原子的p軌道為半充滿,其形成的簡單氫化物的沸點是同主族非金屬元素的氫化物中最高的。D原子得到一個電子后其3p軌道將全充滿。B+離子比D原子形成的離子少一個電子層。C與B可形成BC型的離子化合物。E的原子序數為29。
請回答下列問題:
(1) 元素A簡單氫化物中A原子的雜化類型是 ,B、C、D的電負性由小到大的順序為
__ (用所對應的元素符號表示)。C的氣態氫化物易溶于水的原因是 。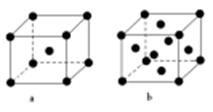
(2)E原子的基態電子排布式為 。元素E的單質晶體在不同溫度下可有兩種堆積方式,晶胞分別如右圖a和b所示,則其面心立方堆積的晶胞與體心立方堆積的晶胞中實際含有的E原子的個數之比為 。
(3)實驗證明:KCl、MgO、CaO、TiN這4種晶體的結構與NaCl晶體結構相似(如圖所示),其中3種離子晶體的晶格能數據如下表:
| 離子晶體 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com