
【題目】已知在同一碳原子上連有兩個羥基的化合物是極不穩定的,它要自動失水生成含醛基的化合物。今在無其他氧化劑存在的條件下,以甲苯和氯氣為主要原料按下列過程制取苯甲醛(C6H5CHO)。
![]()
(1)條件2中試劑為____________________________________________。
(2)寫出苯甲醛與新制Cu(OH)2懸濁液反應的化學方程式:_________________________________________________________________。
(3)苯甲醛在強堿性條件下可發生自身氧化還原反應,即部分氧化成羧酸鹽A,部分還原成醇B。寫出A經酸化后的產物苯甲酸與B酯化反應可生成一種新的化合物C的結構簡式:______________________。
科目:高中化學 來源: 題型:
【題目】回答下列問題
(1)已知鈷屬于鐵系元素,其單質與化合物的性質與鐵相似,其常見化合價有+2和+3,則Co3O4與濃鹽酸反應能生成黃綠色氣體的離子方程式_________________。
(2)碳酸亞鐵(FeCO3)是菱鎂礦的主要成分,將FeCO3加熱到200℃開始分解為FeO和CO2,若在空氣中高溫煅燒FeCO3生成Fe2O3。
已知25℃,101kPa時: 4Fe(s)+3O2(g)=2Fe2O3(s) △H=1648kJ/mol
C(s)+O2(g)=CO2(g) △H=393kJ/mol
2FeCO3(s)=2Fe(s)+2C(s)+3O2(g) △H=+1480kJ/mol
寫出FeCO3在空氣中煅燒生成Fe2O3的熱化學方程式______________。
(3)將標準狀況下1.344L Cl2通入100mL0.5mol/lFeI2溶液中的離子方程式為_____________。
(4)1mol·L-1的NaAlO2溶液和3.0mol·L-1的HCl溶液等體積混合的離子方程式為________________
(5)用于驅動潛艇的液氨-液氧燃料電池示意圖如圖所示:
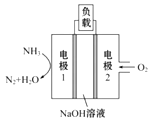
則電極1的電極反應式為:______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向某Na2CO3、NaHCO3的混合溶液中加入少量的BaCl2固體(溶液體積變化、溫度變化忽略不計),測得溶液中離子濃度的關系如圖所示,下列說法正確的是( )
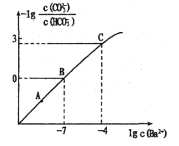
已知:Ksp(BaCO3)=2.40![]() 10-9
10-9
A.A、B、C三點對應溶液pH的大小順序為:A>B>C
B.A點對應的溶液中存在:c(CO32-)< c(HCO3-)
C.B點溶液中 c(CO32-)=0.24mol/L
D.向C點溶液中通入CO2可使C點溶液向B點溶液轉化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯甲醛是一種重要的化工原料,某小組同學利用如圖所示實驗裝置(夾持裝置已略去)制備苯甲醛。
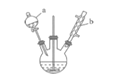
已知有機物的相關數據如下表所示:
有機物 | 沸點℃ | 密度為g/cm3 | 相對分子質量 | 溶解性 |
苯甲醛 | 178.1 | 1.04 | 106 | 微溶于水,易溶于乙醇、醚和鹵代烴 |
苯甲醇 | 205.7 | 1.04 | 108 | 微溶于水,易溶于乙醇、醚和鹵代烴 |
二氯甲烷 | 39.8 | 1.33 | 難溶于水,易溶于有機溶劑 |
實驗步驟:
①向容積為500mL的三頸燒瓶加入90.0mL質量分數為5%的次氯酸鈉溶液(稍過量),調節溶液的pH為9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不斷攪拌。
②充分反應后,用二氯甲烷萃取水相3次,并將有機相合并。
③向所得有機相中加入無水硫酸鎂,過濾,得到有機混合物。
④蒸餾有機混合物,得到2.08g苯甲醛產品。
請回答下列問題:
(1)儀器b的名稱為______,攪拌器的作用是______。
(2)苯甲醇與NaClO反應的化學方程式為_______。
(3)步驟①中,投料時,次氯酸鈉不能過量太多,原因是____;步驟③中加入無水硫酸鎂,若省略該操作, 可能造成的后果是______。
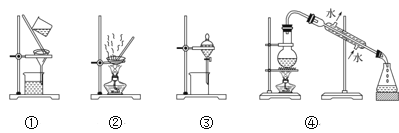
(4)步驟②中,應選用的實驗裝置是___(填序號),該操作中分離出有機相的具體操作方法是___。
(5)步驟④中,蒸餾溫度應控制在_______左右。
(6)本實驗中,苯甲醛的產率為________(保留到小數點后一位)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組利用圖甲裝置制取氨氣并探究氨氣的有關性質。

(1)裝置A中燒瓶內試劑可選用__(填序號)。
a.堿石灰 b.濃硫酸 c.五氧化二磷 d.氯化鈣
(2)若探究氨氣的溶解性,當裝置D中集滿氨氣后,關閉K1、K2,打開K3,引發噴泉的實驗操作是__。不能在K2的導管末端連接圖乙中的__裝置(填序號)。
(3)若探究氨氣的還原性,需關閉K1、K3,K2連接純凈、干燥氯氣的裝置。
①用二氧化錳與濃鹽酸制取氯氣,生成的氣體必須依次通過盛有__試劑和__試劑的洗氣瓶。
②D中氨氣與氯氣反應產生白煙,同時生成一種無色無味的氣體,該反應的化學方程式為__。
③尾氣可用C裝置處理,若尾氣中含有少量Cl2,則C裝置中應盛放__溶液(填化學式),反應的離子方程式為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.丙烷和丁烷是同系物,兩者化學性質相似
B.![]() 和
和![]() 互為同分異構體,兩者化學性質不同
互為同分異構體,兩者化學性質不同
C.氧氣和臭氧互為同素異形體,兩者的熔點不同
D.氧化鈉與過氧化鈉均為離子化合物,兩者所含的化學鍵類型不完全相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用化合物A模擬工業上制備含氧酸D的過程如圖所示,已知D為強酸,請回答下列問題。
![]()
(1)若A在常溫下為固體,B是能使品紅溶液褪色的有刺激性氣味的無色氣體。
①D的化學式是________;
②在工業生產中,B氣體的大量排放被雨水吸收后形成了_____而污染了環境。
(2)若A在常溫下為氣體,C是紅棕色的氣體。
①A的化學式是_________;C的化學式是_______。
②D的濃溶液在常溫下可與銅反應并生成C氣體,反應的化學方程式是____,該反應______(填“屬于”或“不屬于”)氧化還原反應。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E、F、G是七種常見的短周期元素,其原子序數依次增大,請根據所給信息填寫表中空白,并回答下列問題:
編號 | 基本信息 | 解決的問題 |
① | 其中兩種元素的原子核外電子層數與最外層電子數之比分別為 | 這兩種元素分別是______(填元素符號,下同)、______. |
② | 其中一種元素的氧化物與強酸、強堿均能反應;另一種元素的單質、氧化物及氧化物對應的水化物均能與NaOH溶液反應 | 這兩種元素分別是______、______. |
③ | G能與A、E分別形成原子個數比均為 | X的分子式為______, |
(1)僅由表中信息還不能確定的元素是______(填字母序號),若要確定其是何種元素,還需要的條件是______(填序號).
a.單質能與氧氣反應
b.最高價氧化物對應的水化物是強酸
e.單質在常溫下為固體
d.簡單氯化物的穩定性比![]() 的簡單氯化物強
的簡單氯化物強
(2)基本信息②中,兩種元素的氧化物分別與NaOH溶液反應的離子方程式為__________________,__________________.
(3)上述某兩種元素間可形成原子個數比為![]() 及
及![]() 的兩種能與水反應的常見化合物,寫出前者與H2O反應的離子方程式:__________________.
的兩種能與水反應的常見化合物,寫出前者與H2O反應的離子方程式:__________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學采用硫鐵礦焙燒取硫后的燒渣(主要成分為Fe2O3、SiO2、Al2O3,不考慮其他雜質)制取七水合硫酸亞鐵(FeSO4·7H2O),設計了如下流程:

下列說法不正確的是( )
A. 溶解燒渣選用足量硫酸,試劑X選用鐵粉
B. 固體1中一定含有SiO2,控制pH是為了使Al3+轉化為Al(OH)3,進入固體2
C. 從溶液2得到FeSO4·7H2O產品的過程中,須控制條件防止其氧化和分解
D. 若改變方案,在溶液1中直接加NaOH至過量,得到的沉淀用硫酸溶解,其溶液經結晶分離也可得到FeSO4·7H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com