
įONA┤·▒Ē░óĘ³╝ėĄ┬┴_│ŻöĄĄ─öĄųĄŻ¼Ž┬┴ąšfĘ©š²┤_Ą─╩ŪŻ© Ż®
| AŻ«12.5mL 16molĪżL-1ØŌ┴“╦ß┼cūŃ┴┐õ\Ę┤æ¬Ż¼▐DęŲļŖūėöĄ×ķ0.2NA |
| BŻ«0.1 mol24Mg18OŠ¦¾wųą╦∙║¼ųąūė┐éöĄ×ķ2.0 NA |
| CŻ«1L 1 molĪżLŻŁ1Ą─┤ū╦ß╚▄ę║ųąļxūė┐éöĄ×ķ2NA |
| DŻ«4.5 g SiO2Š¦¾wųą║¼ėąĄ─╣Ķ觵IöĄ─┐×ķ0.3 NA |
D
ĮŌ╬÷įćŅ}Ęų╬÷Ż║AĪóļSų°Ę┤æ¬▀MąąŻ¼┴“╦ߥ─ØŌČ╚ųØu£pąĪŻ¼ūā×ķŽĪ┴“╦ß║¾Ż¼Ę┤æ¬Ė─ūāŻ¼Ž╚║¾░l╔·Ż║Zn+2H2SO4(ØŌ)=ZnSO4+SO2Ī³+2H2OĪóZn+H2SO4=ZnSO4+H2Ī³,▐DęŲļŖūėöĄ┤¾ė┌0.2NAŻ¼Õeš`Ż╗BĪó0.1 mol24Mg18OŠ¦¾wųą╦∙║¼ųąūė┐éöĄ×ķŻ║0.1Ī┴Ż©12+10Ż®NA="2.2" NAŻ¼Õeš`Ż╗CĪó┤ū╦ß×ķ╚§╦߯¼╦∙ęį1L 1 molĪżLŻŁ1Ą─┤ū╦ß╚▄ę║ųąļxūė┐éöĄąĪė┌2NAŻ¼Õeš`Ż╗DĪó├┐éĆSiįŁūėą╬│╔4éĆ╣Ķ觵IŻ¼╦∙ęį4.5 g SiO2Š¦¾wųą║¼ėąĄ─╣Ķ觵IöĄ─┐×ķŻ║4.5gĪ┬60g/molĪ┴4 NAmol-1="0.3" NAŻ¼š²┤_ĪŻ
┐╝³cŻ║▒ŠŅ}┐╝▓ķ░óĘ³┘żĄ┬┴_│ŻöĄĄ─æ¬ė├ĪŻ



| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ąĖ„╚▄ę║ųąNO3-╬’┘|Ą─┴┐ØŌČ╚ūŅ┤¾Ą─╩Ū
| AŻ«20 mL 2 moLŻ»L Mg(NO3)2 | BŻ«100 mL 2Ż«5 motŻ»L NaNO3 |
| CŻ«25 mL 1.0molŻ»L Al(NO3)3 | DŻ«30 mL 2Ż«5 molŻ»L NH4NO3 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
ė├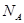 ▒Ē╩Š░óĘ³╝ėĄ┬┴_│ŻöĄĄ─ųĄĪŻŽ┬┴ąöó╩÷ųą▓╗š²┤_Ą─╩Ū
▒Ē╩Š░óĘ³╝ėĄ┬┴_│ŻöĄĄ─ųĄĪŻŽ┬┴ąöó╩÷ųą▓╗š²┤_Ą─╩Ū
AŻ«ūŃ┴┐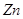 ┼cę╗Č©┴┐Ą─ØŌ┴“╦ßĘ┤æ¬Ż¼«a╔· ┼cę╗Č©┴┐Ą─ØŌ┴“╦ßĘ┤æ¬Ż¼«a╔· Ż©ś╦ørŻ®ÜŌ¾wĢrŻ¼▐DęŲĄ─ļŖūėöĄ×ķ Ż©ś╦ørŻ®ÜŌ¾wĢrŻ¼▐DęŲĄ─ļŖūėöĄ×ķ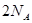 |
BŻ«ę╗Č©Śl╝■Ž┬Ż¼32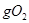 ║═ūŃ┴┐Ą─ĶFĘ█│õĘųĘ┤æ¬Ż¼▐DęŲĄ─ļŖūėöĄ×ķ ║═ūŃ┴┐Ą─ĶFĘ█│õĘųĘ┤æ¬Ż¼▐DęŲĄ─ļŖūėöĄ×ķ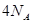 |
CŻ«4Ż«6gęę┤╝║═╝ū╦߯©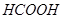 Ż®Ą─╗ņ║Ž╬’ųą║¼ėąĄ─╠╝įŁūėöĄį┌ Ż®Ą─╗ņ║Ž╬’ųą║¼ėąĄ─╠╝įŁūėöĄį┌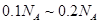 ų«ķg ų«ķg |
DŻ«Ęųūė┐éöĄ×ķ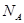 Ą─NO║═ Ą─NO║═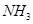 ╗ņ║ŽÜŌ¾wųą║¼ėąĄ─Ą¬įŁūėöĄ×ķ ╗ņ║ŽÜŌ¾wųą║¼ėąĄ─Ą¬įŁūėöĄ×ķ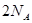 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
ė├nA▒Ē╩Š░óĘ³╝ėĄ┬┴_│ŻöĄĄ─öĄųĄŻ¼Ž┬┴ąöó╩÷š²┤_Ą─╩Ū
| AŻ«│Ż£ž│Żē║Ž┬Ż¼200 g 8Ż«5ŻźĄ─H2O2╦«╚▄ę║ųą║¼č§įŁūė┐éöĄ×ķnA |
| BŻ«ś╦£╩ĀŅørŽ┬Ż¼22Ż«4LCHCI3ųą║¼C -HµIöĄ─┐×ķnA |
| CŻ«│Ż£žŽ┬Ż¼14g▒¹Ž®Ż©CH3CH=CH2Ż®ųą║¼╠╝įŁūėöĄ×ķnA |
| DŻ«│Ż£žŽ┬,pH=13Ą─Üõč§╗»Ōc╚▄ę║ųąŻ¼║¼OHę╗öĄ─┐×ķnA |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ą╬’┘|Ą─ļŖūė╩ĮĢ°īæš²┤_Ą─╩Ū
AŻ«N2Ż║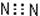 |
BŻ«CO2Ż║ |
CŻ«Na2OŻ║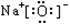 |
DŻ«HClŻ║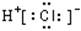 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
Ž┬┴ąĻPė┌╬’┘|Ą─┴┐ØŌČ╚▒Ē╩÷š²┤_Ą─╩Ū
| AŻ«0.2 molĪżLŻŁ1 Na2SO4╚▄ę║ųą║¼ėąNa+║═SO42Ī¬┐é╬’┘|Ą─┴┐×ķ0.6 mol |
| BŻ«50mL 2 molĪżLŻŁ1Ą─NaCl╚▄ę║║═100mL 0.5molĪżLŻŁ1MgCl2╚▄ę║ųąŻ¼ClŻŁĄ─╬’┘|Ą─┴┐ØŌČ╚ŽÓĄ╚ |
| CŻ«ė├1 L╦«╬³╩š22.4 L┬╚╗»ÜõŻ©ś╦ørŽ┬Ż®╦∙Ą├¹}╦ߥ─ØŌČ╚╩Ū1 molĪżLŻŁ1 |
| DŻ«10 g 98%Ą─┴“╦߯©├▄Č╚×ķ1.84g Īż cmĪ¬3Ż®┼c10mL 18.4molĪżLĪ¬1Ą─┴“╦ߥ─ØŌČ╚╩ŪŽÓ═¼Ą─ |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
įONA×ķ░óĘ³╝ėĄ┬┴_│ŻöĄĄ─ųĄŻ¼Ž┬┴ąöó╩÷š²┤_Ą─╩Ū
AŻ«ĘųūėöĄ×ķNAĄ─COĪó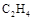 ╗ņ║ŽÜŌ¾w¾wĘe╝s×ķ22Ż«4LŻ¼┘|┴┐×ķ28g ╗ņ║ŽÜŌ¾w¾wĘe╝s×ķ22Ż«4LŻ¼┘|┴┐×ķ28g |
| BŻ«│Ż£ž│Żē║Ž┬,92gĄ─NO2║═N2O4╗ņ║ŽÜŌ¾w║¼ėąĄ─įŁūėöĄ×ķ4NA |
| CŻ«│Ż£ž│Żē║Ž┬Ż¼7Ż«0gęꎮ┼c▒¹Ž®Ą─╗ņ║Ž╬’ųą║¼ėąÜõįŁūėĄ─öĄ─┐×ķ2NA |
DŻ«78g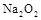 ╣╠¾w┼cH2O═Ļ╚½Ę┤æ¬▐DęŲĄ─ļŖūėöĄ×ķNA ╣╠¾w┼cH2O═Ļ╚½Ę┤æ¬▐DęŲĄ─ļŖūėöĄ×ķNA |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
īŹ“×╩ęė├NaCl╣╠¾w┼õ400 mL 1.0 molŻ»L NaCl╚▄ę║Ż¼Ž┬┴ą┼ąöÓ▓╗ī”Ą─╩ŪŻ© Ż®
| AŻ«ė├═ą▒P╠ņŲĮĘQ╚ĪNaCl╣╠¾w23.4 g |
| BŻ«æ¬▀xė├500 mLĄ─╚▌┴┐Ų┐üĒ┼õųŲ┤╦╚▄ę║ |
| CŻ«į┌▐DęŲ▓┘ū„ųą▓╗╔„īó╚▄ę║×óĄĮ╚▌┴┐Ų┐═Ō├µŻ¼æ¬įōųžą┬┼õų├╚▄ę║ |
| DŻ«╝ėš¶s╦«ų┴ļx┐╠Č╚ŠĆ1-2 cmĢrĖ─ė├─zŅ^Ą╬╣▄Č©╚▌ |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║å╬▀xŅ}
═¼£ž═¼ē║Ž┬Ż¼ā╔éĆ╚▌ĘeŽÓĄ╚Ą─ā”ÜŌŲ┐Ż¼ę╗éĆčbėąC2H4Ż¼┴Ēę╗éĆčbėąC2H2║═C2H6Ą─╗ņ║ŽÜŌ¾wŻ¼ā╔Ų┐ā╚ÜŌ¾wę╗Č©Š▀ėąŽÓ═¼Ą─Ż© Ż®
| AŻ«┘|┴┐ | BŻ«įŁūė┐éöĄ | CŻ«╠╝įŁūėöĄ | DŻ«├▄Č╚ |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com