
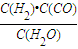 ,它所對(duì)應(yīng)反應(yīng)的化學(xué)方程式為______.
,它所對(duì)應(yīng)反應(yīng)的化學(xué)方程式為______.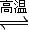 CH3OH(g)△H1=-90.7kJ?mol-1
CH3OH(g)△H1=-90.7kJ?mol-1 CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1
CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1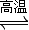 CO2(g)+H2(g)△H3=-41.2kJ?mol-1
CO2(g)+H2(g)△H3=-41.2kJ?mol-1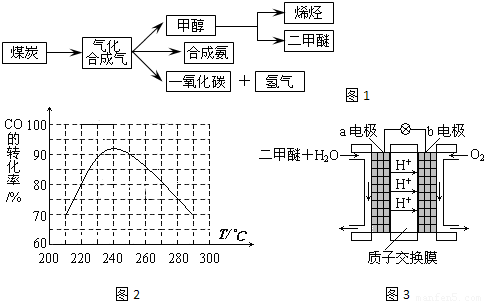
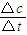 計(jì)算v(CO).
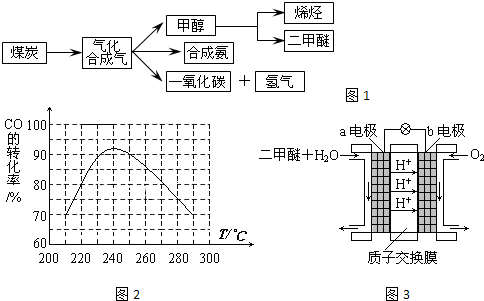
計(jì)算v(CO).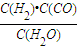 ,生成物為CO、H2,反應(yīng)物含有H2O,三者化學(xué)計(jì)量數(shù)分別為1、1、1,根據(jù)元素守恒,故另一反應(yīng)物為固體C,反應(yīng)中它所對(duì)應(yīng)反應(yīng)的化學(xué)方程式為C(s)+H2O(g)?CO(g)+H2(g).催化反應(yīng)室中溫度小于830℃,升高溫度反應(yīng)③平衡向正反應(yīng)移動(dòng),平衡常數(shù)增大.
,生成物為CO、H2,反應(yīng)物含有H2O,三者化學(xué)計(jì)量數(shù)分別為1、1、1,根據(jù)元素守恒,故另一反應(yīng)物為固體C,反應(yīng)中它所對(duì)應(yīng)反應(yīng)的化學(xué)方程式為C(s)+H2O(g)?CO(g)+H2(g).催化反應(yīng)室中溫度小于830℃,升高溫度反應(yīng)③平衡向正反應(yīng)移動(dòng),平衡常數(shù)增大.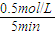 =0.1mol/(L?min);
=0.1mol/(L?min);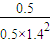 =
=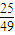 ,若反應(yīng)物的起始濃度分別為:c(CO)=4mol/L,c(H2)=a mol/L,達(dá)到平衡后,c(CH3OH)=2mol/L,則平衡時(shí)c′(CO)=4mol/L-2mol/L=2mol/L,令平衡時(shí)氫氣的濃度為ymol/L,所以
,若反應(yīng)物的起始濃度分別為:c(CO)=4mol/L,c(H2)=a mol/L,達(dá)到平衡后,c(CH3OH)=2mol/L,則平衡時(shí)c′(CO)=4mol/L-2mol/L=2mol/L,令平衡時(shí)氫氣的濃度為ymol/L,所以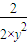 =
=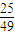


 高效智能課時(shí)作業(yè)系列答案
高效智能課時(shí)作業(yè)系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:閱讀理解

| [H2][CO] |
| [H2O] |
| 容器編號(hào) | n(C)mol | n(H2O)mol | n(CO)mol | n(H2)mol | v正、v逆比較 |
| Ⅰ | 0.2 | 0.12 | 1.20 | 0.20 | v正=v逆 |
| Ⅱ | 0.16 | 0.20 | 0.40 | 0.80 | v正 > > v逆 |
| 0.2×0.4 |
| 0.1 |
| 0.2×0.4 |
| 0.1 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:閱讀理解

| C(H2)C(CO) |
| C(H2O) |
| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數(shù)K | 9.94 | 9 | 1 |
 .已知N-N鍵鍵能為167kJ?mol-1,NO2中氮氧鍵的鍵能為466kJ?mol-1,N2O4中氮氧鍵的鍵能為438.5kJ?mol-1.請寫出NO2轉(zhuǎn)化為N2O4的熱化學(xué)方程式為
.已知N-N鍵鍵能為167kJ?mol-1,NO2中氮氧鍵的鍵能為466kJ?mol-1,N2O4中氮氧鍵的鍵能為438.5kJ?mol-1.請寫出NO2轉(zhuǎn)化為N2O4的熱化學(xué)方程式為查看答案和解析>>
科目:高中化學(xué) 來源: 題型:閱讀理解
| C(H2)?C(CO) |
| C(H2O) |
| 高溫 |
| 高溫 |
| 高溫 |
查看答案和解析>>
科目:高中化學(xué) 來源:2011-2012學(xué)年浙江省溫州市十校聯(lián)考高三(上)期中化學(xué)試卷(解析版) 題型:填空題

 ,它所對(duì)應(yīng)的化學(xué)反應(yīng)為: .
,它所對(duì)應(yīng)的化學(xué)反應(yīng)為: .| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數(shù)K | 9.94 | 9 | 1 |
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com