
【題目】鍺在自然界中非常分散,幾乎沒有比較集中的鍺礦,因此被人們稱為“稀散金屬”。回答下列問題:
(1)基態鍺原子最外層電子排布圖為_______,Ge原子的電子發生躍遷時會吸收或放出不同的光,可用_______![]() 填儀器名稱
填儀器名稱![]() 攝取其原子光譜,從而鑒定Ge元素的存在。
攝取其原子光譜,從而鑒定Ge元素的存在。
(2)鍺元素能形成無機化合物![]() 如鍺酸鈉:
如鍺酸鈉:![]() ;二鍺酸鈉:
;二鍺酸鈉:![]() ;四鍺酸鈉:
;四鍺酸鈉:![]() 等
等![]() ,也能形成類似于烷烴的鍺烷
,也能形成類似于烷烴的鍺烷![]() 。
。
![]() 中鍺原子的雜化方式為______________。
中鍺原子的雜化方式為______________。
![]() 鍺與碳同族,性質及結構有一定的相似性,據此推測
鍺與碳同族,性質及結構有一定的相似性,據此推測![]() 二鍺酸鈉
二鍺酸鈉![]() 中含有的
中含有的![]() 鍵的數目為_________。
鍵的數目為_________。
![]() 至今沒有發現n大于5的鍺烷,根據下表提供的數據分析其中的原因:___________________。
至今沒有發現n大于5的鍺烷,根據下表提供的數據分析其中的原因:___________________。
化學鍵 |
|
|
|
|
鍵能 | 346 | 411 | 188 | 288 |
(3)有機多元膦酸鍺配合物是由![]() Ⅳ
Ⅳ![]() 與
與![]() 形成的,其結構如下:
形成的,其結構如下:
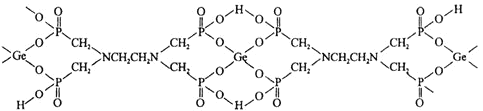
![]() 該配合物中,下列作用力不存在的有_________
該配合物中,下列作用力不存在的有_________
A.極性鍵 ![]() 非極性鍵
非極性鍵 ![]() 金屬鍵
金屬鍵 ![]() 配位鍵
配位鍵 ![]() 氫鍵
氫鍵 ![]() 鍵
鍵
![]() 該配合物中
該配合物中![]() Ⅳ
Ⅳ![]() 的配位數是_______;配位原子是_______
的配位數是_______;配位原子是_______![]() 填元素符號
填元素符號![]() 。
。
![]() 試解釋磷酸
試解釋磷酸![]() 酸性為什么與亞硝酸相近?______________。
酸性為什么與亞硝酸相近?______________。
(4)![]() 常作為軍事上的紅外制導材料,其理想晶胞如圖所示。測得晶胞參數
常作為軍事上的紅外制導材料,其理想晶胞如圖所示。測得晶胞參數![]() ,
,![]() ,該晶體的密度為_______
,該晶體的密度為_______![]() 列出算式即可,阿伏加德羅常數用
列出算式即可,阿伏加德羅常數用![]() 表示
表示![]() 。
。

![]() 原子的分數坐標即將晶胞參數a、b、c均看作“1”所得出的三維空間坐標,以1號Zn為坐標原點,則
原子的分數坐標即將晶胞參數a、b、c均看作“1”所得出的三維空間坐標,以1號Zn為坐標原點,則![]() 晶胞圖中標號為“2”的P原子的分數坐標為_______。
晶胞圖中標號為“2”的P原子的分數坐標為_______。
【答案】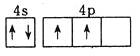 光譜分析儀
光譜分析儀![]() 或光譜儀
或光譜儀![]()
![]()
![]() 因為
因為![]() 和
和![]() 的鍵能較小,鍵容易斷裂,形成的鍺烷不穩定
的鍵能較小,鍵容易斷裂,形成的鍺烷不穩定 ![]()
![]() O 因為
O 因為![]() 和
和![]() 中的非羥基氧的數目相同,都是1個
中的非羥基氧的數目相同,都是1個 ![]()
![]()
【解析】
(1)根據能量最低原理、洪特規則書寫基態鍺原子最外層電子排布圖;光譜儀攝取其原子光譜。
(2)![]() 和C同族,
和C同族,![]() 中Ge的價層電子對數
中Ge的價層電子對數![]() 。
。
![]() 和C同族,推測
和C同族,推測![]() 結構為
結構為![]() 。
。
![]() 和
和![]() 的鍵能較小,鍵容易斷裂;
的鍵能較小,鍵容易斷裂;
(3)![]() 金屬鍵只存在金屬晶體中;
金屬鍵只存在金屬晶體中;
![]() 根據結構簡式可知,該配合物中
根據結構簡式可知,該配合物中![]() 與4個O原子形成配位鍵。
與4個O原子形成配位鍵。
![]() 非羥基氧原子數越多,含氧酸的酸性越強。
非羥基氧原子數越多,含氧酸的酸性越強。
(4)![]() )。
)。
![]() 1號Zn為坐標原點,根據建立的坐標系判斷2號P原子的位置。
1號Zn為坐標原點,根據建立的坐標系判斷2號P原子的位置。
![]() 鍺元素是周期表中32號元素,其基態原子最外層電子排布圖是
鍺元素是周期表中32號元素,其基態原子最外層電子排布圖是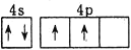 ;核外電子發生躍遷會吸收或放出不同的光,可用光譜分析儀
;核外電子發生躍遷會吸收或放出不同的光,可用光譜分析儀![]() 或光譜儀
或光譜儀![]() 攝取原子光譜,從而鑒定Ge元素的存在;
攝取原子光譜,從而鑒定Ge元素的存在;
![]() 和C同族,
和C同族,![]() 中Ge的價層電子對數為
中Ge的價層電子對數為![]() ,所以其雜化方式為
,所以其雜化方式為![]() 雜化;
雜化;
![]() 和C同族,推測
和C同族,推測![]() 結構為
結構為![]() ,所以每個
,所以每個![]() 中含
中含![]() 鍵6個,故
鍵6個,故![]() 中含
中含![]() 鍵的數目為
鍵的數目為![]() ;
;
![]() 因為
因為![]() 和
和![]() 的鍵能較小,鍵容易斷裂,形成的鍺烷不穩定,所以至今未發現n大于5的鍺烷;
的鍵能較小,鍵容易斷裂,形成的鍺烷不穩定,所以至今未發現n大于5的鍺烷;
![]() 根據配合物的結構分析可知該配合物中存在極性鍵、非極性鍵、配位鍵、氫鍵和
根據配合物的結構分析可知該配合物中存在極性鍵、非極性鍵、配位鍵、氫鍵和![]() 鍵,金屬鍵只存在金屬晶體中,故此配合物中沒有金屬鍵;
鍵,金屬鍵只存在金屬晶體中,故此配合物中沒有金屬鍵;
![]() 分析結構可知,1個Ge和4個O結合,該配合物中
分析結構可知,1個Ge和4個O結合,該配合物中![]() Ⅳ
Ⅳ![]() 的配位數為4,配原子是O;
的配位數為4,配原子是O;
![]() 因為
因為![]() 和
和![]() 中的非羥基氧的數目相同都是1,故磷酸酸性與亞硝酸相近;
中的非羥基氧的數目相同都是1,故磷酸酸性與亞硝酸相近;
![]() 根據均攤法,1個晶胞中,Zn的數目為
根據均攤法,1個晶胞中,Zn的數目為![]() ,Ge的個數為
,Ge的個數為![]() ,磷原子個數為8,密度為
,磷原子個數為8,密度為![]()
![]() ;若把晶胞從上到下平分為2份,再把下方一半平分為8份,則2號P原子位于其中一份的體心。若a、b、c均看作1,以1號Zn為坐標原點,則晶胞中2號P原子的坐標為
;若把晶胞從上到下平分為2份,再把下方一半平分為8份,則2號P原子位于其中一份的體心。若a、b、c均看作1,以1號Zn為坐標原點,則晶胞中2號P原子的坐標為![]() 。
。


 一線名師權威作業本系列答案
一線名師權威作業本系列答案科目:高中化學 來源: 題型:
【題目】25℃時,用濃度為0.100 0 mol·L-1的氫氧化鈉溶液分別滴定20.00 mL濃度均為0.100 0 mol·L-1的二種酸HX、HY(忽略體積變化),實驗數據如下表,下列判斷不正確的是 ( )
數據編號 | 滴入NaOH(aq)的體積/mL | 溶液的pH | |
HX | HY | ||
① | 0 | 3 | 1 |
② | a | 7 | x |
③ | 20.00 | >7 | y |
A. 在相同溫度下,同濃度的兩種酸溶液的導電能力:HX<HY
B. 由表中數據可估算出Ka(HX)≈10-5
C. HY和HX混合,c(H+)=c(X-)+c(Y-)+c(OH-)
D. 上述②反應后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(Ⅰ)CoCl2溶液能發生如下變化:
CoCl2![]() Co(OH)2
Co(OH)2![]() [Co(NH3)6]2+
[Co(NH3)6]2+![]() X
X![]() 晶體Y(CoCl3·5NH3)
晶體Y(CoCl3·5NH3)
向X溶液中加入強堿并加熱至沸騰有氨氣放出,同時產生Co2O3沉淀;若向Y的溶液中加AgNO3溶液,有AgCl沉淀生成,濾出沉淀,再向濾液中加入AgNO3溶液無變化,但加熱至沸騰時又有AgCl沉淀生成,其沉淀量為上次沉淀量的一半。請回答下列問題:
(1)反應②的離子方程式是__________________________________________。
(2)反應①~③中屬于氧化還原反應的是______,配合物Y的化學式為______。
(Ⅱ)一定條件下,將等物質的量的CH4和H2O(g)充入1L恒容密閉容器,發生反應CH4(g)+H2O(g) ![]() CO(g)+3H2(g),達到平衡時測得CO的物質的量為0.10mol。若平衡常數K=27,試計算(要求寫出計算過程,計算結果保留兩位有效數字):
CO(g)+3H2(g),達到平衡時測得CO的物質的量為0.10mol。若平衡常數K=27,試計算(要求寫出計算過程,計算結果保留兩位有效數字):
(1)初始加入容器的甲烷的物質的量__________;
(2)平衡時CH4的體積分數__________;
(3)若溫度不變時再向上述平衡混合物中加入0.01molH2O(g)和0.1molCO,平衡是否移動__________?
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某種碳酸飲料中主要含檸檬酸、碳酸、白砂糖、苯甲酸鈉等成分,常溫下測得其pH約為![]() ,下列說法不正確的是
,下列說法不正確的是![]()
A.檸檬酸的電離會抑制碳酸的電離
B.該碳酸飲料中水的電離受到抑制
C.常溫下,該碳酸飲料中![]() 的值大于純水中
的值大于純水中![]() 的值
的值
D.打開瓶蓋冒出大量氣泡,是因為壓強減小,降低了![]() 的溶解度
的溶解度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】B和Mg在材料科學領域有廣泛的應用和發展前景。
回答下列問題:
(1)下列B原子軌道表達式表示的狀態中,能量更高的是________![]() 填“A”或“B”
填“A”或“B”![]() 。
。
A. ![]() B.
B. ![]()
(2)晶體硼中的基本單元如圖1所示,其中含有12個B原子。![]() 該單元中含有
該單元中含有![]() 鍵的數目為________。
鍵的數目為________。
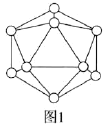
(3)![]() 是重要的還原劑。其中陰離子的立體構型為________,中心原子的雜化形式為________。
是重要的還原劑。其中陰離子的立體構型為________,中心原子的雜化形式為________。
(4)基態Mg原子的核外電子排布式為________;第三周期主族元素中,電負性小于Mg元素的有________![]() 填元素符號,下同
填元素符號,下同![]() ,原子第一電離能小于Mg原子的有________。
,原子第一電離能小于Mg原子的有________。
(5)![]() 和
和![]() 均可作為耐火材料,其原因是________。
均可作為耐火材料,其原因是________。
(6)![]() 常用于光學儀器,其長方體型晶胞結構如圖2所示:
常用于光學儀器,其長方體型晶胞結構如圖2所示:
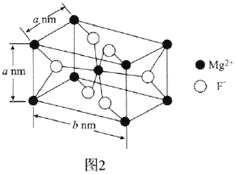
![]() 的配位數為________。
的配位數為________。
![]() 若阿伏加德羅常數的值為
若阿伏加德羅常數的值為![]() ,則
,則![]() 晶體的密度可表示為________
晶體的密度可表示為________![]() 用含a、b、
用含a、b、![]() 的代數式表示
的代數式表示![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表為元素周期表中第四周期的部分元素![]() 從左到右按原子序數遞增排列
從左到右按原子序數遞增排列![]() ,根據要求回答下列問題:
,根據要求回答下列問題:
K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(1)以上元素的基態原子的電子排布中,4s軌道上只有1個電子的元素有______![]() 填元素名稱
填元素名稱![]() 。
。
(2)以上元素中,屬于s區的元素有_________種,屬于d區的元素有______種。
(3)第一電離能![]() ________
________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”,下同
”,下同![]() 。
。
(4)現有含鈦的兩種顏色的晶體,![]() 的配位數均為6,一種為紫色,一種為綠色,相關實驗證明,兩種晶體的組成皆為
的配位數均為6,一種為紫色,一種為綠色,相關實驗證明,兩種晶體的組成皆為![]() 。為測定這兩種晶體的化學式,設計了如下實驗:
。為測定這兩種晶體的化學式,設計了如下實驗:
![]() 分別取等質量的兩種配合物晶體的樣品配成待測溶液;
分別取等質量的兩種配合物晶體的樣品配成待測溶液;
![]() 分別往待測溶液中滴入
分別往待測溶液中滴入![]() 溶液,均產生白色沉淀;
溶液,均產生白色沉淀;
![]() 溶液反應得到的白色沉淀質量為紫色晶體的水溶液反應得到沉淀質量的
溶液反應得到的白色沉淀質量為紫色晶體的水溶液反應得到沉淀質量的![]() 。試推斷紫色晶體的化學式為_________。
。試推斷紫色晶體的化學式為_________。
(5)含有元素K的鹽的焰色反應為__________色。許多金屬鹽都可以發生焰色反應,其原因是____________。
(6)立方氮化硼晶體![]() ,是一種超硬材料,有優異的耐磨性,其晶胞如圖所示。
,是一種超硬材料,有優異的耐磨性,其晶胞如圖所示。
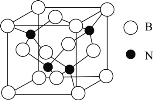
若立方氮化硼晶胞的邊長為![]() ,則立方氮化硼的密度為________g/cm3
,則立方氮化硼的密度為________g/cm3![]() 只要求列算式,不必計算出數值,阿伏加德羅常數的值為NA)。
只要求列算式,不必計算出數值,阿伏加德羅常數的值為NA)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 鹽酸,溶液含R微粒的物質的量分數與pH關系如圖所示
鹽酸,溶液含R微粒的物質的量分數與pH關系如圖所示![]() 不穩定,易轉化為
不穩定,易轉化為![]() 氣體逸出溶液,氣體逸出未畫出,忽略因氣體逸出引起的溶液體積變化
氣體逸出溶液,氣體逸出未畫出,忽略因氣體逸出引起的溶液體積變化![]() 下列說法錯誤的是
下列說法錯誤的是![]()
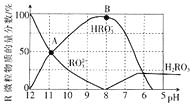
A.![]() 溶液中:
溶液中:![]()
B.當溶液![]() 時,溶液總體積大于40mL
時,溶液總體積大于40mL
C.在B點對應的溶液中,離子濃度最大的是![]()
D.A點對應pH約為![]() ,
,![]() 的水解常數
的水解常數![]() 數量級為
數量級為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解裝置如圖所示:

Ⅰ.當用惰性電極電解時,c為____________極, d極的電極反應_________,電解總反應的化學方程____________________
Ⅱ.(1)若用此裝置進行鐵上鍍銅則c為__________(填鐵或銅),電解液濃度_____________(增大,減小或不變)
(2)電鍍一段時間后對電極進行稱量發現兩極質量差為16克,則電路中轉移的電子___________mol.
Ⅲ.若用此裝置進行粗銅的電解精煉。則要求粗銅板是圖中電極________(填圖中的字母)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某芳香烴A,分子式為C8H10;某烴類衍生物X,分子式為C15H14O3,能使FeCl3溶液顯紫色;J分子內有兩個互為對位的取代基.在一定條件下有如下的轉化關系:(無機物略去)
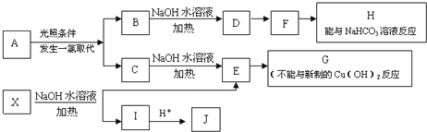
(1)屬于芳香烴類的A的同分異構體中,其沸點的大小關系為______;(不包括A,用結構簡式表示)
(2)J中所含的含氧官能團的名稱為______;
(3)E與H反應的化學方程式是________;反應類型是_______;
(4)B、C的混合物在NaOH乙醇溶液中加熱可以生成同一種有機物I,以I為單體合成的高分子化合物的名稱是______;
(5)已知J有多種同分異構體,寫出一種符合下列性質的J的同分異構體的結構簡式_______;
①與FeCl3溶液作用顯紫色
②與新制Cu(OH)2懸濁液作用產生紅色沉淀
③苯環上的一鹵代物有2種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com