
下表是元素周期表的一部分,有關說法正確的是( )

A.e的氫化物比d的氫化物穩定
B.a、b、e三種元素的原子半徑:e>b>a
C.6種元素中,c元素單質的化學性質最活潑
D. c、e、f的最高價氧化物對應的水化物的酸性依次增強
科目:高中化學 來源:2014高考化學名師知識點精編 專題10鹽類水解與沉淀溶解平衡練習卷(解析版) 題型:選擇題
下列應用與鹽類的水解無關的是( )
A.純堿溶液可去除油污
B.NaCl可用作防腐劑和調味劑
C.TiCl4溶于大量水加熱制備TiO2
D.FeCl3飽和溶液滴入沸水中制Fe(OH)3膠體
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題8電解質溶液練習卷A(解析版) 題型:選擇題
下列敘述正確的是( )
A.0.1 mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.NH4Cl溶液加水稀釋后,恢復至原溫度,pH和KW均增大
C.pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)不相等
D.在NaHCO3溶液中:c(OH-)+c(CO32—)=c(H+)+c(H2CO3)
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題7化學反應速率和化學平衡練習卷A(解析版) 題型:選擇題
納米鈷(Co)常用于CO加氫反應的催化劑,500 K時有催化反應:CO(g)+3H2(g) CH4(g)+H2O(g) ΔH<0。下列有關說法正確的是( )
CH4(g)+H2O(g) ΔH<0。下列有關說法正確的是( )
A.納米技術的應用,提高了催化劑的催化性能
B.縮小容器體積,平衡向正反應方向移動,CO的濃度減小
C.溫度越低,越有利于CO催化加氫
D.從平衡體系中分離出H2O(g)能加快正反應速率
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題7化學反應速率和化學平衡練習卷A(解析版) 題型:選擇題
在常溫下,X2(g)和H2反應生成HX的平衡常數如表中所示,僅依據K的變化,關于等物質的量濃度的H2與X2的反應,下列說法正確的是( )
化學方程式 | 平衡常數K |
F2+H2 | 6.5×1095 |
Cl2+H2 | 2.6×1033 |
Br2+H2 | 1.9×1019 |
I2+H2 | 8.7×102 |
A.F2的轉化率最大
B.X2與H2反應的劇烈程度逐漸減弱
C.X2與H2反應的反應速率依次減小
D.升高溫度,平衡常數都增大
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題6物質結構與元素周期律練習卷(解析版) 題型:選擇題
已知X、Y、Z、W四種短周期元素在周期表中的相對位置如圖所示,下列說法正確的是( )
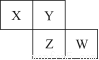
A.Z元素的原子半徑可能比Y元素的小
B.W的原子序數可能是Y的原子序數的2倍
C.W的氣態氫化物的穩定性一定比Y的強
D.Z的化學活潑性一定比X強
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題5化學反應中的能量變化練習卷(解析版) 題型:填空題
化學反應可視為舊鍵斷裂和新鍵形成的過程。現提供H2燃燒反應中有關物質的化學鍵鍵能: H—H鍵鍵能為Q1 kJ·mol-1、H—O鍵鍵能為Q3 kJ·mol-1、O2分子內氧原子間的鍵能為Q2 kJ·mol-1。
(1)請根據上述數據,在圖中標注的數字處,填出能量變化的數值或根據箭頭的指向填寫能量變化是“放出”熱量還是“吸收”熱量。
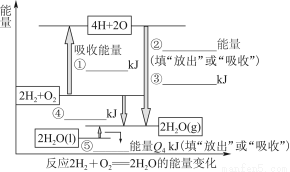
(2)請寫出1 molH2燃燒生成液態水的熱化學反應方程式:____________________________。
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題4離子反應練習卷(解析版) 題型:選擇題
下列有關離子反應或離子方程式的敘述中,正確的是( )
A.能使pH試紙顯深紅色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存
B.惰性電極電解氯化鋁溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.鎂與極稀硝酸反應生成硝酸銨的離子方程式為4Mg+6H++NO3—=4Mg2++NH4++3H2O
D.將10 mL 0.1 mol·L-1 KAl(SO4)2溶液和10 mL 0.2 mol·L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物質的量之比為1∶2
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪復習限時集訓 專題14綜合實驗與探究練習卷A(解析版) 題型:實驗題
一定濃度NaHCO3溶液與CuSO4溶液反應后生成了藍綠色顆粒狀沉淀。就沉淀成分提出了如下三種假設:
假設一:沉淀是CuCO3;假設二:沉淀是Cu(OH)2;
假設三:沉淀是CuCO3和Cu(OH)2的混合物。
(1)寫出假設二,沉淀是Cu(OH)2生成的理由 (用離子方程式表示);
(2)為了探究沉淀的成分,取出了一部分沉淀,滴加稀鹽酸,有氣體放出。憑此現象,判斷沉淀中含有 _;
(3)為了進一步探究沉淀的成分,進而確定假設中何種假設成立,設計實驗,裝置圖如下:
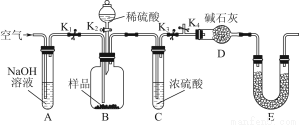
①研究沉淀物組成前,須將沉淀從溶液中分離并凈化。具體操作依次為 _ 、洗滌、干燥;
②裝置E中藥品的名稱是 __作用為 __;
③實驗過程中有以下操作步驟:a.打開K1、K3,關閉K2、K4,通入過量空氣。此步驟的作用是 ;
b.關閉K1、K3,打開K2、K4,充分反應,c.再通入過量空氣時,活塞處于打開的是 _,關閉的是 _。
④若沉淀樣品的質量為m g,裝置D的質量增加了n g;若沉淀樣品為純凈物,m、 n之間的關系為 _
若假設三成立,則Cu(OH)2的質量分數為 _;若不進行步驟c,則會使測得結果 (填“偏高”“無影響”“偏低”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com