
【題目】已知有機物A、B、C、D、E、F、G有如圖轉化關系,其中C的產量可用來衡量一個國家的石油化工發展水平,G的分子式為![]() ,試回答下列有關問題。
,試回答下列有關問題。
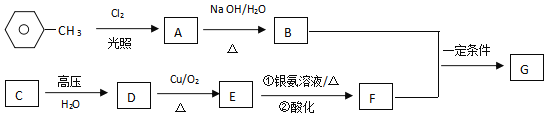
(1)G的結構簡式為______。
(2)C轉化為D的反應類型:______。
(3)寫出B和F反應生成G的化學方程式:______。
(4)寫出同時符合下列條件的G的同分異構體結構簡式______、______。
①苯環上有3個取代基,且有兩個取代基相同;
②能夠與新制的銀氨溶液反應產生光亮的銀鏡;
③核磁共振氫譜共有4種吸收峰。
【答案】![]() 加成反應 CH3COOH+
加成反應 CH3COOH+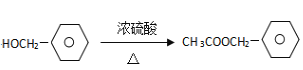 +H2O
+H2O 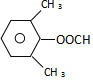

【解析】
C的產量可用來衡量一個國家的石油化工發展水平,則C為![]() ,與水發生加成反應生成D為
,與水發生加成反應生成D為![]() ,D發生催化氧化生成E為
,D發生催化氧化生成E為![]() ,E與銀氨溶液發生氧化反應生成F為
,E與銀氨溶液發生氧化反應生成F為![]() ,甲苯與氯氣在光照條件發生甲基上的取代反應生成A,A發生水解反應生成B,B與F反應生成
,甲苯與氯氣在光照條件發生甲基上的取代反應生成A,A發生水解反應生成B,B與F反應生成![]() ,由G的分子式可知,B為一元醇,故A為
,由G的分子式可知,B為一元醇,故A為![]() ,B為
,B為![]() ,G為
,G為![]() ,以此來解答。
,以此來解答。
⑴由上述分析可知,G為![]() ,名稱為乙酸苯甲酯;故答案為:
,名稱為乙酸苯甲酯;故答案為:![]() 。
。
⑵C轉化為D屬于加成反應,故答案為:加成反應;
⑶B和F反應生成G的化學方程式為![]() ;故答案為:
;故答案為:![]() 。
。
⑷符合下列條件的G的同分異構體:能夠與新制的銀氨溶液反應產生光亮的銀鏡,含有![]() ,苯環上有3個取代基,且有兩個取代基相同,還含有2個
,苯環上有3個取代基,且有兩個取代基相同,還含有2個![]() ,其中氫原子共有四種不同環境的所有物質的結構簡式為
,其中氫原子共有四種不同環境的所有物質的結構簡式為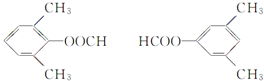 ;
;
故答案為: ;
; 。
。


科目:高中化學 來源: 題型:
【題目】在一定條件下,某可逆反應的正反應速率和逆反應速率隨時間變化的曲線如下 ,下列有關說法不正確的是
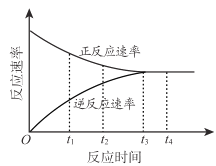
A.t1 時刻,反應向逆反應方向進行
B.t2 時刻,正反應速率大于逆反應速率
C.t3 時刻,反應剛好達到平衡狀態
D.t4時刻,反應限度保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨硼烷(NH3·BH3)電池可在常溫下工作,裝置如圖所示。未加入氨硼烷之前,兩極室質量相等,電池反應為NH3·BH3+3H2O2==NH4BO2+4H2O 。已知H2O2足量,下列說法正確的是( )

A. 正極的電極反應式為2H++2e-===H2↑
B. 電池工作時,H+通過質子交換膜向負極移動
C. 電池工作時,正、負極分別放出H2和NH3
D. 工作足夠長時間后,若左右兩極室質量差為1.9 g,則電路中轉移0.6 mol電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】連二亞硫酸鈉(Na2S2O4)是印染工業的一種常用原料,連二亞硫酸鈉又稱保險粉,可溶于水,但不溶于甲醇,其固體受熱、遇水都會發生反應放出大量的熱,甚至引起燃燒,工業制備流程如圖:
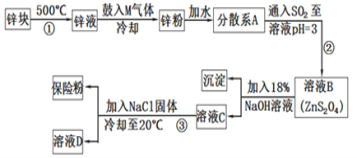
請回答下列問題:
(1)保存連二亞硫酸鈉的注意事項___(任寫一項)。
(2)鼓入的氣體M為空氣的一種主要成分,則M的電子式為___;
(3)流程②的化學方程式為__。
(4)流程③的分離方法步驟為過濾、洗滌、干燥。其中洗滌所用試劑是___;實驗時加入NaCl固體的作用是__。
(5)連二亞硫酸鈉可以用于除去廢水中的重鉻酸根離子(Cr2O72-被轉化為Cr3+,S2O42-被轉化為SO42-),寫出該反應的離子方程式___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究同主族非金屬元素性質的遞變規律,某研究性學習小組的甲同學設計了如圖所示的實驗裝置,其中A裝置內可生成Cl2。
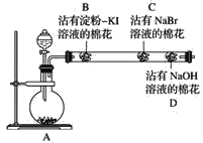
(1)甲同學的部分實驗記錄如下:B處棉花變成藍色;C處棉花變成橙紅色。甲同學由此現象得出的結論是同主族從上到下元素的非金屬性減弱。
①B處發生反應的化學方程式為_________。
②甲同學的結論是________(填“正確”或“不正確”)的,理由是____________________。
(2)乙同學認為應將甲同學實驗中B、C兩處的棉花調換位置,用氯氣先置換出溴,然后溴再與KI接觸,以判斷Br2與KI能否發生反應。該設想是________(填“合理”或“不合理”)的,原因是___
(3)丙同學在甲同學的實驗結束后,取出C處的棉花,將其與另一個沾有淀粉KI溶液的棉花(E)接觸,發現E慢慢出現藍色,結合甲的實驗現象,他認為可以確定同主族元素非金屬性的遞變規律,你同意此種觀點嗎?______(填“同意”或“不同意”),理由是__________
(4)丁同學綜合分析了前面幾位同學的實驗,認為若將沾有Na2S溶液的棉花置于玻璃管中適當的位置,此實驗還可以同時探究同周期元素性質的遞變規律,他提出此觀點的依據是___,預期的現象與結論是___________,相應反應的離子方程式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗的圖示及分析均正確的是( )
選項 | 實驗目的 | 實驗圖示 | 實驗分析 |
A | 催化裂解正戊烷并收集產物 |
| 正戊烷裂解為分子較小的烷烴和烯烴 |
B | 石蠟油的分解并檢驗產物 |
| 石蠟油分解的 產物含有不飽和烴 |
C | 制取并收集乙炔 |
| 用飽和食鹽水代替純水,可達到降低反應速率的目的 |
D | 實驗室制硝基苯 |
| 反應完全后,可用儀器a、b蒸餾提純產品 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物F用于制造香精,可利用下列路線合成。回答下列問題:
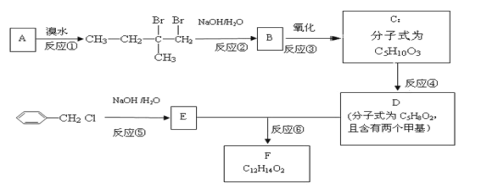
(1)A的化學名稱是___。
(2)B的結構簡式是___。
(3)①~⑥中屬于取代反應的有___(填序號)。
(4)反應⑥的化學方程式為___。
(5)C有多種同分異構體,與C具有相同官能團的有__種(不包括C),其中核磁共振氫譜為四組峰的結構簡式為___(任寫一種)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學家用蘸墨汁書寫后的紙張作為空氣電極,設計并組裝了輕型、柔性、能折疊的可充電鋰空氣電池如下圖1所示,電池的工作原理如下圖2所示。下列有關說法正確的是

A. 放電時,紙張中的纖維素作鋰電池的正極
B. 閉合開關K給鋰電池充電,X為直流電源正極
C. 放電時,Li+由正極經過有機電解質溶液移向負極
D. 充電時,陽極的電極反應式為Li2O2-2e-=O2 +2Li+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵是目前人類使用量最大的金屬,它能形成多種化合物。
(1)取5.6g生鐵與足量的稀硫酸混合反應,無論怎樣進行實驗,最終收集的氣體體積均小于2.24L(標準狀況),最主要的原因是___;所得溶液在長時間放置過程中會慢慢出現淺黃色,試用離子方程式解釋這一變化的原因:___。
(2)ZnFe2O4是一種新型納米材料,可將工業廢氣中的CO轉化為CO2,則ZnFe2O4中Fe元素的化合價為___。ZnFe2O4和CO在1200℃發生反應:6ZnFe2O4+2CO![]() 6ZnO+2CO2+aM(其中a為化合物M的化學計量數),則M的化學式為___,反應中ZnFe2O4作___劑。
6ZnO+2CO2+aM(其中a為化合物M的化學計量數),則M的化學式為___,反應中ZnFe2O4作___劑。
(3)LiFePO4是鋰離子電池材料之一。以FePO4、Li2CO3和單質碳為原料在高溫下制備LiFePO4,該反應還生成一種可然性氣體,則反應的化學方程式為___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com