
研究硫及其化合物對于工農業生產具有重要意義。
(1)圖Ⅰ所示一個容積為4L的密閉容器,內有可移動的隔板。一定溫度(T)下,左室加入2 mol SO3,右室加入2 mol SO2和1 mol O2,在少量催化劑存在下分別發生反應:
左室:
右室:
反應達到平衡時,右室反應過程和能量關系如圖Ⅱ所示。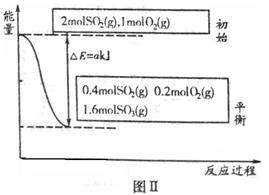
①ΔH2=_______(含a的數學式表示);反應的平衡常數K=_________L·mol-1。
②能說明兩邊反應一定達到平衡的是______________(填序號)。
A.隔板不再移動
B.左右兩邊SO2的物質的量相等
C.左右二室中SO2與O2物質的量之比都是2∶1
③達平衡時,左室反應吸收的熱量為Q1kJ,右室反應吸收的熱量為Q2kJ,則Q1、Q2滿足的關系是_____________(填序號)。
A.Q1=Q2
B.Q1>Q2
C.Q1<Q2
(2)高溫下,熾熱的Cu2S與水蒸氣反應生成金屬銅、H2和SO2(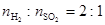 )。
)。
①寫出該反應的化學反應方程式_____________________________________________。
②若有1 mol Cu2S參與反應,則轉移電子的物質的量是_________mol。
(1)①-1.25a kJ/mol 160
② AB ③ C
(2)①Cu2S+2H2O 2Cu+ 2SO2 + H2 ②6
2Cu+ 2SO2 + H2 ②6
解析試題分析:(1)①由圖Ⅱ可以得出,反應物2molSO2平衡時為0.4mol,反應了1.6mol產生akJ的熱量,故該反應的△H2=-2a/1.6=-1.25a kJ/mol相同條件下,左右室反應為等效平衡,達到平衡后兩邊體積相等為2L,
K=c2(SO3)/ c2(SO2) c(O2)=0.82/(0.22×0.1)=160
②A、該反應方程式兩邊化學計量數和不等,平衡移動會導致氣體體積變化,隔板不動,即說明反應達到平衡,正確;B、兩邊是等效平衡,平衡后完全相同,若不相等則沒有達到平衡,正確;C、加入的量是比是2∶1,反應的量為比也是2∶1,所以任何時間左右二室中SO2與O2物質的量之比都是2∶1,錯誤。
③平衡狀態時SO3的物質的量為1.6mol,顯然左室反應的量少,吸收的熱量比右室反應的放出的熱量少,所以Q1<Q2
(2)①該反應化學方程式為Cu2S+2H2O 2Cu+ 2SO2 + H2 ②6
2Cu+ 2SO2 + H2 ②6
考點:考查STS中環境保護有關問題。


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源: 題型:填空題
已知單質硫在通常條件下以S8(斜方硫)的形式存在,而在蒸氣狀態時,含有S2、S4、S6及S8等多種同素異形體,其中S4、S6和S8具有相似的結構特點,其結構如下圖所示:
在一定條件下,S8(s)和O2(g)發生反應依次轉化為SO2(g)和SO3(g)。反應過程和能量關系可用下圖簡單表示(圖中的ΔH表示生成1 mol含硫產物的數據)。
(1)寫出表示S8燃燒熱的熱化學方程式_____________________。
(2)寫出SO3分解生成SO2和O2的熱化學方程式_________________________。
(3)若已知SO2中硫氧鍵的鍵能為d kJ·mol-1,O2中氧氧鍵的鍵能為e kJ·mol-1,則S8分子中硫硫鍵的鍵能為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2013年初,霧霾天氣多次肆虐天津、北京等地區。其中,燃煤和汽車尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為:2NO(g) + 2CO(g)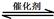 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
①該反應平衡常數表達式
②若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是 (填代號)。
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g)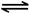 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式: 。
(3)甲烷燃料電池可以提升能量利用率。下圖是利用甲烷燃料電池電解100mL1mol/L食鹽水,電解一段時間后,收集到標準狀況下的氫氣2.24L(設電解后溶液體積不變).
①甲烷燃料電池的負極反應式: 。
②電解后溶液的pH= (忽略氯氣與氫氧化鈉溶液反應)
③陽極產生氣體的體積在標準狀況下是 L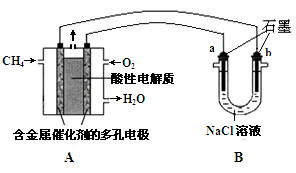
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知反應:3I-(aq)+S2O82-(aq)  I3-(aq)+2SO42-(aq)+Q
I3-(aq)+2SO42-(aq)+Q
(1)寫出反應的平衡常數表達式:K= 。
(2)如圖表示反應過程中有關物質的能量,則反應過程中的Q 0(填>、<、=);(I)、(II)兩曲線中,使用催化劑的是 曲線。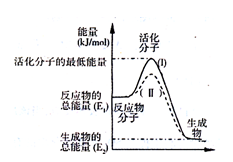
(3)反應的速率可以用I3-與加入的淀粉溶液反應顯藍色的時間t來度量,t越小,反應速率越大。下表是在20℃進行實驗時所記錄的數據
| 實驗編號 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氮及其化合物在工農業生產、生活中有者重要作用。請回答下列問題: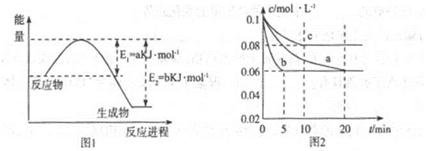
(1)圖1是1molNO2和1molCO反應生成CO2和NO過程中能星變化示意圖(a、b均大于0,)且知:2CO(g)+2NO(g)=N2(g)+2CO2(g)△H=-ckJ·mol-1(c>0)
請寫出CO將NO2還原至N2時的熱化學方程式____________;
(2)圖2是實驗室在三個不同條件的密閉容器中合成氨時,N2的濃度隨時間的變化曲線(以a、b、c表示)。已知三個條件下起始加入濃度均為:c(N2)=0.1mol·L-1,c(H2)=0.3mol·L-1;合成氨的反應:N2(g)+3H2(g) 2NH3(g)△H<0
2NH3(g)△H<0
①計算在a達平衡時H2的轉化率為______;
②由圖2可知,b、c各有一個條件與a不同,則c的條件改變可能是______;
試寫出判斷b與a條件不同的理由____________;
(3)利用圖2中c條件下合成氨(容積固定)。已知化學平衡常數K與溫度(T)的關系如下表:
①試確定K1的相對大小,K1______4.1x106(填寫“>”“-”或“<”)
②下列各項能作為判斷該反應達到化學平衡狀態的依據的 是______(填序號字母)。
A.容器內NH3的濃度保持不變 B.2v(N2)(正)=v(H2)(逆)
C.容器內壓強保持不變 D.混合氣體的密度保持不變
(4)①NH4Cl溶液呈酸性的原因是(用離子反應方程式表示 )______。
②250C時,將pH=x氨水與pH=y的疏酸(且x+y=14,x>11)等體積混合后,所得溶液中各種離子的濃度關系正確的是
A.[SO42-]>[NH4+]>[H+]>[OH-]
B.[NH4+]>[SO42-]>[OH-]>[H+]
C.[NH4+]+[H+]>[OH-]+[SO42-]
D.[NH4+]>[SO42-]>[H+]>[OH-]
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
利用海水資源進行化工生產的部分工藝流程如圖: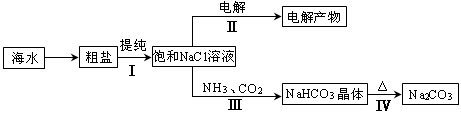
(1)流程I中,欲除去粗鹽中含有的Ca2+、Mg2+、SO42-等離子,需將粗鹽溶解后,按序加入藥品進行沉淀、過濾等。加入藥品和操作的順序可以是 。
a.Na2CO3、NaOH、BaCl2、過濾、鹽酸 b.NaOH、BaCl2、Na2CO3、過濾、鹽酸
c.NaOH、Na2CO3、BaCl2、過濾、鹽酸 d.BaCl2、Na2CO3、NaOH、過濾、鹽酸
(2)流程II中,電解飽和NaCl溶液的離子方程式為 。通電開始后,陽極區產生的氣體是 ,陰極附近溶液pH會 (填“增大”、“減小”或“不變”)。
(3)流程III中,通過反應得到NaHCO3晶體。下圖為NaCl、NH4Cl、NaHCO3、NH4HCO3的溶解度曲線,其中能表示NaHCO3溶解度曲線的是 ,化學反應方程式是 。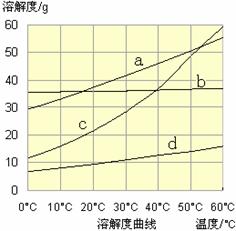
(4)流程IV中,所得純堿常含有少量可溶性雜質,提純它的過程如下:將碳酸鈉樣品加適量水溶解、 、 、過濾、洗滌2-3次,得到純凈Na2CO3?10H2O,Na2CO3?10H2O脫水得到無水碳酸鈉,已知:
Na2CO3·H2O(s)==Na2CO3(s)+H2O(g) ΔH1=+58.73kJ·mol-1
Na2CO3·10H2O(s)==Na2CO3·H2O(s)+9H2O(g) ΔH2=" +473.63" kJ·mol-1
把該過程產生的氣態水完全液化釋放的熱能全部用于生產Na2CO3所需的能耗(不考慮能量損失),若生產1molNa2CO3需要耗能92.36kJ,由此得出:H2O(g)==H2O(l) △H = 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
SNCR-SCR是一種新型的煙氣脫硝技術(除去煙氣中的NOx),其流程如下: 
(1)反應2NO+2CO 2CO2+N2能夠自發進行,則該反應的ΔH 0(填“>”或“<”)。
2CO2+N2能夠自發進行,則該反應的ΔH 0(填“>”或“<”)。
(2)SNCR-SCR流程中發生的主要反應有:
4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g) ΔH=-1627.2kJ?mol-1;
4N2(g)+6H2O(g) ΔH=-1627.2kJ?mol-1;
6NO(g)+4NH3(g) 5N2(g)+6H2O(g) ΔH=-1807.0 kJ?mol-1;
5N2(g)+6H2O(g) ΔH=-1807.0 kJ?mol-1;
6NO2(g)+8NH3(g) 7N2(g)+12H2O(g) ΔH=-2659.9 kJ?mol-1;
7N2(g)+12H2O(g) ΔH=-2659.9 kJ?mol-1;
反應N2(g)+O2(g) 2NO(g)的ΔH= kJ?mol-1。
2NO(g)的ΔH= kJ?mol-1。
(3)NO和NH3在Ag2O催化劑表面的反應活性隨溫度的變化曲線見圖。
①由圖可以看出,脫硝工藝流程應在 (填“有氧”或“無氧”)條件下進行。
②隨著反應溫度的進一步升高,在有氧的條件下NO的轉化率明顯下降的可能原因是 。
(4)NO2也可用尿素[CO(NH2)2]還原,寫出尿素與NO2反應的化學方程式: 。
(5)NO2、O2和熔融NaNO3可制作燃料電池,其原理見圖11。該電池在使用過程中石墨I電極上生成氧化物Y,其電極反應為 。若生成1molY,則理論上需要消耗標準狀況下氧氣的體積為 L。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
Ⅰ.氫氣燃燒生成液態水的熱化學方程式是2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol 請回答下列問題:
(1)生成物能量總和 (填“大于”、“小于”或“等于”)反應物能量總和
(2)若2 mol氫氣完全燃燒生成水蒸氣,則放出的熱量 572 kJ(填“>”、“<”或“=”)
Ⅱ.已知1molCu(s)與適量O2(g)發生反應,生成CuO(s),放出157kJ熱量。寫出該反應的熱化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
高爐煉鐵是冶煉鐵的主要方法。
(1)從煉鐵高爐口排出的尾氣中含有一定量的有毒氣體 (填化學式),會污染空氣。100多年前,人們曾耗巨資改建高爐,結果尾氣中的該物質含量并未減少。高爐煉鐵的主要反應方程式為(設鐵礦石用磁鐵礦) 。
(2)已知:①4Fe(s) + 3O2=2Fe2O3(s) ΔH1
②4Fe3O4(s)+O2(g)=6Fe2O3(s) ΔH2
③3Fe(s)+2O2(g)=Fe3O4(s) ΔH3
則ΔH2= (用含上述ΔH的代數式表示)。
(3)高鐵酸鈉(Na2FeO4)是鐵的一種重要化合物,可用電解法制備,陽極材料為鐵,其電解質溶液應選用_______ (填H2SO4、HNO3、KOH、NaOH、Na2SO4)溶液,原因是_____________,陽極反應式為_________________。
(4)某溫度下,HX的電離平衡常數K為1×10-5。計算該溫度下0.100mol/L的HX溶液的 H+濃度。(平衡時HX的濃度以0.100mol/L計,水的電離忽略不計,寫出計算過程。)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com