
【題目】NA為阿伏伽德羅常數的值。下列說法正確的是
A.2C+SiO2![]() 2CO↑十Si,則每生成4.48 L CO時轉移電子0.4NA
2CO↑十Si,則每生成4.48 L CO時轉移電子0.4NA
B.1 mol NH3完全溶于水,則n(NH3·H2O)+n(NH4+)=l mol
C.氯化鋁在氣態時以雙聚分子存在,其球棍模型為![]() ,則1 mol雙聚分子中含有電子數為128NA
,則1 mol雙聚分子中含有電子數為128NA
D.2SO2(g)+O2(g)2SO3(l) △H=-a kJ·mol-1(a>0),則每生成2 mol SO3(l)時吸熱a kJ
【答案】C
【解析】
A. 2C+SiO2![]() 2CO↑+Si,無標準狀況,不能求出4.48L CO的物質的量,A錯誤;
2CO↑+Si,無標準狀況,不能求出4.48L CO的物質的量,A錯誤;
B. 1 mol NH3完全溶于水,含N的微粒有NH3·H2O、NH4+、NH3,根據物料守恒,n(NH3·H2O)+n(NH4+)+n(NH3)=l mol,B錯誤;
C. 氯化鋁在氣態時以雙聚分子存在,其球棍模型為![]() ,則1mol雙聚分子中含有2NA個Al,6NA個Cl,電子數為13×2NA+17×6NA=128 NA,C正確;
,則1mol雙聚分子中含有2NA個Al,6NA個Cl,電子數為13×2NA+17×6NA=128 NA,C正確;
D. 2SO2(g)+O2(g)2SO3(l)△H=-a kJ·mol-1(a>0),是放熱反應,每生成2mol SO3(l)時放熱a kJ,D錯誤;
故選C。


科目:高中化學 來源: 題型:
【題目】中國不少古詩詞清晰描述了當時人們的生活和社會的發展,如劉禹錫的《浪淘沙》“日照澄洲江霧開,淘金女伴滿江隈,美人首飾侯王印,盡是沙中浪底來。”下列有關本詩中蘊含的化學知識認知正確的是
A.霧的分散質粒子直徑范圍是1~100nmB.淘金原理與化學上的萃取一致
C.沙子的主要成分是![]() D.“沙中浪底來”指的是金的氧化物
D.“沙中浪底來”指的是金的氧化物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬的冶煉方法有很多,有加熱法,熱還原法、 電解法、濕法冶金等:我國古代利用鐵和硫酸銅溶液反應煉銅,屬于___(填冶煉的方法);鋁熱反應是鋁與一些金屬氧化物在高溫下反應,屬于___(填冶煉的方法);寫出鋁與四氧化三鐵的反應方程式:____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】層狀復合金屬氫氧化物(簡稱“層狀氫氧化物”),主體層板由二元(或多元)金屬氫氧化物層構成,層間陰離子可以被其他陰離子取代,因此可以作為離子交換劑,在材料、化工、醫藥和環境保護等方面有著廣泛的用途。鎂鋁碳酸根型水滑石是人們最早發現的層狀氫氧化物。回答下列問題:
(1)下列狀態的鎂中,電離最外層一個電子所需能量最小的是___________(填標號)。
A. B.
B. C.
C.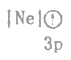 D.
D.
(2)一種水滑石的化學式為Mg4Al2(OH)12CO3H2O.其層板結構如圖1。CO32-中碳的雜化類型是____。在圖中最小的一個二維菱形晶胞(以圖中Al為頂點)中含有___________個Al3+。每個鎂氧八面體周圍有_______________個相鄰鋁氧八面體和_______________個相鄰鎂氧八面體。
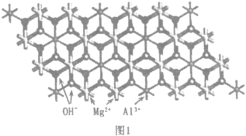
(3)水滑石中氫氧化物層的OH-和層間陰離子間的主要作用力為_______________,水滑石作為離子交換劑,去除水體中陰離子去除效果依次為:PO43->CrO42->NO3-,其原因是___________
(4)當加熱到一定溫度時,水滑石類化合物會發生分解,部分產物轉化為尖晶石結構的MgxAlyOz,晶體結構如圖2所示,它的化學式為___________;A塊、B塊均為邊長為apm的立方體,設阿伏加德羅常數為NA,則最近的兩個Al離子之間的距離為___________pm,密度為___________gcm-3(列出計算表達式)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于 ,下列說法正確的是
,下列說法正確的是
A.該物質可由兩種單體分子之間通過加聚反應生成
B.該物質的有機物單體,不能使FeCl3溶液顯紫色
C.0.1 mol單體(有機物)與足量Na反應,生成2.24 L H2(標準狀況)
D.1 mol該物質與足量NaOH溶液反應,最多可消耗2n mol NaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了講授“氯氣的性質和用途”,一老師以二氧化錳和濃鹽酸為主要原料制取氯氣,并設計了如圖所示裝置(其中A是連有注射器針頭的橡皮管,針頭已插入并穿過橡皮塞)進行教學。
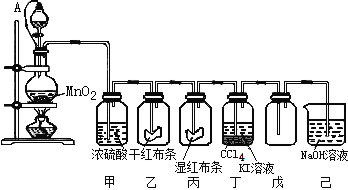
試回答下列問題:
(1)乙和丙中的現象分別是 ____________________、____________________;由上述現象可得出結論:_____________________(寫化學式)具有漂白作用;
(2)分離丁中液體的方法是 _______;
(3)圓底燒瓶內發生反應的化學方程式為__________________________________;
(4)分液漏斗與燒瓶連接橡皮管的目的是 __________________________________;
(5)己燒杯中反應的離子方程式為:________________________________________;
(6)將產生的Cl2通入FeCl2溶液中得到含有FeCl2和FeCl3的混合物,實驗測得混合物中n(Fe元素)∶n(Cl元素)=1:2.4,則該溶液中Fe2+和Fe3+的物質的量濃度之比約為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于下列各圖的敘述,正確的是( )

A. 根據圖甲(S表示溶解度)表示A、B兩物質的溶解度隨溫度變化情況,將A、B飽和溶液分別由t1℃升溫至t2℃時,溶質的質量分數A=B
B. 圖乙表示25℃時,用0.1mol ·L-1鹽酸滴定20mL 0.1mol ·L-1NaOH溶液的pH隨加入酸體積的變化
C. 根據圖丙表示Al3+與OH-反應時含鋁微粒濃度變化曲線,圖中a點溶液中大量存在Al3+
D. 根據圖丁可判斷可逆反應“A2(g)+3B2(g)![]() 2AB3(g)”的ΔH>0
2AB3(g)”的ΔH>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.2-丁烯不存在順反異構體
B.已知丙烷的二氯代物有四種異構體,則其六氯代物的異構體數目為六種
C.菲的結構簡式為 ,它與硝酸反應,可生成4種一硝基取代物
,它與硝酸反應,可生成4種一硝基取代物
D.乙醛的核磁共振氫譜中有二個峰,峰面積之比是1:3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T0℃時,在2 L的密閉容器中發生反應:X(g)+Y(g)![]() Z(g)(未配平),各物質的物質的量隨時間變化的關系如圖a所示。其他條件相同,溫度分別為T1℃、T2℃時發生反應,X的物質的量隨時間變化的關系如圖b所示。下列敘述正確的是( )
Z(g)(未配平),各物質的物質的量隨時間變化的關系如圖a所示。其他條件相同,溫度分別為T1℃、T2℃時發生反應,X的物質的量隨時間變化的關系如圖b所示。下列敘述正確的是( )
圖a 圖b
圖b
A.該反應的正反應是吸熱反應
B.T1℃時,若該反應的平衡常數K =50,則T1<T0
C.圖a中反應達到平衡時,Y的轉化率為37.5%
D.T0℃,從反應開始到平衡時:v(X)=0.083 mol·L-1·min-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com