
【題目】下列反應的離子方程式表示正確的是 ( )
A.碳酸鈣與醋酸溶液反應:CaCO3 +2H+ =Ca2++ CO2 ↑+H2O
B.苯酚鈉溶液和少量CO2反應: 2C6H5O +CO2 +H2O=2C6H5OH +CO32
C.溴乙烷與氫氧化鈉溶液共熱:C2H5Br+OH ![]() C2H5OH+Br
C2H5OH+Br
D.用銀氨溶液檢驗乙醛的醛基:CH3CHO + 2Ag(NH4)2OH ![]() CH3COO- + NH4+ +3NH3 + 2Ag↓+H2O
CH3COO- + NH4+ +3NH3 + 2Ag↓+H2O
科目:高中化學 來源: 題型:
【題目】在一定溫度下,將等量的氣體分別通入起始體積相同的密閉容器Ⅰ和Ⅱ中,使其發生反應,t0時容器Ⅰ中達到化學平衡,X、Y、Z的物質的量的變化如圖所示。則下列有關推斷正確的是( )
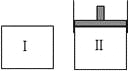

A. 該反應的化學方程式為:3X+2Y![]() 2Z
2Z
B. 若兩容器中均達到平衡時,兩容器的體積V(Ⅰ)<V(Ⅱ),則容器Ⅱ達到平衡所需時間小于t0
C. 若兩容器中均達到平衡時,兩容器中Z的物質的量分數相同,則Y為固態或液態
D. 若達平衡后,對容器Ⅱ升高溫度時,其體積增大,說明Z發生的反應為吸熱反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,可逆反應A(g)+3B(g)![]() 2C(g)達到平衡狀態的標志是( )
2C(g)達到平衡狀態的標志是( )
A.C的生成速率與C的分解速率相等
B.A、B、C的分子數之比為1:3:2
C.單位時間生成nmolA,同時生成3nmolB
D.A、B、C的濃度相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,用NaOH溶液作![]() 捕捉劑不僅可以降低碳排放,而且可得到重要的化工產品
捕捉劑不僅可以降低碳排放,而且可得到重要的化工產品![]()
(1)若某次捕捉后得到![]() 的溶液,則溶液中
的溶液,則溶液中![]() :
:![]() ______
______![]() 常溫下
常溫下![]() 、
、![]() ,
,
(2)欲用5L![]() 溶液將
溶液將![]()
![]() 固體全都轉化為
固體全都轉化為![]() ,則所用的
,則所用的![]() 溶液的物質的量濃度至少為______。
溶液的物質的量濃度至少為______。![]() 已知:常溫下
已知:常溫下![]() 、
、![]() 忽略溶液體積的變化
忽略溶液體積的變化![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】目前世界上60%的鎂是從海水中提取的.主要步驟如下:
下列說法不正確的是( )
A. 為使海水中的MgSO4轉化成Mg(OH)2,試劑①可選擇石灰乳
B. 加入試劑①后,分離得到Mg(OH)2沉淀的方法是過濾
C. 加入試劑②反應的離子方程式為:OH﹣+H+=H2O
D. 通過電解熔融的無水MgCl2得到48gMg,共轉移4mol電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合金是建造航空母艦的主體材料.
(1)航母升降機可由鋁合金制造.
①鋁元素在周期表中的位置為 ______ ![]() 工業用鋁土礦冶煉鋁的化學方程式 ______ .
工業用鋁土礦冶煉鋁的化學方程式 ______ .
②![]() 合金焊接前用NaOH溶液處理
合金焊接前用NaOH溶液處理![]() 膜,其化學方程式為 ______ .
膜,其化學方程式為 ______ .
(2)![]() 也是重要的鋁鹽,其無水
也是重要的鋁鹽,其無水![]() 升華
升華![]() 遇潮濕空氣即產生大量白霧,實驗室可用下列裝置制備.
遇潮濕空氣即產生大量白霧,實驗室可用下列裝置制備.
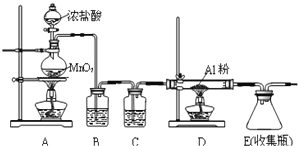
①裝置在實驗開始前應 ______ ,操作方法是: ______ .
②裝置B中盛放飽和NaCl溶液,該裝置的主要作用是 ______ ![]() 裝置C中盛放 ______ .
裝置C中盛放 ______ .
③裝置A中發生的離子反應 ______ .
④該裝置缺少尾氣處理裝置,尾氣處理裝置用的儀器是 ______ 裝堿石灰.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】425℃時,在兩個1L密閉容器中分別發生化學反應,物質的濃度隨時間的變化如圖所示。下列敘述錯誤的是( )
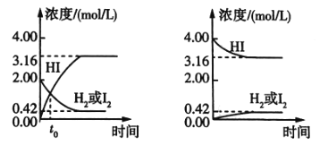
A.圖①中t0時,三種物質的物質的量相等
B.圖①中![]() 時,反應達到平衡狀態
時,反應達到平衡狀態
C.圖②中的可逆反應為2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)
D.圖①②中,當c(HI)=3.16mol/L時,兩容器中的反應均達到平衡狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設![]() 為阿伏加德羅常數的值,下列敘述正確的是( )
為阿伏加德羅常數的值,下列敘述正確的是( )
A.標準狀況下,![]() 分子中含有
分子中含有![]()
![]() 個碳氧雙鍵
個碳氧雙鍵
B.一定溫度下,![]() 完全反應轉移的電子數一定為
完全反應轉移的電子數一定為![]()
![]()
C.常溫常壓下,![]() 固體中離子總數為
固體中離子總數為![]()
![]()
D.常溫常壓下,![]() 溶液中
溶液中![]() 和
和![]() 數目之和為
數目之和為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用0.1 mol·L-1 NaOH溶液滴定40 mL 0.1 mol·L-1 H2SO3溶液,所得滴定曲線如圖所示(忽略混合時溶液體積的變化)。下列敘述錯誤的是( )
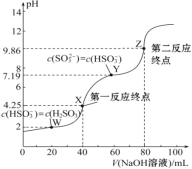
A. Ka2(H2SO3)的數量級為10-8
B. 若滴定到第一反應終點,可用甲基橙作指示劑
C. 圖中Z點對應的溶液中:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)
D. 圖中Y點對應的溶液中:3c(SO32-)=c(Na+)+c(H+)-c(OH-)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com