
分析 該題綜合性比較強,第一問可根據質量守恒定律和復分解反應的特征來解答.在(2)中要求先會寫出:A+CaCl2═B↓+2NaCl的真正的化學方程式即 Na2CO3+CaCl2=CaCO3↓+2NaCl然后根據題中的信息求出A溶液和CaCl2溶液的質量以及生成的NaCl的質量.進而便可求出濾出B后所得溶液中NaCl的質量分數.
解答 解:(1)根據復分解反應的特征A物質必定含有的金屬元素是:鈉;
設A的相對分子質量為m.B的相對分子質量為n.根據質量守恒定律則有m+(40+35.5×2)═n+2(23+35.5)
所以m+111=n+117
故A和B的相對分子質量之差為 117-111=6
故答案為:鈉,6;
(2)解:由題意判斷:B是CaCO3,A是Na2CO3.
設CaCO3的質量為w,Na2CO3溶液的質量為x,CaCl2溶液的質量為y,生成NaCl的質量為z
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
w 4.4g
$\frac{100}{44}=\frac{w}{4.4g}$
w=10g
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111 100 117
10%x 10%y 10g z
$\frac{106}{10%x}=\frac{111}{10%y}=\frac{100}{10g}=\frac{117}{z}$
x=106g;y=111g;z=11.7g
NaCl溶液中溶質的質量分數為 $\frac{11.7g}{106g+111g-10g}$×100%=5.7%
答:濾出B后所得溶液中NaCl的質量分數是5.7%.
點評 本題是一道綜合性比較強的試題,難度比較大,要求學生要掌握復分解反應的特征、質量守恒定律、以及能根據化學方程式進行計算、和會求反應后溶液中溶質質量分數.


科目:初中化學 來源: 題型:實驗探究題
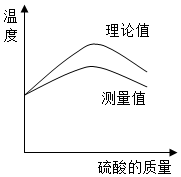 實驗小組欲利用氫氧化鈉溶液與硫酸反應探究中和反應過程中的熱量變化.請你參與探究實驗.
實驗小組欲利用氫氧化鈉溶液與硫酸反應探究中和反應過程中的熱量變化.請你參與探究實驗.查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
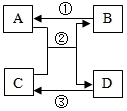 A~D是初中化學所學的常見物質,其轉化關系如圖所示(部分反應物和生成物、反應條件已略去),A、B常溫下為無色氣體且組成元素相同,C、D均為黑色粉末.請回答下列問題:
A~D是初中化學所學的常見物質,其轉化關系如圖所示(部分反應物和生成物、反應條件已略去),A、B常溫下為無色氣體且組成元素相同,C、D均為黑色粉末.請回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
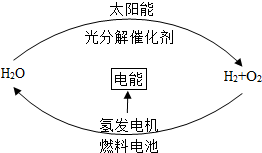 目前,科學家提出了一種最經濟最理想的獲得氫能源的循環體系,如圖所示.下列說法正確的是( )
目前,科學家提出了一種最經濟最理想的獲得氫能源的循環體系,如圖所示.下列說法正確的是( )| A. | 燃料電池能夠使化學反應產生的能量轉化為電能 | |
| B. | 在此循環中發生了反應:2H2O$\frac{\underline{\;電解\;}}{\;}$2H2↑+O2↑ | |
| C. | 該氫能源的循環體系能夠實現電能和太陽能的相互轉化 | |
| D. | 目前未能使用氫氣作為普通燃料的主要原因是氫氣易爆炸 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 如圖是某口服液標簽的部分內容.
如圖是某口服液標簽的部分內容.查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
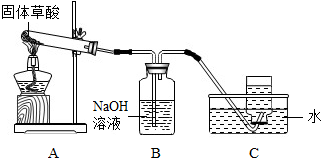
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 用取過酸的滴管直接取酚酞試液 | B. | 稀釋濃硫酸時將水倒入濃硫酸中 | ||
| C. | 多取的藥品放入指定的容器內 | D. | 過濾時用玻璃棒在漏斗內攪拌 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 如圖為實驗室制取氫氣的發生裝置,若液面剛好不與鋅粒接觸面又無酸液可加,要得到氫氣且保證H2的量不受影響,可從長頸漏斗中加入適量試劑的一組是( )
如圖為實驗室制取氫氣的發生裝置,若液面剛好不與鋅粒接觸面又無酸液可加,要得到氫氣且保證H2的量不受影響,可從長頸漏斗中加入適量試劑的一組是( )| A. | ①② | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com