

 激活思維優加課堂系列答案
激活思維優加課堂系列答案 活力試卷系列答案
活力試卷系列答案科目:初中化學 來源: 題型:
 19、(1)鐵是生活中常用的金屬.右圖是某“取暖片”外包裝的圖片.該“取暖片”中發熱劑主要成分有鐵粉、活性炭、氯化鈉、水等,其發熱是利用鐵生銹時會放熱.
19、(1)鐵是生活中常用的金屬.右圖是某“取暖片”外包裝的圖片.該“取暖片”中發熱劑主要成分有鐵粉、活性炭、氯化鈉、水等,其發熱是利用鐵生銹時會放熱.查看答案和解析>>
科目:初中化學 來源: 題型:
 33、人類生活離不開金屬.
33、人類生活離不開金屬.查看答案和解析>>
科目:初中化學 來源: 題型:

查看答案和解析>>
科目:初中化學 來源: 題型:
 人類生活離不開金屬.鐵是生活中常用的金屬.右圖是某“取暖片”外包裝的圖片.該“取暖片”中發熱劑主要成分有鐵粉、活性炭、氯化鈉、水等,其發熱是利用鐵生銹時會放熱.
人類生活離不開金屬.鐵是生活中常用的金屬.右圖是某“取暖片”外包裝的圖片.該“取暖片”中發熱劑主要成分有鐵粉、活性炭、氯化鈉、水等,其發熱是利用鐵生銹時會放熱. 查看答案和解析>>
科目:初中化學 來源: 題型:
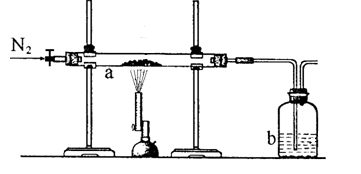
 鐵是生活中常用的金屬.是某“取暖片”外包裝的圖片.該“取暖片”中發熱劑主要成分有鐵粉、氯化鈉、水、活性炭等,其發熱是利用鐵生銹時會放熱的原理.
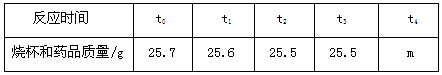
鐵是生活中常用的金屬.是某“取暖片”外包裝的圖片.該“取暖片”中發熱劑主要成分有鐵粉、氯化鈉、水、活性炭等,其發熱是利用鐵生銹時會放熱的原理.| 反應時間 | t0 | t1 | t2 | t3 | t4 |
| 燒杯和藥品質量/g | 25.7 | 25.6 | 25.5 | 25.5 | m |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com