
 海洋資源十分豐富.
海洋資源十分豐富.
| 實驗序號 | 第一次實驗 | 第二次實驗 | 第三次實驗 |
| 所取海水質量/kg | 100 | 100 | 100 |
| 生成沉淀質量/kg | 0.28 | 0.29 | 0.30 |
 Mg+Cl2↑;電能 化學能.
Mg+Cl2↑;電能 化學能. Mg3N2;
Mg3N2;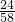 =0.12kg,
=0.12kg, ×100%=0.12%
×100%=0.12% Mg3N2;0.12%
Mg3N2;0.12%

 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:閱讀理解
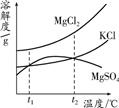 海洋資源十分豐富.
海洋資源十分豐富.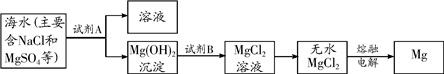
| 實驗序號 | 第一次實驗 | 第二次實驗 | 第三次實驗 |
| 所取海水質量/kg | 100 | 100 | 100 |
| 生成沉淀質量/kg | 0.28 | 0.29 | 0.30 |
查看答案和解析>>
科目:初中化學 來源: 題型:


查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解

| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:
 我國有較長的海岸線,海洋資源十分豐富.
我國有較長的海岸線,海洋資源十分豐富.
查看答案和解析>>
科目:初中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com