
Ęų╬÷ Ż©1Ż®Įī┘Š▀ėą┴╝║├Ą─ī¦ļŖąįĪóī¦¤ßąį║═čėš╣ąįŻ╗
Ż©2Ż®ĶFõPĄ─ų„ę¬│╔Ęų╩Ūč§╗»ĶFŻ¼č§╗»ĶF║═ŽĪ¹}╦ßĘ┤æ¬╔·│╔┬╚╗»ĶF║═╦«Ż╗
Ż©3Ż®õX▒╚Ń~╗ŅØŖŻ¼Ń~▒╚Ńy╗ŅØŖŻ╗
Ż©4Ż®µV▒╚ĶF╗ŅØŖŻ¼ĶF▒╚Ń~╗ŅØŖŻ¼į┌┬╚╗»Ń~║═┬╚╗»µVĄ─╗ņ║Ž╚▄ę║ųą╝ė╚ļę╗Č©┘|┴┐Ą─ĶFĘ█Ż¼ĶF▓╗─▄║═┬╚╗»µVĘ┤æ¬Ż¼─▄║═┬╚╗»Ń~Ę┤æ¬╔·│╔┬╚╗»üåĶF║═Ń~Ż╗
Ń~▓╗─▄║═ŽĪ¹}╦ßĘ┤æ¬Ż¼ĶF─▄║═ŽĪ¹}╦ßĘ┤æ¬╔·│╔┬╚╗»üåĶF║═ÜõÜŌŻ«
ĮŌ┤ ĮŌŻ║Ż©1Ż®AŻ«ŃKĮ’ŚŲĘų„ę¬└¹ė├┴╦Ųõčėš╣ąįŻ╗
BŻ«ĶFÕüų„ę¬└¹ė├┴╦Ųõī¦¤ßąįŻ╗
CŻ«õXī¦ŠĆų„ę¬└¹ė├┴╦Ųõī¦ļŖąįŻ«
╣╩▀xŻ║CŻ«
Ż©2Ż®╔·╗ŅųąĶFųŲŲĘĢ■░l╔·Ė»╬g«a╔·ĶFõPŻ¼ĶFõPĄ─ų„ę¬│╔Ęų╩Ūč§╗»ĶFŻ¼ė├ŽĪ¹}╦ß│²ĶFõPĄ─╗»īWĘĮ│╠╩Į×ķŻ║Fe2O3+6HCl©T2FeCl3+3H2OŻ«
╣╩╠ŅŻ║Fe2O3+6HCl©T2FeCl3+3H2OŻ«
Ż©3Ż®ó┘īóõXĪóŃyĘųäeĮ■╚ļĄĮ┴“╦ßŃ~╚▄ę║ųąŻ¼õX▒Ē├µĖĮų°ę╗īė╝t╔½╣╠¾wŻ¼šf├„õX▒╚Ń~╗ŅØŖŻ¼Ńy▒Ē├µ¤o├„’@¼FŽ¾Ż¼šf├„Ń~▒╚Ńy╗ŅØŖŻ¼įō▀xĒŚ┐╔ąąŻ╗
ó┌īóŃyĘųäeĮ■╚ļĄĮ┴“╦ßõXĪó┴“╦ßŃ~╚▄ę║ųąŻ¼Č╝¤o├„’@¼FŽ¾Ż¼šf├„Ńy▓╗╚ńŃ~ĪóõX╗ŅØŖŻ¼Č°¤oĘ©┤_Č©õX║═Ń~Ą─╗ŅØŖąįŻ¼įō▀xĒŚ▓╗┐╔ąąŻ╗
ó█īóŃ~ĪóŃyĘųäeĮ■╚ļĄĮ┴“╦ßõX╚▄ę║ųąŻ¼Č╝¤o├„’@¼FŽ¾Ż¼šf├„Ń~║═ŃyČ╝▓╗╚ńõX╗ŅØŖŻ¼¤oĘ©┤_Č©Ń~║═ŃyĄ─╗ŅØŖąįŻ¼įō▀xĒŚ▓╗┐╔ąąŻ╗
ó▄īóŃ~Į■╚ļĄĮ┴“╦ßõXųąĢrŻ¼¤o├„’@¼FŽ¾Ż¼šf├„õX▒╚Ń~╗ŅØŖŻ¼īóŃ~Į■╚ļĄĮŽ§╦ßŃy╚▄ę║ųąĢrŻ¼Ń~▒Ē├µĖĮų°ę╗īėŃy░ū╔½╣╠¾wŻ¼šf├„Ń~▒╚Ńy╗ŅØŖŻ¼įō▀xĒŚ┐╔ąąŻ«
╣╩▀xŻ║ó┘ó▄Ż«
Ż©4Ż®ó┘×Vę║ųąę╗Č©║¼ėąĄ─╚▄┘|╩Ūø]ėąĘ┤æ¬Ą─┬╚╗»µV║═Ę┤æ¬╔·│╔Ą─┬╚╗»üåĶFŻ╗
ó┌Ž“×Vį³ųąĄ╬╝ėŽĪ¹}╦߯¼ėąÜŌ┼▌«a╔·Ż¼šf├„ĶF▀^┴┐Ż¼ät×Vį³ųąę╗Č©║¼ėąĄ─╬’┘|╩ŪĘ┤æ¬╔·│╔Ą─Ń~║═▀^┴┐Ą─ĶFŻ«
╣╩╠ŅŻ║MgCl2ĪóFeCl2Ż╗CuĪóFeŻ«
³cįu ę¬Ģ■└¹ė├Įī┘╗ŅäėĒśą“▒ĒĘų╬÷īŹ“ׯ¼ÜõŪ░▀ģĄ─Įī┘Ģ■┼cŽĪ┴“╦ßĪó¹}╦ßĘ┤æ¬Ż¼Ą½Üõ║¾▀ģĄ─Įī┘▓╗Ģ■┼cŽĪ┴“╦ßĪó¹}╦ßĘ┤æ¬Ż¼Ū░▀ģĄ─Įī┘Ģ■░č║¾▀ģĄ─Įī┘Å─Ųõ¹}╚▄ę║ųąų├ōQ│÷üĒŻ«



| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║▀xō±Ņ}
| AŻ« |  | BŻ« |  | CŻ« |  | DŻ« |  |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║▀xō±Ņ}
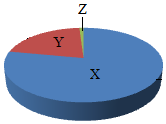 łD×ķ┐šÜŌ│╔Ęų╩ŠęŌłDŻ©░┤¾wĘeĘųöĄėŗ╦ŃŻ®Ż¼ŲõųąĪ░XĪ▒┤·▒ĒĄ─╩ŪŻ©ĪĪĪĪŻ®
łD×ķ┐šÜŌ│╔Ęų╩ŠęŌłDŻ©░┤¾wĘeĘųöĄėŗ╦ŃŻ®Ż¼ŲõųąĪ░XĪ▒┤·▒ĒĄ─╩ŪŻ©ĪĪĪĪŻ®| AŻ« | Ą¬ÜŌ | BŻ« | č§ÜŌ | CŻ« | Č■č§╗»╠╝ | DŻ« | ŽĪėąÜŌ¾w |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║╠Ņ┐šŅ}
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║▀xō±Ņ}
| AŻ« | NaHCO3╩ŪēA | |
| BŻ« | įōĘ┤æ¬ųą╦─ĘN╬’┘|Č╝╩Ū¹} | |
| CŻ« | įōĘ┤æ¬▓╗Ę¹║ŽÅ═ĘųĮŌĘ┤æ¬░l╔·Ą─Śl╝■ | |
| DŻ« | ╬÷│÷Š¦¾w║¾╩ŻėÓ╚▄ę║ųąĄ─╚▄┘|ų╗ėąNH4Clę╗ĘN |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║▀xō±Ņ}
| AŻ« | 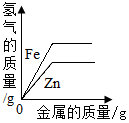 | BŻ« | 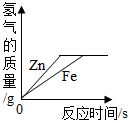 | CŻ« | 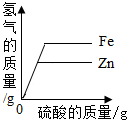 | DŻ« | 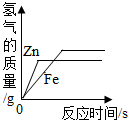 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║ĮŌ┤Ņ}
 Ė∙ō■Ž┬▒ĒīŹ“ׯ¼╗ž┤ŽÓĻPå¢Ņ}
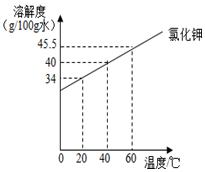
Ė∙ō■Ž┬▒ĒīŹ“ׯ¼╗ž┤ŽÓĻPå¢Ņ}| īŹ“×▓Į¾E | īŹ“×▓┘ū„ | īŹ“×¼FŽ¾ |
| ó± | į┌╩óėą100g╦«Ą─¤²▒ŁųąŻ¼╝ė╚ļ25g┬╚╗»ŌøŻ¼öć░ĶŻ¼╗ųÅ═ĄĮ20ĪµŻ« | ╚½▓┐╚▄ĮŌ |
| ó“ | į┘╝ėXg┬╚╗»ŌøŻ¼öć░ĶŻ¼╗ųÅ═ĄĮ20ĪµŻ¼ŪĪ║├’¢║═Ż« | ╚½▓┐╚▄ĮŌ |
| ó¾ | į┘╝ė6g┬╚╗»ŌøŻ¼öć░ĶŻ¼╗ųÅ═ĄĮ20Īµ | ╣╠¾w▓╗╚▄ |
| ó¶ | ╝ė¤ß | ╚½▓┐╚▄ĮŌ |
| ó§ | └õģsų┴20Īµ | ėą╣╠¾w╬÷│÷ |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║ĮŌ┤Ņ}
 Ī░┐ū├„¤¶Ī▒ėųĮą╠ņ¤¶Ż©╚ńłD╦∙╩ŠŻ®Ż«ę╗░ŃĄ─┐ū├„¤¶╩Ūė├ų±Ų¼╝▄│╔łA═░ą╬Ż¼═Ō├µęį▒Ī╝ł├▄├▄░³ć·Ūęķ_┐┌│»Ž┬Ż«ė¹³c¤¶╔²┐šĢrŻ¼į┌Ąū▓┐Ą─ų¦╝▄ųąķgĮē╔Žę╗ēKš┤ėą├║ė═╗“ŠŲŠ½Ą─┤ų▓╝Ż¼Ę┼’wŪ░īó┤ų▓╝³c╚╝Ż¼ĖąėXĄĮ┐ū├„¤¶Ą─▒Ī╝ł┼“├øūā▌p║¾▒ŃĘ┼╩ųŻ¼ļS║¾š¹éƤ¶Š═Ģ■╚Į╚Į╔²┐šŻ«╚¶─│┐ū├„¤¶▀xė├Ą─╚╝┴Ž×ķŠŲŠ½Ż©C2H5OHŻ®Ż¼šłīæ│÷ŠŲŠ½═Ļ╚½╚╝¤²Ą─╗»īWĘĮ│╠╩ĮŻ║C2H5OH+3O2$\frac{\underline{\;³c╚╝\;}}{\;}$2CO2+3H2OŻ«
Ī░┐ū├„¤¶Ī▒ėųĮą╠ņ¤¶Ż©╚ńłD╦∙╩ŠŻ®Ż«ę╗░ŃĄ─┐ū├„¤¶╩Ūė├ų±Ų¼╝▄│╔łA═░ą╬Ż¼═Ō├µęį▒Ī╝ł├▄├▄░³ć·Ūęķ_┐┌│»Ž┬Ż«ė¹³c¤¶╔²┐šĢrŻ¼į┌Ąū▓┐Ą─ų¦╝▄ųąķgĮē╔Žę╗ēKš┤ėą├║ė═╗“ŠŲŠ½Ą─┤ų▓╝Ż¼Ę┼’wŪ░īó┤ų▓╝³c╚╝Ż¼ĖąėXĄĮ┐ū├„¤¶Ą─▒Ī╝ł┼“├øūā▌p║¾▒ŃĘ┼╩ųŻ¼ļS║¾š¹éƤ¶Š═Ģ■╚Į╚Į╔²┐šŻ«╚¶─│┐ū├„¤¶▀xė├Ą─╚╝┴Ž×ķŠŲŠ½Ż©C2H5OHŻ®Ż¼šłīæ│÷ŠŲŠ½═Ļ╚½╚╝¤²Ą─╗»īWĘĮ│╠╩ĮŻ║C2H5OH+3O2$\frac{\underline{\;³c╚╝\;}}{\;}$2CO2+3H2OŻ«▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║│§ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║ĮŌ┤Ņ}
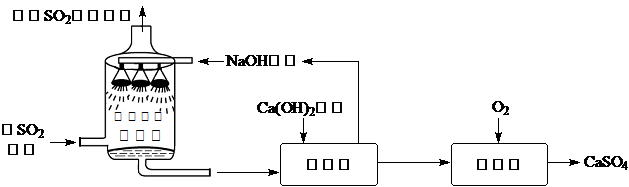
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com