
【題目】下列各組中兩個化學反應,屬于同一反應類型的一組是 ()
A.由苯制溴苯;由乙酸與乙醇制取乙酸乙酯
B.由乙烯制1,2-二溴乙烷;由乙烷制一氯乙烷
C.乙烯使溴水褪色;乙烯使酸性高錳酸鉀溶液褪色
D.由溴乙烷制取乙烯;由苯制取環己烷
科目:高中化學 來源: 題型:
【題目】已知2H2O2(1)=2H2O(1)+O2(g)反應過程中的能量變化曲線如圖所示,下列說法不正確的是

A. 該反應的△H<0,△S>0
B. 途徑Ⅱ與途徑I相比,可能是加了催化劑
C. 其他條件相同時,產生相同體積的氧氣時放出的熱量:途徑I >途徑Ⅱ
D. 其他條件相同時,產生相同體積的氧氣所需的時間:途徑I>途徑Ⅱ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化氯(ClO2)可用于自來水消毒。以粗鹽為原料生產ClO2的工藝主要包括:①粗鹽精制;②電解微酸性NaCl溶液;③ClO2的制取。工藝流程如下圖:

提供的試劑:飽和Na2CO3溶液、飽和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)粗食鹽水中含有Ca2+、Mg2+、SO![]() 等雜質。除雜操作時,往粗鹽水中先加入過量的試劑X,選出試劑X所代表的試劑,按滴加順序依次為是__________(填化學式),充分反應后將沉淀一并濾去。經檢測發現濾液中仍含有一定量的SO
等雜質。除雜操作時,往粗鹽水中先加入過量的試劑X,選出試劑X所代表的試劑,按滴加順序依次為是__________(填化學式),充分反應后將沉淀一并濾去。經檢測發現濾液中仍含有一定量的SO![]() ,其原因是__________________。
,其原因是__________________。
(已知:Ksp(BaSO4)=1.1×10-10 ;Ksp(BaCO3)=5.1×10-9)
(2)上述過程中,將食鹽水在特定條件下電解得到的氯酸鈉與鹽酸反應生成ClO2。電解時生成的氣體B是________;電解時陽極反應式為_________________。反應Ⅲ的化學方程式為___________________。
(3)ClO2很不穩定,需隨用隨制,產物用水吸收得到ClO2溶液。為測定所得溶液中ClO2的含量,進行了以下實驗:
步驟1:準確量取ClO2溶液10.00 mL,稀釋成100 mL試樣。
步驟2:量取V1mL試樣加入到錐形瓶中,調節試樣的pH≤2.0,加入足量的KI晶體,搖勻,在暗處靜置30分鐘。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步驟3:以淀粉溶液作指示劑,用c mol·L-1Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O![]() =2I-+S4O
=2I-+S4O![]() )
)
①準確量取10.00 mL ClO2溶液的玻璃儀器是_______________。
②上述步驟3中滴定終點的現象是______________。
③若實驗中使用的Na2S2O3標準溶液部分因被氧氣氧化而變質,則實驗結果________________(填“偏高”、“偏低”或“無影響”)
④根據上述步驟可計算出原ClO2溶液的濃度為 ________mol·L-1(用含字母的代數式表示)。
(4)“有效氯含量”可用來衡量含氯消毒劑的消毒能力,其定義是:每克含氯消毒劑的氧化能力相當于多少克Cl2的氧化能力。ClO2的有效氯含量為___。(計算結果保留兩位小數)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生活中處處有化學,下列有關說法正確的是( )
A.淀粉和纖維素均為天然高分子化合物
B.飲用礦泉水瓶的主要成分是聚氯乙烯
C.凡含有食品添加劑的食物均不可食用
D.大米煮成粥后,淀粉就變成了葡萄糖
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式碳酸銅可用于生產木材防腐劑等。工業上可用微蝕刻廢液(含有一定量Cu2+、H+、SO42-、H2O2和微量Fe3+)制備高純度堿式碳酸銅,其制備過程如下:
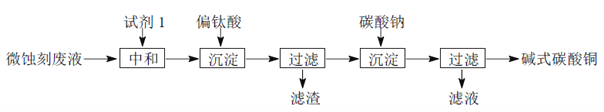
(1)試劑1最好選用________________。
a.Fe2O3 b.CaCO3 C.CuO
(2)加入Na2CO3沉淀前須除去Fe3+,否則Fe2(SO4)3會與Na2CO3反應,產生一種氣體,同時生成NaFe3(OH)6(SO4)2沉淀,影響產品質量,寫出該反應的化學方程式______________________。
(3)加入Na2CO3沉淀時,反應液pH對產品中SO42-的含量以及反應液中Cu2+沉淀效率的影響如下圖所示,第二次沉淀時溶液pH最好控制在___________________________。

(4)所制得的堿式碳酸銅的組成可表示為:xCuCO3·yCu(OH)2·zH2O,要測定其組成,甲同學設計的實驗方案中需要如下五個步驟:①稱取12.0克的樣品;②高溫分解;③測出生成CO2的質量為2.2克;④測出生成水蒸氣的質量為1.8克;⑤稱量生成CuO的質量為8.0克。而乙同學認為除步驟②外,實驗只需測定四個量中的部分數據即可,則合理的組合為______________(填序號,寫一組即可)。根據你的選擇,計算出堿式碳酸銅的組成,寫出計算過程。____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】物質中的雜質(括號內的物質)除去時,所使用的試劑和主要操作都正確的是( )
選項 | 物質 | 使用的試劑 | 主要操作 |
A | 乙醇(水) | 金屬鈉 | 過濾 |
B | 乙酸乙酯(乙酸) | 飽和碳酸鈉溶液 | 分液 |
C | 苯(苯酚) | 濃溴水 | 振蕩、分液 |
D | 乙烷(乙烯) | 酸性高錳酸鉀溶液 | 洗氣 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某氨肥樣品可能含有NH4HCO3、NH4Cl、.NH4NO3中的一種或幾種。稱取該樣品1.000克,溶于水配成100mL溶液,將溶液分成兩等份依次完成如下實驗:
①向一份溶液中加入10mL0.2 mol·L-1的鹽酸與之充分反應,可收集到標準狀況下的CO2氣體44.8mL(設產生的CO2全部逸出)。
②向另一份溶液中加入足量的6mol·L-1氫氧化鈉溶液,加熱,產生的氣體(設產生的NH3全部逸出)至少需要25mlL0.15 mol·L-1的硫酸才能被完全反應。下列說法正確的是
A. 1.000g樣品中一定含有NH4HCO30.316克
B. 向①反應所得的溶液中加入硝酸酸化的硝酸銀溶液,若有白色沉淀生成,說明原樣品中一定含有NH4Cl
C. 原樣品的含氨量為21%
D. 無需另外再設計實驗驗證,就能確定原樣品中是否含有NH4Cl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】選擇下列實驗方法分離物質,將分離方法的序號填在橫線上.
A.萃取 B.分液 C.過濾 D.加熱分解 E.蒸發 F.蒸餾
①把飽和食鹽水中的食鹽提取出來
②把碘水中的碘提取出來
③用海水制取蒸餾水
④除去氧化鈣中的碳酸鈣
⑤分離柴油和水的混合物 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com