
如圖所示的裝置中,M為金屬活動性順序表中位于氫之前的金屬,N為石墨棒,下列關于此裝置的敘述中不正確的是( )。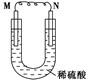
| A.N上有氣體放出 |
| B.M為負極,N為正極 |
| C.是化學能轉變?yōu)殡娔艿难b置 |
| D.導線中有電流通過,電流方向是由M到N |
 名校名師培優(yōu)作業(yè)本加核心試卷系列答案
名校名師培優(yōu)作業(yè)本加核心試卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化學 來源: 題型:單選題
下圖所示裝置I是一種可充電電池,裝置Ⅱ為電解池。離子交換膜只允許Na+通過,充放電的化學方程式為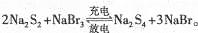 閉合開關K時,b極附近先變紅色。下列說法正確的是
閉合開關K時,b極附近先變紅色。下列說法正確的是
| A.當有0.01 mol Na+通過離子交換膜時,b電極上析出112 mL的氣體 |
| B.負極反應為3Br--2e-= Br3- |
| C.閉合K后,b電極附近的pH變小 |
| D.閉合K后.a電極上有氯氣產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
利用反應2Cu+O2+2H2SO4=2CuSO4+2H2O可制備CuSO4,若將該反應設計為原電池。
(1)負極材料是________(寫名稱),電極反應為__________________。
(2)正極電極反應式為__________________________________。
(3)溶液中SO42—向________極移動。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
電解裝置如圖所示,電解槽內裝有KI及淀粉溶液,中間用陰離子交換膜隔開。在一定的電壓下通電,發(fā)現左側溶液變藍色,一段時間后,藍色逐漸變淺。已知:3I2+6OH-=IO+5I-+3H2O,下列說法不正確的是( )
| A.右側發(fā)生的電極反應式:2H2O+2e-=H2↑+2OH- |
| B.電解結束時,右側溶液中含有IO3- |
C.電解槽內發(fā)生反應的總化學方程式:KI+3H2O KIO3+3H2↑ KIO3+3H2↑ |
| D.如果用陽離子交換膜代替陰離子交換膜,電解槽內發(fā)生的總化學反應不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
為研究金屬腐蝕的條件和速率,某課外小組學生用金屬絲將三根大小相同的鐵釘分別固定在圖示的三個裝置中,再放置于玻璃鐘罩里保存相同的一段時間。下列對實驗結束時現象的描述不正確的是 ( )。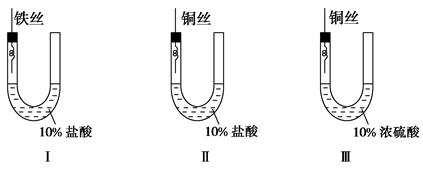
| A.裝置Ⅰ左側的液面一定會下降 |
| B.左側液面裝置Ⅰ比裝置Ⅱ的低 |
| C.裝置Ⅱ中的鐵釘腐蝕最嚴重 |
| D.裝置Ⅲ中的鐵釘幾乎沒被腐蝕 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
實驗室用鉛蓄電池作電源電解飽和食鹽水制取Cl2,已知鉛蓄電池放電時發(fā)生如下反應:
負極:Pb+SO42—-2e-=PbSO4
正極:PbO2+4H++SO42—+2e-=PbSO4+2H2O
今欲制得Cl2 0.050 mol, 這時電池內消耗的H2SO4的物質的量至少是( )。
| A.0.025 mol | B.0.050 mol | C.0.10 mol | D.0.20 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一種燃料電池中發(fā)生的化學反應為:在酸性溶液中甲醇與氧作用生成水和二氧化碳。該電池負極發(fā)生的反應是( )
| A.CH3OH(g)+O2(g)-2e-=H2O(l)+CO2(g)+2H+(aq) |
| B.O2(g)+4H+(aq)+4e-=2H2O(l) |
| C.CH3OH(g)+H2O(l)-6e-=CO2(g)+6H+(aq) |
| D.O2(g)+2H2O(l)+4e-=4OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
如圖是Zn和Cu形成的原電池,某實驗興趣小組做完實驗后,在讀書卡片上記錄如下,其中正確的是( )
①Zn為正極,Cu為負極;
②H+向負極移動;
③電子是由Zn經外電路流向Cu;
④Cu極上有H2產生;
⑤若有1 mol電子流過導線,則產生的H2為0.5 mol;
⑥正極的電極反應式為Zn-2e-=Zn2+
| A.①②③ | B.③④⑤ | C.④⑤⑥ | D.②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關原電池的說法中,正確的是( )
A.鋁片和鎂片用導線連接后插入NaOH溶液中,鎂片較活潑,作負極
B鋁片和銅片用導線連接后插入濃硝酸中,銅作負極
C.鍍鋅鐵和鍍錫鐵的鍍層破損后,前者較易被腐蝕
D.將反應2Fe3++Fe=3Fe2+設計為原電池,則可用鋅片作負極,鐵片作正極,FeCl3溶液作電解質
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com