
(17分)合成氨工業(yè)上常用下列方法制備H2:
方法:
方法:

試計(jì)算25℃時(shí)由方法②制備l000g H2所放出的能量為_________ kJ。
(2)在一定的條件下,將C(s)和H2O(g)分別加入甲、乙兩個密閉容器,發(fā)生反應(yīng):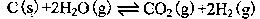 其相關(guān)數(shù)據(jù)如下表所示:
其相關(guān)數(shù)據(jù)如下表所示: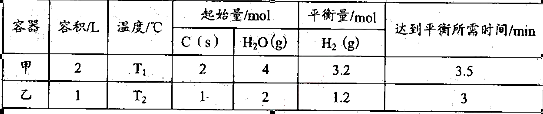
①T1_________T2(填“>”、“=”或“<”);
T1℃時(shí),該反應(yīng)的平衡常數(shù)K="_________" 。
②乙容器中,當(dāng)反應(yīng)進(jìn)行到1.5min時(shí),H2O(g)的物質(zhì)的量濃度范圍是_________。
③一定條件下,在密閉恒容的容器中,能表示上述反應(yīng)達(dá)到化學(xué)平衡狀態(tài)的是_________。
A.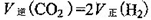
B.混合氣體的密度保持不變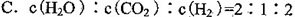
D.混合氣體的平均相對分子質(zhì)量保持不變
④某同學(xué)為了研究反應(yīng)條件對化學(xué)平衡的影響,測得逆反應(yīng)速率與時(shí)間的關(guān)系如圖所示: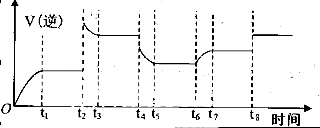
可見在t1、t3、t5、t7時(shí)反應(yīng)都達(dá)了到平衡狀態(tài),如果t2、t4、t6、t8時(shí)都只改變了一個反應(yīng)條件,則從t1到t8哪個時(shí)間段H2O (g)的平衡轉(zhuǎn)化率最低_________,t4時(shí)刻改變的條件是__________。
⑤在25 ℃時(shí),c mol/L,的醋酸與0.02mol/L NaOH溶液等體積混合后溶液剛好呈中性,
用含c的代數(shù)式表示CH3COOH的電離常數(shù)Ka=_________。
(17分)(1)20500kJ (2分)
(2)① > (2分) 12.8(2分)
② <1.4mol/L (2分)
③BD(選全得2分,漏選得1分,有錯選0分)
④t7-t8(或“t7到t8”)(2分) 降低溫度(2分)
⑤ 2×10-9/(c-0.02) (3分)
解析試題分析:(1)根據(jù)蓋斯定律得由方法②制取氫氣的熱化學(xué)方程式可由已知中的反應(yīng)得到,每生成1mol氫氣放出的熱量=①-②-③=(394-111-242)kJ=41kJ,1000g氫氣的物質(zhì)的量是500mol,所以制備l000g H2所放出的能量為500×41=20500kJ;
(2)①由表中數(shù)據(jù)可計(jì)算各物質(zhì)的平衡濃度,所以T1的化學(xué)平衡常數(shù)K1=1.62×0.8/0.42=12.8,同理可計(jì)算T2的平衡常數(shù)K2=1.35,因?yàn)樵摲磻?yīng)是吸熱反應(yīng),K1> K2,所以T1>T2
②反應(yīng)進(jìn)行到一半時(shí),若按反應(yīng)速率一直不變計(jì)算,1.5min時(shí)水蒸氣的濃度是2mol/L-0.6mol/L=1.4mol/L,但是反應(yīng)速率隨反應(yīng)的進(jìn)行逐漸減小,前一半的反應(yīng)速率大于后一半的反應(yīng)速率,所以消耗水蒸氣的濃度較大,則剩余水蒸氣的濃度應(yīng)小于1.4mol/L;
③A、平衡時(shí)氫氣的正反應(yīng)速率是二氧化碳逆反應(yīng)速率的2倍,錯誤;B、該反應(yīng)有固體參與,所以氣體的質(zhì)量一直在變,當(dāng)達(dá)到平衡時(shí)氣體的質(zhì)量不再變化,容器的體積一直不變,所以當(dāng)氣體的密度不變時(shí)證明已達(dá)平衡狀態(tài),正確;C、氣體的濃度之比符合化學(xué)計(jì)量數(shù)之比時(shí) 不能判斷平衡是否到達(dá),錯誤;D、混合氣體的質(zhì)量與氣體的物質(zhì)的量在未達(dá)平衡時(shí)一直在變,即氣體的平均相對分子質(zhì)量在變,平衡時(shí)混合氣體的質(zhì)量、物質(zhì)的量均固定,混合氣體的平均相對分子質(zhì)量不再變化,正確,答案選BD;
④H2O (g)的平衡轉(zhuǎn)化率最低,證明平衡一直逆向移動,t2~t4逆反應(yīng)速率陡然增大后減小至不變,說明改變的一個條件是增大壓強(qiáng),平衡逆向移動;t4~t6逆反應(yīng)速率陡然減小至不變,說明改變的條件是降低溫度,平衡逆向移動;t6~t7逆反應(yīng)速率先不變再逐漸增大至不變,說明改變的條件是又充入了水蒸氣,雖然平衡正向移動,但水蒸氣的轉(zhuǎn)化率降低了,所以水蒸氣的轉(zhuǎn)化率最低的是t7-t8;t4時(shí)刻改變的條件是降低溫度;
⑤混合溶液呈中性證明c(OH-)= c(H+)=1×10-7mol/L,根據(jù)電荷守恒得c(Na+)=c(CH3COO-)=0.01mol/L,因?yàn)榇姿徕c溶液呈堿性,現(xiàn)在溶液呈中性,說明醋酸過量,所以剩余醋酸的物質(zhì)的量濃度是(c-0.02)/2mol/L,則產(chǎn)生的電離平衡常數(shù)K= c(H+) c(CH3COO-)/ c(CH3COOH)= 2×10-9/(c-0.02)。
考點(diǎn):考查化學(xué)平衡狀態(tài)的判斷,轉(zhuǎn)化率的判斷,對圖像的分析,反應(yīng)熱效應(yīng)的計(jì)算,混合溶液的計(jì)算


 計(jì)算高手系列答案
計(jì)算高手系列答案
| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:填空題
(16分)化工工業(yè)中常用乙苯脫氫的方法制備苯乙烯。已知某溫度下:
反應(yīng)①:CO2(g)+H2(g) CO(g)+H2O(g),ΔH=" +41.2" kJ/mol;
CO(g)+H2O(g),ΔH=" +41.2" kJ/mol;
反應(yīng)②: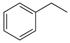 (g)
(g)
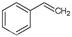 (g)+H2(g),ΔH=" +117.6" kJ/mol。
(g)+H2(g),ΔH=" +117.6" kJ/mol。
①、②的化學(xué)反應(yīng)平衡常數(shù)分別為K1、K2。
(1)請寫出二氧化碳氧化乙苯制備苯乙烯的熱化學(xué)反應(yīng)方程式 。該反應(yīng)的化學(xué)平衡常數(shù)K= (用K1、K2表示)。
(2)恒溫恒容條件下,反應(yīng)①達(dá)到平衡后,t1時(shí)刻通入少量CO2。請
畫出t1之后的正逆反應(yīng)曲線,并作出標(biāo)注。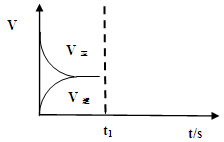
(3)已知某溫度下,Ag2SO4飽和溶液中c(Ag+)="0.04" mol/L,則該溫度
下Ksp(Ag2SO4)= 。(保留兩位有效數(shù)字)
(4)電解法制備高鐵酸鈉(Na2FeO4),總反應(yīng)式為:Fe+2H2O+2OH-=FeO42-+3H2↑,電解質(zhì)溶液選用NaOH溶液。該電解池陽極材料是 (寫化學(xué)式);陽極的電極反應(yīng)式為__ _________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(8分) 關(guān)于反應(yīng)熱請回答如下問題:
(1)向1L1mol/L的NaOH溶液中加入下列物質(zhì):①濃H2SO4;②稀硝酸;③稀醋酸,恰好完全反應(yīng)的熱效應(yīng)為△H1、△H2、△H3,則三者由小到大順序?yàn)?u> 。
(2) 實(shí)驗(yàn)測得,向200mL1mol/L的NaOH溶液中加入稀醋酸恰好反應(yīng)放出Q kJ的熱量,請寫出熱化學(xué)反應(yīng)方程式:_________________________ 。
(3)已知反應(yīng)CH3—CH3(g)―→CH2=CH2(g)+H2(g),有關(guān)化學(xué)鍵的鍵能如下。
| 化學(xué)鍵 | C—H | C=C | C—C | H—H |
| 鍵能/kJ·mol-1 | 414.4 | 615.3 | 347.4 | 435.3 |
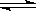 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(15分)氨是最重要的化工產(chǎn)品之一。
(1)合成氨用的氫氣可以甲烷為原料制得:CH4(g)+H2O(g)  CO(g)+3H2(g)。有關(guān)化學(xué)反應(yīng)的能量變化如下圖所示。CH4(g)與H2O(g)反應(yīng)生成CO(g)和H2(g)的熱化學(xué)方程式為 。
CO(g)+3H2(g)。有關(guān)化學(xué)反應(yīng)的能量變化如下圖所示。CH4(g)與H2O(g)反應(yīng)生成CO(g)和H2(g)的熱化學(xué)方程式為 。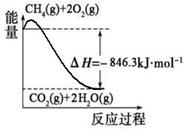
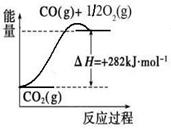

(2)CO對合成氨的催化劑有毒害作用,常用乙酸二氨合銅(Ⅰ)溶液來吸收原料氣中CO,其反應(yīng)原理為:[Cu(NH3)2CH3COO] (l)+CO(g)+NH3(g)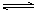 [Cu(NH3)3] CH3COO·CO(l) △H<0。吸收CO后的乙酸銅氨液經(jīng)過適當(dāng)處理后又可再生,恢復(fù)其吸收CO的能力以供循環(huán)使用,再生的適宜條件是 。
[Cu(NH3)3] CH3COO·CO(l) △H<0。吸收CO后的乙酸銅氨液經(jīng)過適當(dāng)處理后又可再生,恢復(fù)其吸收CO的能力以供循環(huán)使用,再生的適宜條件是 。
(填寫選項(xiàng)編號)
A.高溫、高壓 B.高溫、低壓 C.低溫、低壓 D.低溫、高壓
(3)用氨氣制取尿素[CO(NH2)2]的反應(yīng)為:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) △H<0
CO(NH2)2(l)+H2O(g) △H<0
某溫度下,向容積為100L的密閉容器中通入4mol NH3和2molCO2,該反應(yīng)進(jìn)行到40 s時(shí)達(dá)到平衡,此時(shí)CO2的轉(zhuǎn)化率為50%。該溫度下此反應(yīng)平衡常數(shù)K的值為_________。下圖中的曲線表示該反應(yīng)在前25 s內(nèi)的反應(yīng)進(jìn)程中的NH3濃度變化。若反應(yīng)延續(xù)至70s,保持其它條件不變情況下,請?jiān)趫D中用實(shí)線畫出使用催化劑時(shí)該反應(yīng)的進(jìn)程曲線。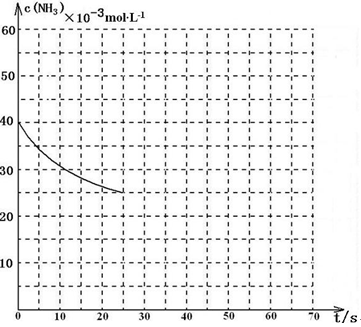
(4)將尿素施入土壤后,大部分是通過轉(zhuǎn)化為碳酸銨或碳酸氫銨后才被作物所利用,尿素分子在微生物分泌的脲酶作用下,轉(zhuǎn)化為碳酸銨。已知弱電解質(zhì)在水中的電離平衡常數(shù)(25℃)如下表:
| 弱電解質(zhì) | H2CO3 | NH3·H2O |
| 電離平衡常數(shù) | Ka1=4.30×10-7 Ka2=5.61×10-11 | 1.77×10-5 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(14分)運(yùn)用化學(xué)反應(yīng)原理分析解答以下問題
(1)已知: ①CO(g)+2H2(g)  CH3OH(g) △Hl= -91kJ·mol-l
CH3OH(g) △Hl= -91kJ·mol-l
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2= -24 kJ·mol-l ③CO(g) +H2O(g)
CH3OCH3(g)+H2O(g) △H2= -24 kJ·mol-l ③CO(g) +H2O(g)  CO2(g)+H2(g) △H3= -41 kJ·mol-l
CO2(g)+H2(g) △H3= -41 kJ·mol-l
且三個反應(yīng)的平衡常數(shù)依次為K1、K2、K3 則反應(yīng) 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) △H= .
則反應(yīng) 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) △H= .
化學(xué)平衡常數(shù)K= (用含K1、K2、K3的代數(shù)式表示)。
(2)一定條件下,若將體積比為1:2的CO和H2氣體通入體積一定的密閉容器中發(fā)生反應(yīng) 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g),下列能說明反應(yīng)達(dá)到平衡狀態(tài)是 。
3CO(g) +3H2(g) CH3OCH3(g) +CO2(g),下列能說明反應(yīng)達(dá)到平衡狀態(tài)是 。
a.體系壓強(qiáng)保持不變 B.混合氣體密度保持不變
c. CO和H2的物質(zhì)的量保持不變 d.CO的消耗速度等于CO2的生成速率
(3)氨氣溶于水得到氨水。在25℃下,將x mol.L-l的氨水與y mol.L-1的鹽酸等體積混合,反應(yīng)后溶液顯中性,則c(NH4+)____c(Cl-)(填“>”、“<”、“=”);用含x和y的代數(shù)式表示出氨水的電離平衡常數(shù) .
(4)科學(xué)家發(fā)明了使NH3直接用于燃料電池的方法,其裝置用鉑黑作電極、加入電解質(zhì)溶液中,一個電極通入空氣,另一電極通入NH3。其電池反應(yīng)式為:4NH3+3O2 = 2N2+6H2O,電解質(zhì)溶液應(yīng)顯 (填“酸性”、“中性”、“堿性”),
寫出正極的電極反應(yīng)方程式 .
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
丙烷在燃燒時(shí)能放出大量的熱,它也是液化石油氣的主要成分,作為能源應(yīng)用于人們的日常生產(chǎn)和生活。已知:
①2C3H8(g)+7O2(g) =6CO(g)+8H2O(g) △H =-2389.8 kJ/mol
②2CO(g) + O2(g) =2CO2(g) △H =-566 kJ/mol
③H2O(l) = H2O(g) △H ="+" 44.0 kJ/mol
(1)寫出C3H8燃燒時(shí)燃燒熱的熱化學(xué)方程式 。
(2)C3H8在不足量的氧氣里燃燒,生成CO、CO2、H2O(g),將所有的產(chǎn)物通入一個體積固定的密閉容器中,在一定條件下發(fā)生如下可逆反應(yīng):CO(g) +H2O(g)  CO2(g) +H2(g)該反應(yīng)的平衡常數(shù)與溫度的關(guān)系如下表:
CO2(g) +H2(g)該反應(yīng)的平衡常數(shù)與溫度的關(guān)系如下表:
| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數(shù)K | 9.94 | 9 | 1 |
| | H2O | CO | CO2 | H2 |
| 甲 (質(zhì)量/g) | 1.8 | 8.4 | a | 1 |
| 乙 (質(zhì)量/g) | 1.8 | 2.8 | 0 | 0 |

查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(14分)2013年10月我市因臺風(fēng)菲特遭受到重大損失,市疾控中心緊急采購消毒藥品,以滿足災(zāi)后需要。復(fù)方過氧化氫消毒劑具有高效、環(huán)保、無刺激無殘留,其主要成分H2O2是一種無色粘稠液體,請回答下列問題:
⑴火箭發(fā)射常以液態(tài)肼(N2H4)為燃料,液態(tài)H2O2為助燃劑。已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g) △H="-" 534 kJ·mol-1 ①
H2O2(1)=H2O(1)+1/2O2(g) △H="-" 98.64 kJ·mol-1 ②
H2O(1)=H2O(g) △H=+44kJ·mol-l ③
則反應(yīng)N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)的△H= ,
⑵據(jù)報(bào)道,以硼氫化合物NaBH4(B元素的化合價(jià)為+3價(jià))和H2O2作 原料的燃 料電池,負(fù)極材料采用Pt/C,正極材料采用MnO2,可用作空軍通信衛(wèi)星電,其工作原理如圖所示。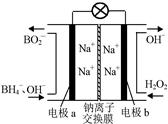
則該電池的正極反應(yīng)____ ___
⑶H2O2是一種不穩(wěn)定易分解的物質(zhì)。右圖是H2O2在沒有催化劑時(shí)反應(yīng)進(jìn)程與能量變化圖,請?jiān)趫D上畫出使用催化劑加快分解速率時(shí)能量與進(jìn)程圖 。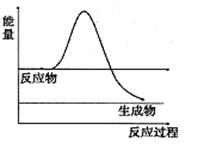
⑷某化學(xué)興趣小組欲測定H2O2的分解速率,取溶液0.5L進(jìn)行分析,數(shù)據(jù)如表格所示:
| t(S) | 0 | 2 | 4 | 6 | 8 | 10 |
| n(H2O2) (moL) | 0.8 | 0.7 | 0.62 | 0.55 | 0.27 | 0.03 |

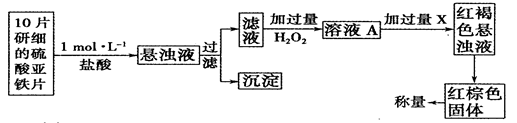
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
大氣中的部分碘源于O3對海水中I-的氧化。將O3持續(xù)通入NaI溶液中進(jìn)行模擬研究.
(1)O3將I-氧化成I2的過程由3步反應(yīng)組成:
①I-(aq)+ O3(g)= IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq)  HOI(aq) △H2
HOI(aq) △H2
③HOI(aq) + I-(aq) + H+(aq) I2(aq) + H2O(l) △H3
I2(aq) + H2O(l) △H3
總反應(yīng)的化學(xué)方程式為__ ____,其反應(yīng)△H=___ ___
(2)在溶液中存在化學(xué)平衡:I2(aq) + I-(aq)  I3-(aq),其平衡常數(shù)表達(dá)式為_______.
I3-(aq),其平衡常數(shù)表達(dá)式為_______.
(3)為探究Fe2+ 對O3氧化I-反應(yīng)的影響(反應(yīng)體如左圖),某研究小組測定兩組實(shí)驗(yàn)中I3-濃度和體系pH,結(jié)果見右圖和下表。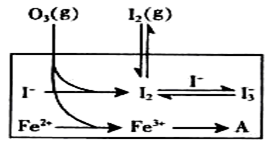
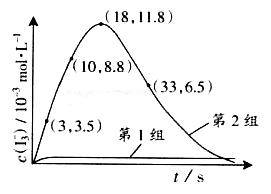
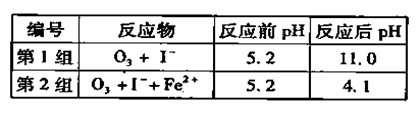
①第1組實(shí)驗(yàn)中,導(dǎo)致反應(yīng)后pH升高的原因是_______。
②圖13中的A為__ ___,由Fe3+生成A的過程能顯著提高Ⅰ-的轉(zhuǎn)化率,原因是 。
③第2組實(shí)驗(yàn)進(jìn)行18s后,I3-濃度下降。導(dǎo)致下降的直接原因有(雙選)______。
| A.c(H+)減小 | B.c(I-)減小 | C.I2(g)不斷生成 | D.c(Fe3+)增加 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
I.“低碳循環(huán)”引起各國的高度重視,而如何降低大氣中CO2的含量及有效地開發(fā)利用CO2,引起了全世界的普遍重視。所以“低碳經(jīng)濟(jì)”正成為科學(xué)家研究的主要課題:
(1)將不同量的CO(g)和H2O(g)分別通入到體積為2L的恒容密閉容器中,進(jìn)行反應(yīng):
CO(g)+H2O(g) CO2(g)+H2(g),得到如下二組數(shù)據(jù):
CO2(g)+H2(g),得到如下二組數(shù)據(jù):
| 實(shí)驗(yàn)組 | 溫度℃ | 起始量/mol | 平衡量/mol | 達(dá)到平衡所需時(shí)間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺 | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com