
����еIJ��ֵ�Դ��O3��(du��)��ˮ��I������������O3���m(x��)ͨ��NaI������Һ��Һ���M(j��n)��ģ�M�о���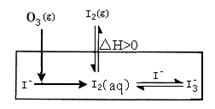
��1��O3��I��������I2���^�̿ɰl(f��)�����·���(y��ng)��
��I����aq��+ O3��g��= IO��(aq) +O2��g����H1
��IO����aq��+H+(aq)  HOI(aq) ����H2
HOI(aq) ����H2
��HOI(aq) + I��(aq) + H+(aq) I2(aq) + H2O(l) ��H3
I2(aq) + H2O(l) ��H3
��O3��g��+2I����aq��+2H+��aq��=��I2(aq) + O2��g��+ H2O(l) ��H4
�t��H3�c��H1����H2����H4֮�g���P(gu��n)ϵ�ǣ���H3 = ��
��2������Һ�д��ڻ��W(xu��)ƽ�⣺ I2(aq) + I��(aq)  I3��(aq)��ƽ�ⳣ��(sh��)���_(d��)ʽ�� ���ڷ���(y��ng)������(g��)�^����I3�����|(zh��)�������׃����r�� ��
I3��(aq)��ƽ�ⳣ��(sh��)���_(d��)ʽ�� ���ڷ���(y��ng)������(g��)�^����I3�����|(zh��)�������׃����r�� ��
��3����̽���ض���(du��)I2(aq) + I��(aq) I3��(aq) ��H5 ����(y��ng)��Ӱ푡���ij�ض�T1�£���һ������0.2 mol��L-1NaI������Һ�������]�����У�������һ������O3��g����O3���w���㣬�����]������O2�c I������(y��ng)������t�r(sh��)�̣��y(c��)��������I2��g���ĝ�ȡ�Ȼ��քe�ڜضȞ�T2��T3��T4��T5�£�����������ʼ��(sh��)�(y��n)�l����׃���؏�(f��)������(sh��)�(y��n)����(j��ng)�^��ͬ�r(sh��)�g�y(c��)��I2��g����ȣ��õ�څ��(sh��)�D��Ҋ�Dһ�����t��
I3��(aq) ��H5 ����(y��ng)��Ӱ푡���ij�ض�T1�£���һ������0.2 mol��L-1NaI������Һ�������]�����У�������һ������O3��g����O3���w���㣬�����]������O2�c I������(y��ng)������t�r(sh��)�̣��y(c��)��������I2��g���ĝ�ȡ�Ȼ��քe�ڜضȞ�T2��T3��T4��T5�£�����������ʼ��(sh��)�(y��n)�l����׃���؏�(f��)������(sh��)�(y��n)����(j��ng)�^��ͬ�r(sh��)�g�y(c��)��I2��g����ȣ��õ�څ��(sh��)�D��Ҋ�Dһ�����t��
������T3�r(sh��)�������ПoO3�� T4��T5�ضȅ^(q��)�g������(n��i)I2��g����ȳʬF(xi��n)��Dһ��ʾ��׃��څ��(sh��)���t��H5 0(�������)��ԓ�l�����ڜضȞ�T4�r(sh��)����Һ��I������S�r(sh��)�g׃����څ��(sh��)������D����ʾ����t2�r(sh��)����ԓ����(y��ng)�wϵ�ض�������T5�����S��ԓ�ضȡ�Ո(q��ng)?ji��n)ڈD2�Ю���t2�r(sh��)�̺���Һ�� I�����׃����څ��(sh��)������
������T3�r(sh��)��������߀��O3���tT1��T2�ضȅ^(q��)�g������(n��i)I2��g����ȳʬF(xi��n)��Dһ��ʾ��׃��څ��(sh��)������ܵ�ԭ���� �����Ό�һ�c(di��n)��
��4�����÷���(y��ng)�͈ܺD2����Ϣ��Ӌ(j��)��0-t1�r(sh��)�g��(n��i)��I2(aq)��ʾ�Ļ��W(xu��)����(y��ng)���� ��
��1����H4-��H2-��H1�� ��2�� ; �����Ӻ�pС��
; �����Ӻ�pС��
��3���٣� ��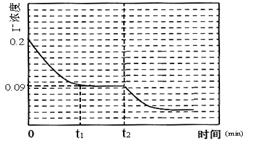
��O3�^�m(x��)����I-ʹ��Һ��I2������ӣ�ʹI2(aq)  I2(g)ƽ�����������Ƅ�(d��ng)�����wI2������ӣ���Һ�ض����ߣ�ʹI2(aq)
I2(g)ƽ�����������Ƅ�(d��ng)�����wI2������ӣ���Һ�ض����ߣ�ʹI2(aq)  I2(g)��H>0��ƽ�����������Ƅ�(d��ng)�����wI2������ӣ����ɗl�����Ό�һ�c(di��n)�o2�֣�
I2(g)��H>0��ƽ�����������Ƅ�(d��ng)�����wI2������ӣ����ɗl�����Ό�һ�c(di��n)�o2�֣�
(4)0.11/2t1 mol��L-1��min-1��2�֣�
����ԇ�}��������1���^����֪��4��(g��)�ữ�W(xu��)����ʽ�еķ���(y��ng)������������֪�����ɢ�ʽ�p��ʽ�p��ʽ�����ɵõ���ʽ�����ԣ���H3= ��H4����H2����H1��
��2������(j��)ƽ�ⳣ��(sh��)�Ķ��x�ɵ÷���(y��ng)I2(aq) + I��(aq) I3��(aq)��ƽ�ⳣ��(sh��)���_(d��)ʽ�飺
I3��(aq)��ƽ�ⳣ��(sh��)���_(d��)ʽ�飺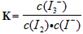 ����֪O3��I��������I2���^���пɰl(f��)��4��(g��)����(y��ng)�������ڷ���(y��ng)������(g��)�^����I3�����|(zh��)�������׃����r�ǣ��_ʼ�r(sh��)�S��O3��ͨ�룬O3���Ԍ�I��������I2��I2�cI���Y(ji��)���γ�I3�����Ķ�ʹI3�����|(zh��)���������������O3���ИO��(qi��ng)�����ԣ�ͨ���O3߀���Ԍ�I��������IO�������⣬�S��O3�ij��m(x��)ͨ�룬O3��һ����I��������IO�������⣬ʹI������������ͬ�r(sh��)I2�������p�٣��Ķ�ʹI3���ĝ��׃С��
����֪O3��I��������I2���^���пɰl(f��)��4��(g��)����(y��ng)�������ڷ���(y��ng)������(g��)�^����I3�����|(zh��)�������׃����r�ǣ��_ʼ�r(sh��)�S��O3��ͨ�룬O3���Ԍ�I��������I2��I2�cI���Y(ji��)���γ�I3�����Ķ�ʹI3�����|(zh��)���������������O3���ИO��(qi��ng)�����ԣ�ͨ���O3߀���Ԍ�I��������IO�������⣬�S��O3�ij��m(x��)ͨ�룬O3��һ����I��������IO�������⣬ʹI������������ͬ�r(sh��)I2�������p�٣��Ķ�ʹI3���ĝ��׃С��
��3������T3�r(sh��)���������џoO3�����ԏĈDʾ����֪�����˕r(sh��)����Һ��ֻ���ڃɂ�(g��)ƽ�⣺I2��ag) I2��g)����I2(aq) + I��(aq)
I2��g)����I2(aq) + I��(aq) I3��(aq) ������(j��)I2��ag)
I3��(aq) ������(j��)I2��ag) I2��g)��H>0�����ߜضȣ�I2��ag)�A��������I2��g)�������ڲ����]�������ؕr(sh��)��I2(g)��ȕ�(hu��)���ӣ����ǏĈDһT4��T5��ʾ��I2(g)���׃������������(sh��)�H�����ߜض�I2��g)��Ȝp�٣���ôֻ���Д��ǜض�������ʹƽ��I2(aq) + I��(aq)
I2��g)��H>0�����ߜضȣ�I2��ag)�A��������I2��g)�������ڲ����]�������ؕr(sh��)��I2(g)��ȕ�(hu��)���ӣ����ǏĈDһT4��T5��ʾ��I2(g)���׃������������(sh��)�H�����ߜض�I2��g)��Ȝp�٣���ôֻ���Д��ǜض�������ʹƽ��I2(aq) + I��(aq) I3��(aq) �����Ƅ�(d��ng)���Ƅ�(d��ng)�Y(ji��)��ʹI2(aq)��ȜpС���Ķ���(d��o)��I2��ag)
I3��(aq) �����Ƅ�(d��ng)���Ƅ�(d��ng)�Y(ji��)��ʹI2(aq)��ȜpС���Ķ���(d��o)��I2��ag) I2��g)ƽ�������Ƅ�(d��ng)��ʹI2(g)��ȜpС���ɴ˿����Д��H5��0��I2(aq) + I��(aq)
I2��g)ƽ�������Ƅ�(d��ng)��ʹI2(g)��ȜpС���ɴ˿����Д��H5��0��I2(aq) + I��(aq) I3��(aq)�����ᷴ��(y��ng)��
I3��(aq)�����ᷴ��(y��ng)��
Ҫ����t2�r(sh��)�̺���Һ�� I�����׃����څ��(sh��)������������ȴ_�����������c(di��n)����
�c(di��n)�ͽK�c(di��n)����֪�D����ʾ�������ǜض���T4�r(sh��)����Һ��I������S�r(sh��)�g׃����څ��(sh��)��������������������֪����(y��ng)���_(d��)��ƽ�⣬��t2�r(sh��)������(y��ng)�wϵ�ض�������T5�����S��ԓ�ضȣ��Ǹ�׃�ķ���(y��ng)�l�������ߜضȣ����˕r(sh��)ƽ���Ȼ��(hu��)�l(f��)���Ƅ�(d��ng)������T5�ض������������c(di��n)����T4�ض��������ĽK�c(di��n)������(bi��o)λ�Ñ�(y��ng)�飨0.09��t2�����������ߜضȼӿ췴��(y��ng)���ʣ��s���_(d��)��ƽ��ĕr(sh��)�g��������T5�ض��£��_(d��)��ƽ�����õĕr(sh��)�gҪ��T4�ض����٣����Թ��c(di��n)���F(xi��n)����r(sh��)�g��T4�ض����١�����ԓ����(y��ng)�����ᷴ��(y��ng)�����ߜض���ʹƽ��I2(aq) + I��(aq) I3��(aq)�����Ƅ�(d��ng)���Ķ�ʹI����ȜpС���Y(ji��)�ψD���еĔ�(sh��)��(j��)��֪��T4�ض���I���D(zhu��n)����Ȟ�0.11mol/L���D(zhu��n)���ʞ�
I3��(aq)�����Ƅ�(d��ng)���Ķ�ʹI����ȜpС���Y(ji��)�ψD���еĔ�(sh��)��(j��)��֪��T4�ض���I���D(zhu��n)����Ȟ�0.11mol/L���D(zhu��n)���ʞ� ����T5�ض���I�����D(zhu��n)���ʞ�һ������55%��I����ƽ����ҪС��0.09mol/L��(0.09mol/L��55%)��0.04mol/L�����Թ��c(di��n)��ƽ���c(di��n)����λ������(bi��o)��(y��ng)��I�����С��0.04mol/L̎���K�c(di��n)�c���c(di��n)��ƽ���c(di��n)����һ�lֱ���ϡ��ɴ˾Ϳɮ���t2�r(sh��)�̺���Һ�� I�����׃����څ��(sh��)������Ҋ�𰸣���
����T5�ض���I�����D(zhu��n)���ʞ�һ������55%��I����ƽ����ҪС��0.09mol/L��(0.09mol/L��55%)��0.04mol/L�����Թ��c(di��n)��ƽ���c(di��n)����λ������(bi��o)��(y��ng)��I�����С��0.04mol/L̎���K�c(di��n)�c���c(di��n)��ƽ���c(di��n)����һ�lֱ���ϡ��ɴ˾Ϳɮ���t2�r(sh��)�̺���Һ�� I�����׃����څ��(sh��)������Ҋ�𰸣���
����T3�r(sh��)��������߀��O3���tT1��T2�ضȅ^(q��)�g������(n��i)I2��g����ȳʬF(xi��n)��Dһ��ʾ��׃��څ��(sh��)�������ǣ�a.����������߀��O3��O3�^�m(x��)����I-ʹ��Һ��I2������ӣ��Ķ�ʹI2(aq)  I2(g)ƽ�����������Ƅ�(d��ng)�����wI2������ӣ�b.�wϵ�Ĝض����ߣ�ʹI2(aq)
I2(g)ƽ�����������Ƅ�(d��ng)�����wI2������ӣ�b.�wϵ�Ĝض����ߣ�ʹI2(aq)  I2(g)��H>0��ƽ�����������Ƅ�(d��ng)���Ķ����wI2������ӡ�
I2(g)��H>0��ƽ�����������Ƅ�(d��ng)���Ķ����wI2������ӡ�
��4������(j��)�D����ʾI����ȵĔ�(sh��)��(j��)��Ӌ(j��)�����I��(aq)��ʾ�Ļ��W(xu��)����(y��ng)���ʣ�
V(I��) = 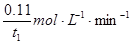 ���ٸ���(j��)��1���з���(y��ng)�ܵĻ��W(xu��)����ʽ��I��(aq)�cI2(aq)�Ļ��W(xu��)Ӌ(j��)����(sh��)֮��2 : 1���ó���I2(aq)��ʾ�Ļ��W(xu��)����(y��ng)���ʣ�V (I2) =
���ٸ���(j��)��1���з���(y��ng)�ܵĻ��W(xu��)����ʽ��I��(aq)�cI2(aq)�Ļ��W(xu��)Ӌ(j��)����(sh��)֮��2 : 1���ó���I2(aq)��ʾ�Ļ��W(xu��)����(y��ng)���ʣ�V (I2) =  ��
��
���c(di��n)�����W(xu��)����(y��ng)�c���������W(xu��)����(y��ng)���ʡ����W(xu��)ƽ��


 53�S�Üy(c��)ϵ�д�
53�S�Üy(c��)ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
2012��11��16�գ�5���к����l(f��)�F(xi��n)�����F��ʡ����(ji��)�������P(gu��n)�^(q��)���^�������(n��i)����(j��ng)��(d��ng)?sh��)ع������T�����{(di��o)�飬5���к��������������(n��i)����ȡů��(d��o)��CO�ж���������
(1)CO�ж�������CO�cѪҺ��Ѫ�t����Ѫ�t�ز��ַ���(y��ng)����̼��Ѫ�t���ף�����(y��ng)�Ļ��W(xu��)����ʽ�ɱ�ʾ��CO��HbO2 O2��HbCO����(sh��)�(y��n)������c(HbCO)��ʹֻ��c(HbO2)��
O2��HbCO����(sh��)�(y��n)������c(HbCO)��ʹֻ��c(HbO2)��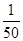 ��Ҳ������˵������p������֪t ��r(sh��)��������(y��ng)��ƽ�ⳣ��(sh��)K��200������β�O2�ĝ�ȼs��1.0��10��2 mol��L��1����ʹc(HbCO)С��c(HbO2)��
��Ҳ������˵������p������֪t ��r(sh��)��������(y��ng)��ƽ�ⳣ��(sh��)K��200������β�O2�ĝ�ȼs��1.0��10��2 mol��L��1����ʹc(HbCO)С��c(HbO2)��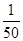 ���t����β�CO�ĝ�Ȳ��ܳ��^______mol��L��1��
���t����β�CO�ĝ�Ȳ��ܳ��^______mol��L��1��
(2)����������(g��)�cCO���P(gu��n)�ķ���(y��ng)��
Fe(s)��CO2(g) FeO(s)��CO(g)����H��Q1��ƽ�ⳣ��(sh��)K1
FeO(s)��CO(g)����H��Q1��ƽ�ⳣ��(sh��)K1
Fe(s)��H2O(g) FeO(s)��H2(g)����H��Q2��ƽ�ⳣ��(sh��)��K2
FeO(s)��H2(g)����H��Q2��ƽ�ⳣ��(sh��)��K2
H2(g)��CO2(g) CO(g)��H2O(g)����H��Q3��ƽ�ⳣ��(sh��)��K3
CO(g)��H2O(g)����H��Q3��ƽ�ⳣ��(sh��)��K3
�ڲ�ͬ�Ĝض���K1��K2��K3�Ĕ�(sh��)ֵ���£�
| T/�� | K1 | K2 | K3 |
| 700 | 1.47 | 2.38 | 0.62 |
| 900 | 2.15 | 1.67 | |
 CO(g)��H2O(g)��________(��š�������)�ᷴ��(y��ng)��Q3________0(�����������������)���۸�׃�l��ʹ���淴��(y��ng)H2(g)��CO2(g)
CO(g)��H2O(g)��________(��š�������)�ᷴ��(y��ng)��Q3________0(�����������������)���۸�׃�l��ʹ���淴��(y��ng)H2(g)��CO2(g) CO(g)��H2O(g)�ѽ�(j��ng)������ƽ�������Ƅ�(d��ng)���ɲ�ȡ�Ĵ�ʩ��________��
CO(g)��H2O(g)�ѽ�(j��ng)������ƽ�������Ƅ�(d��ng)���ɲ�ȡ�Ĵ�ʩ��________���鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
������(CH3OCH3)��һ�N��Ҫ���坍ȼ�Ϛ⣬�䃦(ch��)�\(y��n)��ȼ����ȫ�ԡ���Փȼ���ضȵ�����ָ��(bi��o)����(y��u)��Һ��ʯ�͚⣬Ҳ������ȼ��늳ص�ȼ�ϣ����кܺõĺ�չǰ����
��1����֪H2��CO��CH3OCH3��ȼ����(��H)�քe��-285.5kJ/mol��-283kJ/mol��-1460.0 kJ/mol���t���I(y��)������ˮú��ɷְ�1:1�ϳɶ����ѵğữ�W(xu��)����ʽ�� ��
��2�����I(y��)�ϲ���늸��h(yu��n)���۷�̎����ˮ�r(sh��)��������ˮ��pH��5.0��ͨ�^늽�����Fe(OH)3�z�w�������������s�|(zh��)��ͬ�r(sh��)����ꎘO�a(ch��n)����H2�����Ҹ����ˮ�棬���ڳ�ȥ����(sh��)�(y��n)���Զ�����ȼ��늳�ģ�Mԓ�����O(sh��)Ӌ(j��)���b�����D��ʾ��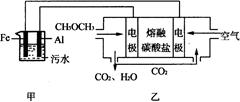
�����b��������̼���}��늽��|(zh��)��ϡ�����ٲ��Ϟ�늘O������ԓȼ��늳ص����O늘O����(y��ng)ʽ ���������|(zh��)������늳�����̼���}���� ��
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)2CO3
�ڌ������b����ꖘO�a(ch��n)���x������Fe(OH)3�������x�ӷ���ʽ�� ��
����֪������Kap[Fe(OH)3]=4.0��10��38��늽�һ�Εr(sh��)�g���b����c(Fe3+)= ��
����֪��H2S����xƽ�ⳣ��(sh��)��K1=9.1��10��8��K2=1.1��10��12��H2CO3����xƽ�ⳣ��(sh��)��K1=4.31��10��7��K2=5.61��10��11���y(c��)��늘O���D(zhu��n)����Ӟ�0.24mol�r(sh��)�������b�������ɵ�CO2ͨ��200mL 0.2mol/L��Na2S��Һ�У����и��(xi��ng)���_����
A���l(f��)������(y��ng)���x�ӷ���ʽ�飺CO2+S2��+H2O=CO32��+H2S
B���l(f��)������(y��ng)���x�ӷ���ʽ�飺CO2+S2��+H2O=HCO3��+HS��
C��c(Na+)=2[c(H2S)+c(HS��)+c(S2��)]
D��c(Na+)+c(H+)=2c(CO32��)+2c(S2��)+c(OH��)
E��c(Na+)>c(HCO3��)>c(HS��)>c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
����еIJ��ֵ�Դ��O3��(du��)��ˮ��I������������O3���m(x��)ͨ��NaI��Һ���M(j��n)��ģ�M�о���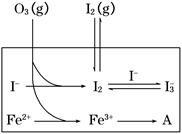
(1)O3��I��������I2���^����3������(y��ng)�M�ɣ�
��I��(aq)�� O3(g)===IO��(aq)��O2(g)����H1
��IO��(aq)��H��(aq) HOI(aq)����H2
HOI(aq)����H2
��HOI(aq)��I(xi��n)��(aq)��H��(aq) I2(aq)��H2O(l)����H3
I2(aq)��H2O(l)����H3
������(y��ng)�Ļ��W(xu��)����ʽ��_________________________________���䷴��(y��ng)�ᦤH��________��
(2)����Һ�д��ڻ��W(xu��)ƽ�⣺I2(aq)��I(xi��n)��(aq) I3��(aq)����ƽ�ⳣ��(sh��)���_(d��)ʽ��________��
I3��(aq)����ƽ�ⳣ��(sh��)���_(d��)ʽ��________��
(3) ��̽��Fe2����(du��)O3����I������(y��ng)��Ӱ�(����(y��ng)�wϵ���ψD)��ij�о�С�M�y(c��)���ɽM��(sh��)�(y��n)��I3����Ⱥ��wϵpH���Y(ji��)��Ҋ�D���±���
| ��̖(h��o) | ����(y��ng)�� | ����(y��ng)ǰpH | ����(y��ng)��pH |
| ��1�M | O3��I(xi��n)�� | 5.2 | 11.0 |
| ��2�M | O3��I(xi��n)����Fe2�� | 5.2 | 4.1 |
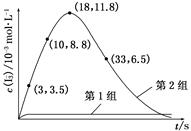
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�挦(du��)Ŀǰ���緶����(n��i)����ԴΣ�C(j��)���״�����һ�N�^�õĿ�������Դ�����ЏV���đ�(y��ng)��ǰ����
��1����֪�ڳ��س����·���(y��ng)�ğữ�W(xu��)����ʽ��
��CO��g����2H2��g��  CH3OH��g������H1����90 kJ��mol��1
CH3OH��g������H1����90 kJ��mol��1
��CO��g����H2O��g��  CO2��g����H2��g����H2����41 kJ��mol��1
CO2��g����H2��g����H2����41 kJ��mol��1
�����ɶ�����̼������Ƃ�״��ğữ�W(xu��)����ʽ��_______________________��
��2�����ݷe��V L�������г���a mol CO�c2a mol H2���ڴ��������·���(y��ng)���ɼ״���ƽ��r(sh��)���D(zhu��n)�����c�ضȡ�����(qi��ng)���P(gu��n)ϵ��D��ʾ��
��p1________p2������ڡ�����С�ڡ����ڡ�����
���������l����׃����r�£�������a mol CO�c2a mol H2���_(d��)����ƽ��r(sh��)��CO���D(zhu��n)����________����������pС����׃������ͬ����ƽ�ⳣ��(sh��)________��
��3����֪��T ��r(sh��)��CO��g����H2O��g��??CO2��g����H2��g����ƽ�ⳣ��(sh��)K��0.32����ԓ�ض��£���֪cʼ��CO����1 mol��L��1��cʼ��H2O����1 mol��L��1��ij�r(sh��)�̽�(j��ng)�y(c��)��CO���D(zhu��n)���ʞ�10%���tԓ����(y��ng)________����ѽ�(j��ng)���]�С����_(d��)��ƽ�⣬ԭ����___________________________________________���˕r(sh��)��v��________v�����>����<������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
̼���仯�����ЏV������;��
(1)��ˮ����ͨ�^�t���̼���ɮa(ch��n)��ˮú�⡣����(y��ng)��
C(s)��H2O(g) CO(g)��H2(g)����H����131.3 kJ��mol��1��
CO(g)��H2(g)����H����131.3 kJ��mol��1��
���Ϸ���(y��ng)�_(d��)��ƽ������w�e��׃�ėl���£����´�ʩ���������H2O��ƽ���D(zhu��n)���ʵ���________��(����̖(h��o))
| A�����ߜض� | B������̼������ | C��������� | D����CO���Մ���ȥCO |
 2CO(g)����H����172.5 kJ��mol��1���tCO(g)��H2O(g)
2CO(g)����H����172.5 kJ��mol��1���tCO(g)��H2O(g) CO2(g)��H2(g)����׃?ch��)�H��________��
CO2(g)��H2(g)����׃?ch��)�H��________�� CH3OH(g)���״���һ�Nȼ�ϣ������ü״��O(sh��)Ӌ(j��)һ��(g��)ȼ��늳أ���ϡ������늽��|(zh��)��Һ�����ʯī��늘O��ԓ늳�ؓ(f��)�O����(y��ng)ʽ��__________________________________��
CH3OH(g)���״���һ�Nȼ�ϣ������ü״��O(sh��)Ӌ(j��)һ��(g��)ȼ��늳أ���ϡ������늽��|(zh��)��Һ�����ʯī��늘O��ԓ늳�ؓ(f��)�O����(y��ng)ʽ��__________________________________�� CO2(g)��H2(g)���õ�����(sh��)��(j��)��
CO2(g)��H2(g)���õ�����(sh��)��(j��)��| �ض�/�� | ��ʼ��/mol | ƽ����/mol | �_(d��)��ƽ������r(sh��)�g/min | ||
| H2O | CO | H2 | CO | | |
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
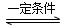 2NH3(g)����H����92.4 kJ��mol��1����(sh��)�(y��n)��ģ�M�������a(ch��n)���քe�ڲ�ͬ��(sh��)�(y��n)�l���·���(y��ng)��N2����S�r(sh��)�g׃����D����ʾ��
2NH3(g)����H����92.4 kJ��mol��1����(sh��)�(y��n)��ģ�M�������a(ch��n)���քe�ڲ�ͬ��(sh��)�(y��n)�l���·���(y��ng)��N2����S�r(sh��)�g׃����D����ʾ��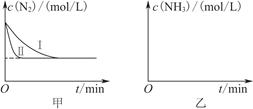
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�״���һ�N��������Դ�����ЏV�����_�l(f��)�͑�(y��ng)��ǰ����
��1�����I(y��)��һ��������ЃɷN����(y��ng)�ϳɼ״���
����(y��ng)��CO��g����2H2��g��=CH3OH��g������H1
����(y��ng)��CO2��g����3H2��g��=CH3OH��g����H2O��g������H2
����������(y��ng)���ϡ�ԭ�ӽ�(j��ng)��(j��)��ԭ�t����________�������
���±����Д�(sh��)��(j��)�Ƿ���(y��ng)���ڲ�ͬ�ض��µĻ��W(xu��)ƽ�ⳣ��(sh��)��K����
| �ض� | 250 �� | 300 �� | 350 �� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�S�����繤�I(y��)��(j��ng)��(j��)�İl(f��)չ���˿ڵĄ�����ȫ����Դ�o�������������RԽ��Խ��(y��n)�صĆ��}����ν��ʹ����CO2�ĺ�������Ч���_�l(f��)����CO2������ȫ������ձ���ҕ��
��1����D��C�����������׃���P(gu��n)ϵ�D������׃�����ÓQ����(y��ng)���t�仯�W(xu��)����ʽ�ɞ�______________________________________��
�D��׃���^����Щ�����ᷴ��(y��ng)________������̖(h��o)����
��2���״���һ�N��������Դ�������_�l(f��)�͑�(y��ng)�õďV�ǰ�������I(y��)�Ͽ������·����ϳɼ״���
����һ��CO��g����2H2��g��??CH3OH��g��
��������CO2��g����3H2��g��??CH3OH��g����H2O��g��
��25�桢101 kPa�£�1�˼״���ȫȼ���ş�22.68 kJ�������״�ȼ���ğữ�W(xu��)����ʽ��_____________________________________________��
ij�����l(f��)늏SCO2������ŷ�����2 200�f������CO2��ȫ�D(zhu��n)����״����t��Փ���ɴ˫@�õļ״���ȫȼ���ş�s��________kJ��������λ��Ч��(sh��)�֣���
��3�������ұ���^��������һ������(y��ng)�nj�ԭ�Ͻ�tʯ�D(zhu��n)����TiO2����tʯ����2C��2Cl2�ߜ�,TiCl4��2CO����֪��C��s����O2��g��=CO2��g������H����393.5 kJ��mol��1
2CO��g����O2��g��=2CO2��g������H����566 kJ��mol��1
TiO2��s����2Cl2��g��=TiCl4��s����O2��g������H����141 kJ��mol��1
�tTiO2��s����2Cl2��g����2C��s��=TiCl4��s����2CO��g���Ħ�H��________��
��4�����������ڃ����՚⣬���ˮ������̎�����I(y��)�U�������Ư�ׄ������������c���K����㞡�����������І��|(zh��)����(y��ng)���磺
6Ag��s����O3��g��=3Ag2O��s������H����235.8 kJ��mol��1��
��֪��2Ag2O��s��=4Ag��s����O2��g����H����62.2 kJ��mol��1��
�tO3�D(zhu��n)����O2�ğữ�W(xu��)����ʽ��_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
�\(y��n)�û��W(xu��)����(y��ng)ԭ��֪�R(sh��)�ڹ��I(y��)���a(ch��n)������Ҫ���x��
��1�� ���I(y��)���a(ch��n)������NH3(g)�cCO2(g)��(j��ng)�ɲ�����(y��ng)�������أ��ɲ�����(y��ng)������׃��ʾ��D���£�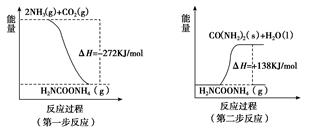
�tNH3(g)�cCO2(g)����(y��ng)�������صğữ�W(xu��)����ʽ��___________ _____��
��2�����I(y��)���a(ch��n)����CO���Ժϳɼ״�CO(g)��2H2(g)  CH3OH(g)����H����90.1 kJ��mol��1 ��һ������(qi��ng)�£��ݷe��V L�������г���a mol CO�c2a mol H2���ڴ��������·���(y��ng)���ɼ״���ƽ���D(zhu��n)�����c�ضȡ�����(qi��ng)���P(gu��n)ϵ��D��ʾ��
CH3OH(g)����H����90.1 kJ��mol��1 ��һ������(qi��ng)�£��ݷe��V L�������г���a mol CO�c2a mol H2���ڴ��������·���(y��ng)���ɼ״���ƽ���D(zhu��n)�����c�ضȡ�����(qi��ng)���P(gu��n)ϵ��D��ʾ��
��p1________p2(����ڡ�����С�ڡ����ڡ�)��
��100 ��r(sh��)��ԓ����(y��ng)�Ļ��W(xu��)ƽ�ⳣ��(sh��)K��_ ____(mol��L��1)��2��
���������l����׃����r�£�������a mol CO��2a molH2���_(d��)����ƽ��r(sh��)��CO���D(zhu��n)����________(��������pС����׃��)��
��3�����I(y��)���a(ch��n)����SO2��ԭ����ȡ����
������ԭ늳�ԭ������SO2��O2��H2O���Ƃ����ᣬԓ늳��ö�ײ�����늘O�������������w��ͬ�r(sh��)Ҳ��ʹ���w�c늽��|(zh��)��Һ��ֽ��|��Ո(q��ng)����ԓ늳ص�ؓ(f��)�O��늘O����(y��ng)ʽ___ ____________��
����Na2SO3��Һ�������SO2��NaHSO3��Һ��Ȼ��늽�ԓ��Һ���Ƶ����ᡣ늽�ԭ��ʾ��D���D��ʾ��Ո(q��ng)�����_ʼ�r(sh��)ꖘO����(y��ng)��늘O����(y��ng)ʽ____ ______��
��4�����I(y��)���a(ch��n)���ð�ˮ����SO2
�����|(zh��)������SO2�cNH3����ˮ��ַ���(y��ng)������ԓ����(y��ng)���x�ӷ���ʽ ��������Һ�� �ԡ�
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com