
已知:A為常見的短周期輕金屬,含A的合金材料常用于火箭、飛機等制造業;B是一種鹽,在工農業生產中用途較廣;C、F、H為常見非金屬單質;常溫下C、F、I、E、J和K為氣體;E對空氣的相對密度為0.586;常溫常壓下G為液體。有關物質間的轉化關系如下(圖中部分反應物或產物已省略):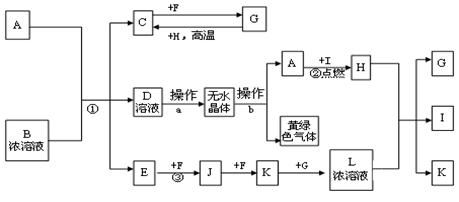
請填空:
(1)B的化學式為 。
(2)操作a必須在HCl氣流中加熱得無水物而不能直接加熱濃縮,其原因是 ;操作b為 。
(3)反應①的離子反應方程式為 。反應③的化學反應方程式為 。
(1)NH4Cl (2)抑制Mg2+的水解( 寫方程式同樣給分), 熔融狀態下電解
(3)Mg+2NH4+=Mg2++H2↑+2NH3↑ 4NH3+5O2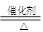 4NO+6H2O
4NO+6H2O
解析試題分析:根據題給信息和轉化關系圖分析,A為常見的短周期輕金屬,含A的合金材料常用于火箭、飛機等制造業,則A為鎂;E對空氣的相對密度為0.586,E的相對分子質量為17,E為氨氣;常溫常壓下G為液體,G為水;黃綠色氣體為氯氣,結合流程圖及相關物質的轉化關系知,B是一種鹽,為氯化銨,C為氫氣,D為氯化鎂,F為氧氣,H為碳,I為二氧化碳,J為一氧化氮,K為二氧化氮,L為硝酸;(1)B為氯化銨,化學式為NH4Cl;(2)操作a為由氯化鎂溶液中得無水氯化鎂,氯化鎂為強酸弱堿鹽,為抑制Mg2+的水解,必須在HCl氣流中加熱得無水物;操作b為熔融狀態下電解;(3)反應①為鎂和氯化銨溶液反應生成氫氣、氨氣和氯化鎂,離子反應方程式為Mg+2NH4+=Mg2++H2↑+2NH3↑;反應③為氨的催化氧化,化學反應方程式為4NH3+5O2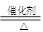 4NO+6H2O。
4NO+6H2O。
考點:考查無機推斷及相關物質的性質及相互轉化關系。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
如圖表示各物質之間的轉化關系。已知D、E、Z是中學化學常見的單質,其他都是化合物。Z、Y是氯堿工業的產品。D元素的原子最外層電子數與電子層數相等,且D的硫酸鹽可作凈水劑。E為日常生活中應用最廣泛的金屬。除反應①外,其他反應均在水溶液中進行。請回答下列問題。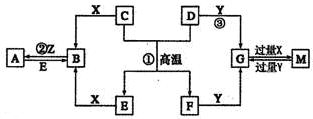
(1)寫出X的電子式: 。
(2)常溫時pH =12的G溶液中,溶質的陽離子與溶質的陰離子濃度之差為 (寫出計算式)。
(3)在電鍍工業中,若將E作為待鍍金屬,銅為鍍層金屬,則銅是____極,請寫出在E電極上發生的電極反應式: 。
(4)寫出反應③的離子方程式: 。
(5)現有無標簽的Y和M的兩種無色水溶液,不用其他任何試劑,請你設計一個簡單的實驗對這兩種溶液加以鑒別 (回答實驗操作、現象及結論)。
(6)A溶液與NaOH溶液混合可形成沉淀,某溫度下此沉淀的Ksp =2.097×l0-39。將0.01 mol/L的A溶液與0.001 mol·L-1的NaOH溶液等體積混合,你認為能否形成沉淀____(填“能”或“不能”),請通過計算說明 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖中A~G是化合物,H是一種無色氣態單質,D高溫下是氣體,而常溫下是一種無色液體, E為淡黃色的固體。它們之間有如下轉化關系: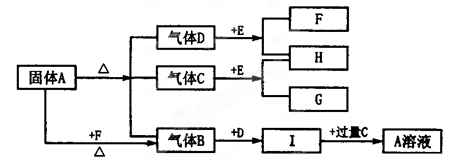
(1)寫出A的化學式 ;C的結構式 ;
(2)A溶液與過量F溶液反應的離子方程式
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
如下圖所示中各方框表示有關的一種反應物或生成物(某些物質已經略去),其中常溫下A、C和D為無色氣體,C能使濕潤的紅色石蕊試紙變藍,X分解產生A、B和C三種產物的比值為1:1:1。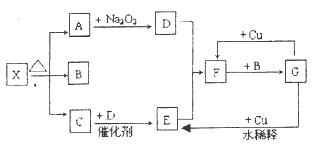
(1)寫出下列各物質的化學式:
X: ;B: ;F: ;G: 。
(2)按要求寫出下列變化的反應化學方程式:
A→D的化學反應方程式: ;
G→E的離子反應方程式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
三種金屬單質A、B、C與氣體甲、乙、丙及物質D、E、F、G、H之間發生如下轉化關系(圖中有些反應的產物和反應的條件沒有標出)。請根據以上信息回答下列問題: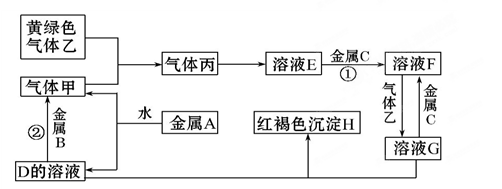
(1)寫出下列物質的化學式:
A_____、乙____ ,C的一種氧化物是具有磁性的黑色晶體,該氧化物的化學式是__________。
(2)寫出反應②的化學方程式: ____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
中學化學中常見的幾種物質存在下圖所示的轉化關系。其中, A是一種黑色粉末狀固體,C是一種黃綠色氣體,實驗室中常用E溶液吸收多余的C。(圖中部分產物和反應條件已略去)。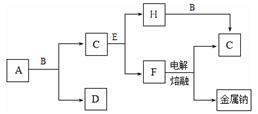
試回答下列問題:
(1)寫出A與B的濃溶液反應的化學方程式 。
(2)將B的濃溶液與H的濃溶液混合,立即產生大量氣體C,該反應的離子方程式為 。
(3)某課外小組同學用E溶液吸收C,利用下圖所示裝置向吸收液中持續通入SO2氣體。實驗過程中觀察到如下現象: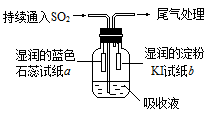
①開始時,溶液上方出現白霧,試紙a變紅。甲同學認為是HCl使a變紅,乙同學不同意甲的觀點,乙同學認為使a變紅的是
(寫出一種即可)。
②片刻后,溶液上方出現黃綠色氣體,試紙b變藍。用離子方程式解釋b變藍的原因: 。
③最終試紙b褪色。同學們認為可能的原因有兩種:一是I2有還原性,黃綠色氣體等物質將其氧化成IO3-,從而使藍色消失;二是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、X是中學化學常見物質,均由短周期元素組成,轉化關系如圖。請針對以下三種不同情況回答:
(1)若A、B、C中均含同一種常見金屬元素,該元素在 C中以陰離子形式存在,將A、C的水溶液混合可得B的白色膠狀沉淀。
①A中含有的金屬元素的原子結構示意圖為 。
②該金屬元素的單質與某紅色氧化物在高溫下反應,可用于焊接鐵軌及定向爆破,已知:1mol該單質完全反應,當溫度恢復至298K時,共放熱QkJ,請寫出該反應的熱化學反應方程式為 。
(2)若A、B、C的焰色反應均呈黃色,水溶液均為堿性。
①用化學方程式表明B溶液呈堿性的原因 。
②自然界中存在B、C和H2O按一定比例結晶而成的固體。取一定量該固體溶于水配成100 mL溶液,測得溶液中金屬陽離子的濃度為0.5 mol/L。若取相同質量的固體加熱至恒重,剩余固體的質量為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
X是一種新型無機材料,它與碳化硅(SiC)結構相似、物理性質相近。 X有如下的轉化關系:其中,C是一種能使濕潤的紅色石蕊試紙變藍的無色氣體,D為白色膠狀沉淀,E溶液的焰色反應火焰呈黃色,M是一種常見金屬,過量的M與L可生成Q和I。
(1)X與A溶液反應的離子方程式為
(2)把紅熱的木炭投入到L的濃溶液中,可發生劇烈反應,
①化學方程式為_________________
②若把產生的氣體通入足量的飽和碳酸氫鈉溶液中,再把逸出的氣體干燥后通入足量的過氧化鈉固體,充分反應后,再通入水中,最后收集到的氣體是 ______________________
③若把產生的氣體直接通入足量的澄清石灰水中,現象是__________________________
(3)將K、I、G混合氣體充滿容器后倒置于水槽中,氣體完全溶解,溶液充滿整個容器。則三者的物質的量之比可能為_______
A.1∶1 ∶1 B.4∶2∶2.5 C.4∶8∶7 D.6∶4∶5
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
構建知識網絡是學習化學的重要方法。下列物質的轉化網絡可以概括幾類反應,其中A、B、D、E、M、N、X、Y均表示一種中學化學中常見的無機物,反應②、③、④、⑤
的生成物可以是一種或幾種。請回答下列問題: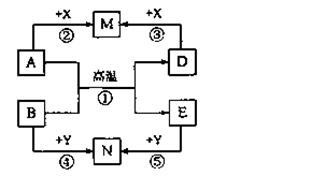
(1)A為固態非金屬單質時,若反應①用于生產半導體材料,則M為________ Y為 。
(2)A為金屬單質時,若M為NaAlO2溶液,N為棕黃色溶液,反應⑤的離子方程式是 。
(3)反應①在常溫下進行時,也有很多組物質符合網絡圖中的轉化關系,請列舉一例(要求反應①中只有一種元素的化合價發生變化):A、B的化學式分別是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com