
(16分)I、用CH4催化還原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+ CO2(g)+2H2O(g) △H=" -574" kJ·mol-l
②CH4(g)+4NO(g)=2N2(g)+ CO2(g)+ 2H2O(g) △H=" -1160" kJ·mol-l
③H2O(g)=H2O(1) △H=-44.0 kJ·mol-l
寫出CH4(g)與NO2(g)反應生成N2(g)、CO2(g)和H2O(1)的熱化學方程式____ 。
II、開發新能源和三廢處理都是可持續發展的重要方面。
(1)由碳的氧化物贏接合成乙醇燃料已進入大規模生產。如采取以CO和H2為原料合成乙醇,化學反應方程式:2CO(g)+4H2(g)-CH3CH2OH(g)+H2O(g);若密閉容器中充有10 mol CO與20mol H2,在催化劑作用下反應生成乙醇:CO的轉化率(a)與溫度、壓強的關系如圖所示。
①若A、B兩點表示在某時刻達到的平衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數:K=____ ;
②若A、C兩點都表示達到的平衡狀態,則白反應開始到達平衡狀態所需的時間tA tC(填 “>”、“<”或“=”)。
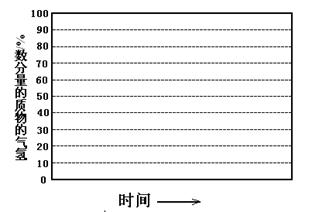
(2)日前工業上也可以用CO2來生產甲醇。一定條件下發生反應:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)△H<0,若將6mo1 CO2和8mol H2充入2L的密閉容器中,測得H2的物質的量隨時間變化的曲線如右圖所示(實線)。
CH3OH(g)+H2O(g)△H<0,若將6mo1 CO2和8mol H2充入2L的密閉容器中,測得H2的物質的量隨時間變化的曲線如右圖所示(實線)。
①若改變某一實驗條件再進行兩次實驗,測得H2的物質的量隨時間變化如圖中虛線所示,曲線I對應的實驗條件改變可能是 ,曲線II對應的實驗條件改變可能是____ 。
②請在答題卷圖中繪出甲醇的物質的量隨時間變化曲線。
III、用MnO2制KMnO4的工藝流程如圖:電解池中兩極材料均為碳棒,在水或酸性溶液中K2MnO4發生歧化而變成MnO2和KMnO4。
①寫出240℃熔融時發生反應的化學方程式 ,投料時必須滿足n(KOH):n(MnO2) 。
②陽極的電極反應為 。
③B物質是 (填化學式),可以循環使用的物質是 (填化學式)。
28.(16分)Ⅰ、 CH4(g)+2NO2(g) = N2(g) + CO2(g) +2H2O(l) ⊿H=" -955" kJ·mol-1(2分)
Ⅱ、(1)①K="0.25" (2分) ② > (1分)
(2)①升溫(1分)增壓(1分)(其他合理答案參照給分)
②如右圖(2分)
Ⅲ、① 2MnO2 + O2 + 4KOH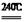 2K2MnO4 + 2H2O(2分)
2K2MnO4 + 2H2O(2分)
大于2 : 1 (1分)
② MnO42- - e- = MnO4- (2分)
③ H2(1分) KOH固體 (1分)
解析試題分析:Ⅰ:(1)將方程式(①+②+③×4)/2得CH4(g)與NO2(g)反應生成N2(g)、CO2(g)和H2O的方程式,故△H=(-574 -1160-44.0×4)/2= -955 kJ·mol-1;Ⅱ:(1)①A點時CO的轉化率為50%,轉化量為5mol,故平衡時CO、H2、CH3CH2OH、H2O的物質的量分別為5mol、10mol、2.5mol、2.5mol,平衡濃度分別為0.5mol/L、1mol/L、0.25mol/L、0.25mol/L,代入平衡常數表達式K=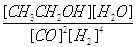 =0.25;②C點的溫度高,反應速率快,達到平衡所用的時間短;(2)①曲線Ⅰ和實線相比較,加快了反應速率,平衡向左移動了,故為升高溫度;虛線Ⅱ和實線相比較,反應速率加快,平衡向右移動了,故為加壓;②甲醇的物質的量從零開始逐漸增大,達到平衡狀態時氫氣消耗6mol,生成甲醇2mol,以后甲醇的物質的量不再發生變化了;Ⅲ①由題目信息可得通過二氧化錳和KOH、氧氣在熔融條件下生成K2MnO4,結合原子守恒和氧化還原方程式的配平方法寫出化學方程式;當KOH和二氧化錳之比為2:1時恰好完全反應,當在水或酸性溶液中K2MnO4發生歧化而變成MnO2和KMnO4,需保持堿性環境,故兩者物質的量之比大于2:1;②陽極MnO42-失去電子發生氧化反應生成MnO4- ,故為MnO42- - e- = MnO4- ;③陰極氫離子得電子生成氫氣,同時生成氫氧化鉀,氫氧化鉀可以循環使用。
=0.25;②C點的溫度高,反應速率快,達到平衡所用的時間短;(2)①曲線Ⅰ和實線相比較,加快了反應速率,平衡向左移動了,故為升高溫度;虛線Ⅱ和實線相比較,反應速率加快,平衡向右移動了,故為加壓;②甲醇的物質的量從零開始逐漸增大,達到平衡狀態時氫氣消耗6mol,生成甲醇2mol,以后甲醇的物質的量不再發生變化了;Ⅲ①由題目信息可得通過二氧化錳和KOH、氧氣在熔融條件下生成K2MnO4,結合原子守恒和氧化還原方程式的配平方法寫出化學方程式;當KOH和二氧化錳之比為2:1時恰好完全反應,當在水或酸性溶液中K2MnO4發生歧化而變成MnO2和KMnO4,需保持堿性環境,故兩者物質的量之比大于2:1;②陽極MnO42-失去電子發生氧化反應生成MnO4- ,故為MnO42- - e- = MnO4- ;③陰極氫離子得電子生成氫氣,同時生成氫氧化鉀,氫氧化鉀可以循環使用。
考點:蓋斯定律、化學平衡常數的計算、影響化學平衡的條件、電極反應式的書寫和電極產物的判斷等知識


科目:高中化學 來源: 題型:填空題
以黃鐵礦(主要成分是FeS2)為原料生產硫酸的工藝流程圖如下:
(1)若從下列四個城市中選擇一處新建一座硫酸廠,你認為廠址宜選在______的郊區(填標號)
A.有豐富黃鐵礦資源的城市 B.風光秀麗的旅游城市
C.消耗硫酸甚多的工業城市 D.人口稠密的文化、商業中心城市
(2)沸騰爐中發生反應的化學方程式為_____,接觸室中發生反應的化學方程式是_____。
(3) 在硫酸工業制法中,下列生產操作與說明生產操作的主要原因二者都正確的是_____。
A. 硫鐵礦燃燒前要粉碎,因為大塊的黃鐵礦不能在空氣中反應
B. 從沸騰爐出來的氣體要凈化,因為爐氣中的SO2會與雜質反應
C. SO2氧化成SO3要用催化劑,這樣可提高SO2的轉化率
D. SO3用98. 3%的濃硫酸來吸收,目的是為了防止形成酸霧,以提髙SO3吸收效率
(4) 下表是壓強對SO2平衡轉化率的影響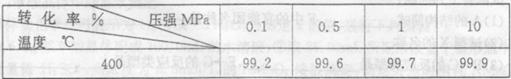
對于SO2轉化SO3的反應,增大壓強可使轉化率______________,但在實際工業生產中常采用常壓條件,理由是________________________________。
(5)某工廠用500t含硫量為48%的黃鐵礦制備硫酸,若在沸騰爐中有2%的FeS2損失,在接觸室中SO3的產率為96%,則可得到98%的濃硫酸的質量是_____t。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
一定溫度時,在容積一定的密閉容器中,反應A(?)+B(g)  C(g)+D(g)達到平衡后,升高溫度容器內氣體的密度增大。請回答下列問題:
C(g)+D(g)達到平衡后,升高溫度容器內氣體的密度增大。請回答下列問題:
(1)正反應是 (填“放熱”或“吸熱”)反應;該反應的化學平衡常數的表達式是 。
(2)能判斷該反應一定達到平衡狀態的依據是 。(填寫字母編號)
A.體積分數組成C%=D%
B.單位時間內生成n molA的同時生成n molC
C.溫度和體積一定時,某一生成物濃度不再變化
D.溫度和體積一定時,容器內壓強不再變化
(3)該反應的正反應速率隨時間變化的關系如圖所示。t2時改了某種條件,改變的條件是 。(填寫字母編號)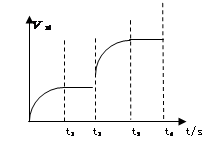
A.升溫 B.加壓 C.催化劑 D.增加A的量
(4)升高溫度到T℃時,在一密閉容器中充入2mol A和3mol B,發生上述反應。平衡后測得K=1。然后在溫度不變的情況下,擴大容器容積至原來的10倍,結果A的百分含量始終未改變,則此時B的轉化率是 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(18分)為有效控制霧霾,各地積極采取措施改善大氣質量,研究并有效控制空氣中的氮氧化物、碳氧化物和硫氧化物含量顯得尤為重要。
(1)汽車內燃機工作時會引起N2和O2的反應:N2(g)+O2(g) 2NO(g),是導致汽車尾氣中含有NO的原因之一。
2NO(g),是導致汽車尾氣中含有NO的原因之一。
①在T1、T2溫度下,一定量的NO發生分解反應時N2的體積分數隨時間變化如圖所示,根據圖像判斷反應N2(g)+O2(g) 2NO(g)的△H__________0(填“>”或“<”)。
2NO(g)的△H__________0(填“>”或“<”)。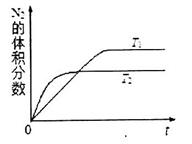
②在T3溫度下,向2L密閉容器中充入10molN2與5mo1O2,50秒后達到平衡,測得NO的物質的量為2mol,則該反應的速率v (N2)=___________________。該溫度下,若開始時向上述容器中充入N2與O2均為1 mol,則達到平衡后N2的轉化率為____________。
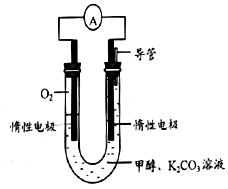
(2)利用下圖所示裝置(電極均為惰性電極)可吸收SO2,用陰極排出的溶液可吸收NO2。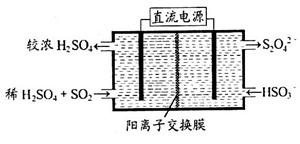
①陽極的電極反應式為_____________________。
②在堿性條件下,用陰極排出的溶液吸收NO2,使其轉化為無害氣體,同時有SO32—生成。該反應中氧化劑與還原劑的物質的量之比為_______________。
(3)一定條件下可用甲醇與CO反應生成醋酸消除CO污染。常溫下,將a mol·L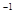 的醋酸與b mol
的醋酸與b mol L
L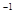 Ba(OH)2溶液等體積混合,充分反應后,溶液中存在2c(Ba2+)=c(CH3COO-),則該混合溶液中醋酸的電離常數Ka=______________________(用含a和b的代數式表示)。
Ba(OH)2溶液等體積混合,充分反應后,溶液中存在2c(Ba2+)=c(CH3COO-),則該混合溶液中醋酸的電離常數Ka=______________________(用含a和b的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(18分)堿金屬元素的單質及其化合物被廣泛應用于生產、生活中。
②一定量的Na在足量O2中充分燃燒,參加反應的O2體積為5.6 L(標準狀況),則該反應過程中轉移電子的數目為_________。
(2)金屬鋰廣泛應用于化學電源制造,鋰水電池就是其中的一種產品。該電池以金屬鋰和 鋼板為電極材料,以LiOH為電解質,加入水即可放電。
總反應為:2Li+2H2O=2LiOH+H2↑
①鋰水電池放電時,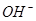 向_________極移動。
向_________極移動。
②寫出該電池放電時正極的電極反應式:_________________。
③電解熔融LiCl可以制備金屬Li。但LiC1熔點在873 K以上,高溫下電解,金屬Li產量極低。經過科學家不斷研究,發現電解LiCl—KCl的熔鹽混合物可以在較低溫度下生成金屬Li。
你認為,熔鹽混合物中KCl的作用是_________________________________________。
寫出電解該熔鹽混合物過程中陽極的電極反應式:______________________________。
(3)最新研究表明,金屬鉀可作工業上天然氣高溫重整的催化劑,有關反應為: 。一定溫度下,向2 L容積不變的密閉容器中充入4 mol
。一定溫度下,向2 L容積不變的密閉容器中充入4 mol 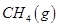 和6 mo1 H2O(g)發生反應,10 min時,反應達到平衡狀態,測得CH4(g)和H2(g)的物質的量隨時間變化的曲線如圖所示。
和6 mo1 H2O(g)發生反應,10 min時,反應達到平衡狀態,測得CH4(g)和H2(g)的物質的量隨時間變化的曲線如圖所示。
①0~10 min內用 (CO)表示的化學反應速率為_________。
(CO)表示的化學反應速率為_________。
②下列敘述中,能夠證明該反應已達到平衡狀態的是_________(填序號)。
a.生成3 molH-H鍵的同時有4 molC-H鍵斷裂
b.其他條件不變時,反應體系的壓強保持不變
c.反應混合氣體的質量保持不變
d.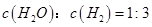
③此溫度下,該反應的化學平衡常數K=_________mo12·L-2。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(14分)工業上一般在恒容密閉容器中可以采用下列反應合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(1)判斷反應達到平衡狀態的依據是(填字母序號)__________
| A.生成CH3OH的速率與消耗CO的速率相等 | B.混合氣體的密度不變 |
| C.混合氣體的相對平均分子質量不變 | D.CH3OH、CO、H2的濃度都不再發生變化 |
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
[15分]甲烷自熱重整是先進的制氫方法,包含甲烷氧化和蒸汽重整。向反應系統同時通入甲烷、氧氣和水蒸氣,發生的主要化學反應有:
| 反應過程 | 化學方程式 | 焓變△H (kJ/mol) | 活化能Ea (kJ/mol) |
| 甲烷氧化 | CH4(g)+2O2(g) CO2(g)+2H2O(g) CO2(g)+2H2O(g) | -802.6 | 125.6 |
CH4(g)+O2(g) CO2(g)+2H2(g) CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 蒸汽重整 | CH4(g)+H2O(g) CO(g)+3H2(g) CO(g)+3H2(g) | 206.2 | 240.1 |
CH4(g)+2H2O(g) CO2(g)+4H2(g) CO2(g)+4H2(g) | 165.0 | 243.9 |
 CO2(g)+H2(g)的△H= kJ/mol。
CO2(g)+H2(g)的△H= kJ/mol。 CO(g)+3H2(g)的KP= ;
CO(g)+3H2(g)的KP= ;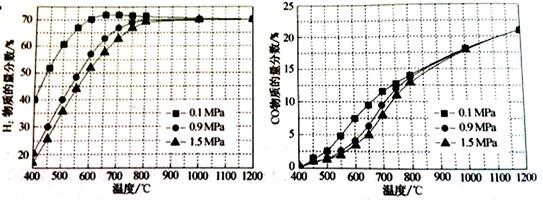
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
I.800℃時,向容積為2L的恒容密閉容器中充入一定量的CO和H2O維持恒溫,發生反應CO(g)+H2O(g) H2(g)+CO2(g),反應過???中測定的部分數據見下表:
H2(g)+CO2(g),反應過???中測定的部分數據見下表:
| 反應時間/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | | 0.80 |
| n(H2O)/ mol | 0.60 | | 0.20 | |


 2NH4+(aq) + Mg(OH)2(s)該反應化學平衡常數的表達式為K= ,列出該反應平衡常數K與Kb(NH3·H2O)、Ksp(Mg(OH)2)的關系式 。
2NH4+(aq) + Mg(OH)2(s)該反應化學平衡常數的表達式為K= ,列出該反應平衡常數K與Kb(NH3·H2O)、Ksp(Mg(OH)2)的關系式 。查看答案和解析>>
科目:高中化學 來源: 題型:計算題
(1)將不同量的CO(g)和H2O(g)分別通入體積2L的恒容密閉容器中,進行反應CO(g)+H2O(g) CO2(g)+H2(g),得到如下兩組數據:
CO2(g)+H2(g),得到如下兩組數據:
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com