
下列物質屬于電解質的是 ;能導電的物質是 。
①氨水 ②蔗糖 ③燒堿 ④NH3·H2O ⑤CO2 ⑥銅
 新活力總動員暑系列答案
新活力總動員暑系列答案 龍人圖書快樂假期暑假作業鄭州大學出版社系列答案
龍人圖書快樂假期暑假作業鄭州大學出版社系列答案科目:高中化學 來源: 題型:填空題
某溶液中的溶質由下列中的幾種離子構成:Na+、Fe3+、Cu2+、Ba2+、AlO2—、CO32—、SO32—、SO42—。取該溶液進行有關實驗,實驗步驟及結果如下:
①向溶液中加入過量稀鹽酸,得到氣體甲和溶液甲;
②向溶液甲中加入過量NH4HCO3溶液,得到白色沉淀乙、氣體乙和溶液乙;
③向溶液乙中加入過量Ba(OH) 2溶液,得到白色沉淀丙、氣體丙和溶液丙。
④檢驗氣體甲、氣體乙、氣體丙,都只含有一種成份,而且各不相同。
請回答下列問題:
(1)只根據實驗①能得出的結論是 (3分)
(2)沉淀丙中一定含有 (1分),可能含有 (1分)
(3)該溶液中肯定存在的離子有
(4)氣體乙分子的結構式為
(5)向溶液甲中加入NH4HCO3溶液至過量,該過程中可能發生反應的離子方程式為 ; ; (根據需要,可不填完,也可補充)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有以下物質:①KCI晶體②食鹽水③液態的醋酸④I2⑤BaSO4固體⑥蔗糖(C12H22O11 )⑦酒精(C2H5OH)⑧熔融的NaOH⑨K2O⑩SO2。請回答下列問題:
(1)以上物質中能導電的是_________________(用序號)。
(2)以上物質屬于電解質的是_________________(用序號)。
(3)以上物質中屬于非電解質的是_________________(用序號)。
(4)從②溶液中得到氯化鈉固體,應選擇下列裝置中的______________(填代表裝置圖的字母,下同);分離④與⑦的混合液,應選擇下列裝置中的________________。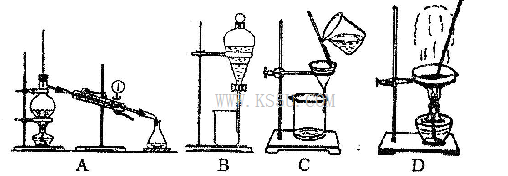
(5)請寫出③和⑧中兩種物質的溶液混合后發生反應的離子方程式:________________________________________________________________________.
(6)在標準狀況下,__________L⑩與34. 2g⑥中含有相同的氧原子數。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有含NaCl、Na2SO4和NaNO3的混合物,選擇適當的試劑將其轉化為相應的沉淀或固體,從而實現Cl-、SO42-、和NO3-的相互分離。相應的實驗過程可用下圖表示: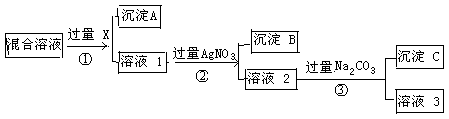
請回答下列問題:⑴寫出實驗流程中下列物質的化學式
試劑X : 沉淀A:
⑵上述實驗流程中加入過量的Na2CO3的目的是 。
⑶按此實驗方案得到的溶液3中肯定含有 (填化學式)雜質。
(4)請寫出①②中反應的離子方程式①
②
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有下列物質①NaCl晶體②冰醋酸(純醋酸晶體) ③干冰 ④銅⑤蔗糖 ⑥熔融的KNO3 ⑦稀硫酸溶液 ⑧酒精 ⑨液氯⑩BaSO4固體
(1)以上物質能導電的是 ;(2)以上物質屬于電解質的是 ;(3)以上物質屬于非電解質的是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在某鈉鹽溶液中,除Cl-之外可能還含有等物質的量的下列陰離子中的一種或多種:SO32-、CO32-、SiO32-、I-、NO3-、SO42-。在此溶液中加入過量鹽酸,產生氣泡,溶液顏色變深,但仍澄清,并且原溶液中的陰離子種類減少了3種。試回答下列問題。
(1)原溶液中是否有SiO32-? (填“有”或“沒有”),判斷理由是 。(用離子方程式表示)
(2)生成的氣體中一定有 。它具有的性質是 (填字母序號)。
| A.無色無味 |
| B.無色有刺激性氣味 |
| C.屬于大氣污染物 |
| D.難溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(12分)(1)環境專家認為可以用金屬鋁將水體中的NO3-轉化為N2,從而消除污染。該反應中涉及的微粒有:H2O、Al、OH-、Al(OH)3、NO3-、N2,請將這些微粒中除NO3-以外的微粒填入以下空格內(不用配平)。 
該反應過程中,被氧化與被還原的元素的物質的量之比為 。
(2)我國首創的海洋電池以海水為電解質溶液,電池總反應是4Al +3O2+6H2O ="4" Al(OH)3。電池正極的電極反應式是 ;消耗13.5 g Al時轉移_________mole-。
(3)鋁與某些金屬氧化物在高溫下的反應稱為鋁熱反應,可用于冶煉高熔點的金屬。
已知:4Al(s) +3O2(g) = 2Al2O3(s)△H = -2830 kJ/mol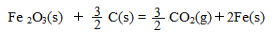 △H = +230 kJ/mol
△H = +230 kJ/mol
C(s)+O2(g) = CO2(g) △H = -390 kJ/mol
鋁與氧化鐵發生鋁熱反應的熱化學方程式是 ,鋁熱反應屬于______(填字母)反應。
a.氧化還原 b.復分解 c.置換
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)M由兩種短周期元素組成,每個M分子含有18個電子,其分子球棍模型如圖所示。測得M的摩爾質量為32g/mol。畫出編號為2的原子結構示意圖: 。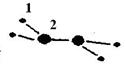
(2)已知1.0mol·L—1NaHSO3溶液的pH為3.5,加入氯水,振蕩后溶液pH迅速降低。溶液pH降低的原因是 (用離子方程式表示)。
(3)在常溫常壓和光照條件下,N2在催化劑(TiO2)表面與H2O反應,生成1molNH3和O2時的能量變化值為382.5kJ,達到平衡后此反應NH3生成量與溫度的實驗數據如下表。則該反應的熱化學方程式為 。
| T/K | 303 | 313 | 323 |
| NH3生成量/(10—1mol) | 4.3 | 5.9 | 6.0 |
 Mg2+(aq) +2NH3·H2O(aq)
Mg2+(aq) +2NH3·H2O(aq) | 實驗① | 等體積1 mol/L氨水和0.1 mol/L MgCl2溶液混合 | 生成白色沉淀 |
| 實驗② | 等體積0.1 mol/L氨水和1 mol/L MgCl2溶液混合 | 無現象 |
| 實驗編號 | I—的初始濃度 (mol·L—1) | ClO—的初始濃度 (mol·L—1) | OH—的初始濃度 (mol·L—1) | 初始速率v (mol·L—1· s—1) |
| 1 | 2 × 10—3 | 1.5 × 10—3 | 1.00 | 1.8 × 10—4 |
| 2 | a | 1.5 × 10—3 | 1.00 | 3.6 × 10—4 |
| 3 | 2 × 10—3 | 3 × 10—3 | 2.00 | 1.8 × 10—4 |
| 4 | 4 × 10—3 | 3 × 10—3 | 1.00 | 7.2 × 10—4 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
同位素示蹤法可用于反應機理的研究,下列反應或轉化中同位素示蹤表示正確的是( )
| A.2Na218O2 + 2H2O ="=" 4Nal8OH + O2↑ |
| B.NaH+D2O===NaOH+D2↑ |
| C.2KMnO4 + 5H218O2 + 3H2SO4 ="=" K2SO4 + 2MnSO4 + 518O2↑+ 8H2O |
| D.K37ClO3 + 6HCl ="=" K37Cl + 3Cl2↑+ 3H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com