
【題目】芳香化合物在催化劑催化下與鹵代烴發生取代反應稱為Friedel-Crafts烷基化反應。某科研小組以苯和氯代叔丁烷[ClC(CH3)3]為反應物,無水AlCl3為催化劑條件下制備叔丁基苯(![]() )。
)。
反應如下: +ClC(CH3)3
+ClC(CH3)3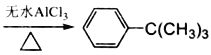 +HCl
+HCl
已知下列信息:
物質 | 相對分子質量 | 密度 | 熔點 | 沸點 | 溶解性 |
AlCl3 | —— | —— | 190℃ | 180℃ | 遇水極易潮解并產生白色煙霧,微溶于苯 |
苯 | 78 | 0.88g/cm3 | —— | 80.1℃ | 難溶于水,易溶于乙醇 |
氯代叔丁烷 | 92.5 | 1.84 g/cm3 | —— | 51.6℃ | 難溶于水,可溶于苯 |
叔丁基苯 | 134 | 0.87 g/cm3 | —— | 169℃ | 難溶于水,易溶于苯 |
I、如下圖是實驗室制備無水AlCl3的實驗裝置:
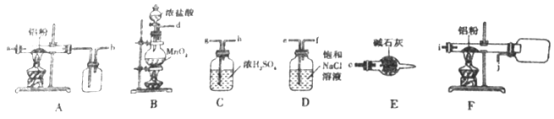
(1)E裝置中的儀器名稱是_______________。
(2)寫出B裝置中發生反應的離子方程式:________________________。
(3)選擇合適的裝置制備無水AlCl3正確的連接順序為:_____________ (寫導管口標號)。
(4)下列操作正確的是________。
甲:先加熱硬質玻璃管再加熱圓底燒瓶
乙:先加熱圓底燒瓶再加熱硬質玻璃管
(5)E裝置的作用是:_______________________。
p>II、實驗室制取叔丁基苯裝置如圖: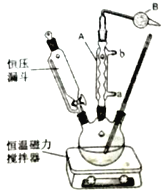
在三頸燒瓶中加入50mL的苯和適量的無水AlCl3,由恒壓漏斗滴加氯代叔丁烷[ClC(CH3)3]10mL,一定溫度下反應一段時間后,將反應后的混合物洗滌分離,在所得產物中加入少量無水MgSO4固體,靜置,過濾,蒸餾得叔丁基苯20g。
(6)使用恒壓漏斗的優點是____________________;加無水MgSO4固體的作用是___________。
(7)上述反應后混合物的洗滌所用的試劑有如下三種,正確的順序是_____________。
①5%Na2CO3溶液 ②稀鹽酸 ③H2O
(8)叔丁基苯的產率為______。(保留3位有效數字)
【答案】 干燥管 MnO2+4H++2C1-=Mn2++Cl2↑+2H2O d、e、f、g、h、i、j、c 乙 防止空氣中的水蒸氣進入,還吸收多余的氯氣 使液體順利滴下 干燥 ②①③ 75.0%
【解析】I.(1). E裝置中的儀器名稱是干燥管,故答案為:干燥管;
(2). 在B裝置中,濃鹽酸和MnO2反應生成氯化錳、氯氣和水,離子方程式為:MnO2+4H++2Cl=Mn2++Cl2↑+2H2O,故答案為:MnO2+4H++2Cl=Mn2++Cl2↑+2H2O;
(3). B裝置產生的氯氣中混有氯化氫和水蒸氣雜質,用D裝置除去HCl 雜質,C裝置除去水蒸氣雜質,由于氯化鋁易升華,產生的氯化鋁顆粒易堵塞導氣管,所以得到純凈的氯氣后在F裝置中和鋁反應制取氯化鋁而不用A裝置,根據信息可知氯化鋁遇水極易潮解并產生白色煙霧,所以最后必須用E裝置吸收多余的氯氣并可以防止空氣中的水蒸氣進入F裝置中,因此制備無水氯化鋁正確的連接順序為d、e、f、g、h、i、j、c,故答案為:d、e、f、g、h、i、j、c;
(4). 制備無水氯化鋁時,應先加熱圓底燒瓶產生氯氣,將裝置中的空氣排盡,以防止鋁粉被空氣中的氧氣氧化,故答案為:乙;
(5). 由上述分析可知,用E裝置可以吸收多余的氯氣并能防止空氣中的水蒸氣進入F裝置中使氯化鋁潮解,故答案為:防止空氣中的水蒸氣進入,還吸收多余的氯氣;
II. (6). 使用恒壓漏斗可以平衡漏斗內外壓強,使液體順利滴下,在洗滌后所得產物中加入少量無水MgSO4固體,目的是吸收產品中少量的水分,起到干燥的作用,故答案為:使液體順利滴下;干燥;
(7). 稀鹽酸洗滌可以除去氯化鋁雜質,再用5%Na2CO3溶液除去過量的鹽酸,最后用水洗滌除去剩余的5%Na2CO3,故答案為:②①③;
(8).加入苯的物質的量為50mL×0.88g/mL÷78g/mol=0.56mol,氯代叔丁烷的物質的量為10mL×1.84g/mL÷92.5g/mol=0.199mol,由反應方程式 +ClC(CH3)3
+ClC(CH3)3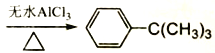 +HCl可知,加入的苯過量,則理論上生成叔丁基苯的質量為:0.199mol×134g/mol=26.66g,叔丁基苯的產率為:
+HCl可知,加入的苯過量,則理論上生成叔丁基苯的質量為:0.199mol×134g/mol=26.66g,叔丁基苯的產率為:![]() ×100%=75.0%,故答案為:75.0%。
×100%=75.0%,故答案為:75.0%。
【題型】實驗題
【結束】
9
【題目】一種含鋁、鋰、鈷的新型電子材料,生產中產生的廢料數量可觀,廢料中的鋁以金屬鋁箔的形式存在;鈷以Co2O3·CoO的形式存在,吸附在鋁箔的單面或雙面:鋰混雜于其中。(已知Co2O3的氧化性>Cl2的氧化性)從廢料中回收氧化鈷(CoO)的工藝流程如下:
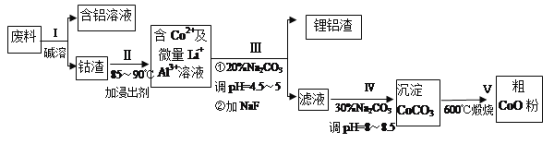
已知:①CoCO3的溶度積為:Ksp=1.0×10-13;
②溶液中離子濃度小于1.0×10-5mol/L時認為該離子沉淀完全。
(1)“堿溶”前通常將廢料粉碎,其目的是____________。
(2)過程I中采用NaOH溶液溶出廢料中的A1,反應的離子方程式為_________________。
(3)過程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出鈷。則浸出含鉆物質的反應化學方程式為 (產物中只有一種酸根) _______________________________________。在實驗室模擬工業生產時,也可用鹽酸浸出鈷,但實際工業生產中不用鹽酸,請分析不用鹽酸浸出鈷的主要原因______________________________________。
(4)過程III得到鋰鋁渣的主要成分是LiF和AI(OH)3,碳酸鈉溶液在產生 Al(OH)3時起重要作用,請寫出該反應的離子方程式__________________________________。
(5)將2.0×10-4 mol/LCoSO4與2.2×10-4mol/L的Na2CO3等體積混合,此時溶液中的Co2+的濃度為__________,Co2+是否沉淀完全? __________(填“是”或“否”)。
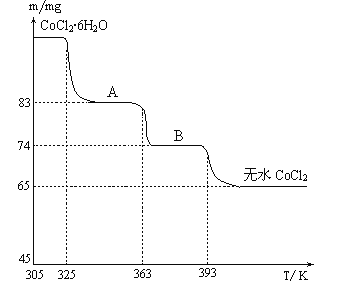
(6)CoO溶于鹽酸可得粉紅色的CoCl2溶液。CoCl2含結晶水數目不同而呈現不同顏色,利用藍色的無水CoCl2吸水變色這一性質可制成變色水泥和顯隱墨水。如圖是粉紅色的CoCl2·6H2O晶體受熱分解時,剩余固體質量隨溫度變化的曲線,物質B的化學式是____________________。
【答案】 略 略 略 略 略 略 略 略
【解析】(1). “堿溶”前通常將廢料粉碎,可以增大固體反應物的接觸面積,加快反應速率,故答案為:增大反應物接觸面積,加快反應速率;
(2). NaOH溶液和Al反應生成偏鋁酸鈉和氫氣,離子方程式為:2A1+2OH-+2H2O=2A1O2-+3H2↑,故答案為:2A1+2OH-+2H2O=2A1O2-+3H2↑;
(3). 廢料中鈷以Co2O3·CoO的形式存在,鈷的化合價為+2價和+3價,由流程圖可知,加入Na2S2O3溶液后,鈷全部變為+2價,說明Co3+氧化S2O32-,還原產物為Co2+,由產物中只有一種酸根離子可知氧化產物為SO42-,根據得失電子守恒和原子守恒,浸出含鈷物質的反應化學方程式為:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,由題中信息可知,Co2O3的氧化性>Cl2的氧化性,則Co2O3·CoO可氧化鹽酸產生Cl2,污染環境,所以實際工業生產中不用鹽酸浸出含鈷物質,故答案為:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O;Co2O3·CoO可氧化鹽酸產生Cl2,污染環境;
(4). 在過程III中加入碳酸鈉溶液,碳酸根離子和鋁離子發生雙水解反應生成氫氧化鋁沉淀,離子方程式為:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑,故答案為:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑;
(5). 將2.0×10-4mol/LCoSO4與2.2×10-4mol/L的Na2CO3等體積混合,Co2+與CO32-反應生成CoCO3,離子方程式為:Co2++ CO32-= CoCO3,由離子方程式可知,反應后的溶液中c(CO32-)=( 2.2×10-4-2.0×10-4)mol/L÷2=1×10-5mol/L,則反應后的溶液中c(Co2+)=![]() =1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案為:1.0×10-8mol/L;是;
=1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案為:1.0×10-8mol/L;是;
(6). 據圖可知,n(CoCl2)=65×10-3g÷130g/mol=5×10-4mol,B中含有水的物質的量為n(H2O)=(74-65)×10-3g÷18g/mol=5×10-4mol,則n(CoCl2): n(H2O)=1:1,則物質B為CoCl2·H2O,故答案為:CoCl2·H2O。


科目:高中化學 來源: 題型:
【題目】過碳酸鈉( Na2CO4)是一種很好的供氧劑,其與稀鹽酸反應的化學方程式為:2Na2CO4+4HCl=4NaCl+2CO2 +O2+2H2O.市售過碳酸鈉一般都含有碳酸鈉,為測定某過碳酸鈉樣品(只含Na2CO4和Na2CO3)的純度,某化學興趣小組采用以下兩種方案實施:
方案一:![]()
(1)操作①和③的名稱分別為
(2)上述操作中,使用到玻璃棒的有 __(填操作序號)。
(3)請簡述操作③的操作過程
方案二:按下圖安裝好實驗裝置,Q為一塑料氣袋,隨意取適量樣品于其中,打開分液漏斗活塞,將稀鹽酸滴入氣袋中至充分反應。

(4)為測定反應生成氣體的總體積,滴稀鹽酸前必須關閉 ,打開 (填“K1”、“K2”或“K3”)。導管a的作用是 。
(5)當上述反應停止后,使K1、K3處于關閉狀態,K2處于打開狀態,再緩緩打開Kl。 B中裝的固體試劑是 ,為何要緩緩打開K1? 。
(6)實驗結束時,量筒I中有xmL水,量筒Ⅱ中收集到了ymL氣體,則樣品中過碳酸鈉的質量分數是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應一定不能自發的是( )
A.2KClO3(s)═2KCl(s)+3O2(g)△H=﹣78.03kJmol﹣1 △S=+1110 Jmol﹣1K﹣1
B.CO(g)═C(s,石墨)+ ![]() O2(g)△H=+110.5kJmol﹣1△S=﹣89.36 Jmol﹣1K﹣1
O2(g)△H=+110.5kJmol﹣1△S=﹣89.36 Jmol﹣1K﹣1
C.4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H=﹣444.3kJmol﹣1△S=﹣280.1 J.mol﹣1K﹣1
D.NH4HCO3(s)+CH3COOH(aq)═CO2(g)+CH3COONH4(aq)+H2O(l)△H=+37.301kJmol﹣1△S=+184.05 Jmol﹣1K﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為測定石灰石樣品中碳酸鈣(合SiO2雜質)的含量。現利用如圖所示裝置進行實驗,充分反應后,測定裝置C中生成的BaCO3沉淀質量。下列說法正確的是
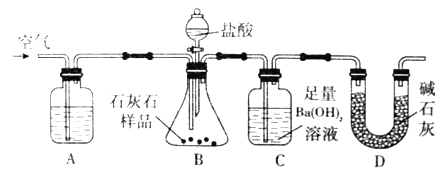
A. 裝置A中藥品應為濃硫酸
B. 在B~C之間應增添盛有飽和NaHCO3溶液的洗氣裝置,以除去氯化氫氣體
C. 只要測定裝置C在吸收CO2前后的質量差,也可以確定碳酸鈣的質量分數
D. 為了測得C中生成的沉淀質量,需經過過濾、洗滌、干燥、稱量等操作
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,Ag2SO4在水溶液中的沉淀溶解平衡曲線如圖所示,下列說法中不正確的是( ) 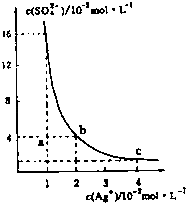
A.b點對應的Kap等于c點對應的Kap
B.采取蒸發溶劑的方法可以使溶液從a點變到b點
C.該溫度下,Ag2SO4的溶度積常數(Kap)為1.6×10﹣5(molL﹣1)2
D.0.02molL﹣1的AgNO3溶液與的0.2molL﹣1的Na2SO4溶液等體積混合不會生成沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】合成氨工業對國民經濟和社會發展具有重要的意義。對于一定體積密閉容器中的反應:N2(g)+3H2(g)![]() NH3(g)(正反應為放熱反應),673K、30MP下,n (NH3)和n (H2)隨時間t變化的關系如圖所示.下列敘述中,不正確的是()
NH3(g)(正反應為放熱反應),673K、30MP下,n (NH3)和n (H2)隨時間t變化的關系如圖所示.下列敘述中,不正確的是()

A. 點c處正反應速率比逆反應速率大 B. 點a的正反應速率比點b的正反應速率大
C. 氣體的平均摩爾質量:點b大于點a D. 混合氣體的密度:點b大于點a
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種含鋁、鋰、鈷的新型電子材料,生產中產生的廢料數量可觀,廢料中的鋁以金屬鋁箔的形式存在;鈷以Co2O3·CoO的形式存在,吸附在鋁箔的單面或雙面:鋰混雜于其中。(已知Co2O3的氧化性>Cl2的氧化性)從廢料中回收氧化鈷(CoO)的工藝流程如下:
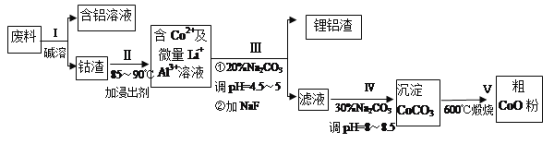
已知:①CoCO3的溶度積為:Ksp=1.0×10-13;
②溶液中離子濃度小于1.0×10-5mol/L時認為該離子沉淀完全。
(1)“堿溶”前通常將廢料粉碎,其目的是____________。
(2)過程I中采用NaOH溶液溶出廢料中的A1,反應的離子方程式為_________________。
(3)過程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出鈷。則浸出含鉆物質的反應化學方程式為 (產物中只有一種酸根) _______________________________________。在實驗室模擬工業生產時,也可用鹽酸浸出鈷,但實際工業生產中不用鹽酸,請分析不用鹽酸浸出鈷的主要原因______________________________________。
(4)過程III得到鋰鋁渣的主要成分是LiF和AI(OH)3,碳酸鈉溶液在產生 Al(OH)3時起重要作用,請寫出該反應的離子方程式__________________________________。
(5)將2.0×10-4 mol/LCoSO4與2.2×10-4mol/L的Na2CO3等體積混合,此時溶液中的Co2+的濃度為__________,Co2+是否沉淀完全? __________(填“是”或“否”)。
(6)CoO溶于鹽酸可得粉紅色的CoCl2溶液。CoCl2含結晶水數目不同而呈現不同顏色,利用藍色的無水CoCl2吸水變色這一性質可制成變色水泥和顯隱墨水。如圖是粉紅色的CoCl2·6H2O晶體受熱分解時,剩余固體質量隨溫度變化的曲線,物質B的化學式是____________________。

【答案】 略 略 略 略 略 略 略 略
【解析】(1). “堿溶”前通常將廢料粉碎,可以增大固體反應物的接觸面積,加快反應速率,故答案為:增大反應物接觸面積,加快反應速率;
(2). NaOH溶液和Al反應生成偏鋁酸鈉和氫氣,離子方程式為:2A1+2OH-+2H2O=2A1O2-+3H2↑,故答案為:2A1+2OH-+2H2O=2A1O2-+3H2↑;
(3). 廢料中鈷以Co2O3·CoO的形式存在,鈷的化合價為+2價和+3價,由流程圖可知,加入Na2S2O3溶液后,鈷全部變為+2價,說明Co3+氧化S2O32-,還原產物為Co2+,由產物中只有一種酸根離子可知氧化產物為SO42-,根據得失電子守恒和原子守恒,浸出含鈷物質的反應化學方程式為:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,由題中信息可知,Co2O3的氧化性>Cl2的氧化性,則Co2O3·CoO可氧化鹽酸產生Cl2,污染環境,所以實際工業生產中不用鹽酸浸出含鈷物質,故答案為:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O;Co2O3·CoO可氧化鹽酸產生Cl2,污染環境;
(4). 在過程III中加入碳酸鈉溶液,碳酸根離子和鋁離子發生雙水解反應生成氫氧化鋁沉淀,離子方程式為:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑,故答案為:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑;
(5). 將2.0×10-4mol/LCoSO4與2.2×10-4mol/L的Na2CO3等體積混合,Co2+與CO32-反應生成CoCO3,離子方程式為:Co2++ CO32-= CoCO3,由離子方程式可知,反應后的溶液中c(CO32-)=( 2.2×10-4-2.0×10-4)mol/L÷2=1×10-5mol/L,則反應后的溶液中c(Co2+)=![]() =1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案為:1.0×10-8mol/L;是;
=1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案為:1.0×10-8mol/L;是;
(6). 據圖可知,n(CoCl2)=65×10-3g÷130g/mol=5×10-4mol,B中含有水的物質的量為n(H2O)=(74-65)×10-3g÷18g/mol=5×10-4mol,則n(CoCl2): n(H2O)=1:1,則物質B為CoCl2·H2O,故答案為:CoCl2·H2O。
題型】綜合題
【結束】
10
【題目】砷元素廣泛存在于自然界,砷與其化合物被運用在農藥、除草劑、殺蟲劑等。
(1)砷的常見氧化物有As2O3和As2O5,其中As2O5熱穩定性差。根據圖1寫出As2O3轉化為As2O5的熱化學方程式__________________________________。
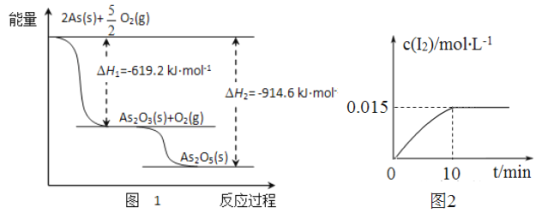
(2)砷酸鈉具有氧化性,298K時,在100mL燒杯中加入10mL0.1 mol/L Na3AsO4溶液、20mL0.1 mol/L KI溶液和20mL0.05mol/L硫酸溶液,發生下列反應:AsO43-(無色)+12(淺黃色)+H2O △H。測得溶液中c(I2)與時間(t)的關系如圖2所示(溶液體積變化忽略不計)。
①升高溫度,溶液中AsO43-的平衡轉化率減小,則該反應的△H________0(填“大于”“小于”或“等于”)。
②0~10min內,I的反應速率v(Iˉ)= ____________。
③下列情況表明上述可逆反應達到平衡狀態的是_______(填字母代號)。
a.c(AsO33-)+c(AsO42-)不再變化 b.溶液顏色保持不再變化
C.c(AsO33-)與c(AsO42-)的比值保持不再變化 d.I的生成速率等于I2的生成速率
④在該條件下,上述反應平衡常數的表達式K=______________。
(3)利用(2)中反應可測定含As2O3和As2O5的試樣中的各組分含量(所含雜質對測定無影響),過程如下:
①將試樣02000g溶于NaOH溶液,得到含AO33-和AsO43-的混合溶液。
②上述混合液用0.02500 mol·L-1的I2溶液滴定,用淀粉試液做指示劑,當________________,則滴定達到終點。重復滴定3次,平均消耗I2溶液40.00mL。則試樣中As2O5的質量分數是_________(保留四位有效數字)。若滴定終點時,仰視讀數,則所測結果_________ (填“偏低”,“偏高”,“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用 0.50molL﹣1NaOH標準液10.00mL,將未知濃度的鹽酸20.00mL恰好滴定至終點,下列說法正確的是( )
A.若選用酚酞作指示劑,終點時,液體恰好褪色
B.用量筒量取上述鹽酸
C.若滴定完畢,滴定管尖嘴懸有一滴液體,則所測的鹽酸濃度偏大
D.鹽酸的濃度為1.00 molL﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,H2SO3及其鈉鹽的溶液中,H2SO3、HSO3-、SO32-的物質的量分數(α)隨溶液pH變化關系如下圖所示,下列敘述錯誤的是( )
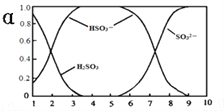
A. 溶液的pH=5時,硫元素的主要存在形式為HSO3-
B. 當溶液恰好呈中性時:c(Na+)>c(SO32-)+c(HSO3-)
C. 向pH=8的上述溶液中滴加少量澄清石灰水,![]() 的值增大
的值增大
D. 向pH=3的上述溶液中滴加少量稀硫酸,α(HSO3-)減小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com