
【題目】CH4、H2、C都是優質的能源物質,它們燃燒的熱化學方程式為:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH= -890.3 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
(1)在深海中存在一種甲烷細菌,它們依靠酶使甲烷與O2作用而產生的能量存活,甲烷細菌使1 mol甲烷生成CO2氣體與液態水,放出的能量____________(填“>”、“<”或“=”)890.3 kJ。
(2)甲烷與CO2可用于合成合成氣(主要成分是一氧化碳和氫氣):CH4+CO2= 2CO+2H2,1 g CH4完全反應可釋放15.46 kJ的熱量,則:

①上圖(所有物質均為氣態)能表示該反應過程中能量變化的是__________(填字母)。
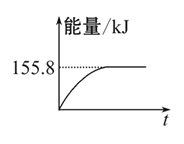
②若將物質的量均為1 mol的CH4與CO2充入某恒容密閉容器中,體系放出的熱量隨時間的變化如圖所示,則CH4的轉化率為 。
(3)C(s)與H2(g)不反應,所以C(s)+2H2(g)=CH4(g)的反應熱無法直接測量,但通過上述反應可求出C(s)+2H2(g)=CH4(g)的反應熱ΔH= 。
(4)目前對于上述三種物質的研究是燃料研究的重點,下列關于上述三種物質的研究方向中可行的是_____________(填字母)。
A.尋找優質催化劑,使CO2與H2O反應生成CH4與O2,并放出熱量
B.將固態碳合成為C60,以C60作為燃料
C.尋找優質催化劑,利用太陽能使大氣中的CO2與海底開采的CH4合成合成氣(CO、H2)
【答案】(1)= (2)①D ②63% (3)-74.8 kJ·mol-1 (4)C
【解析】
試題分析:(1)給定反應的反應熱只取決于反應物和生成物的多少和狀態,與中間過程無關,故甲烷細菌使1 mol甲烷生成CO2氣體與液態水,放出的能量仍等于890.3 kJ。
(2)①1 g CH4完全反應釋放15.46 kJ的熱量,則1 mol CH4完全反應放出熱量為247.36 kJ,故D圖符合題意;②CH4的轉化率=155.8/247.36 ×100%≈63%。
(3)根據蓋斯定律:②+③-①即得C(s)+2H2(g)=CH4(g) ΔH=-74.8 kJ·mol-1。
(4)A、已知CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1,則CO2與H2O反應生成CH4與O2的反應吸熱,錯誤;B、將固態碳合成為C60,以C60作為燃料,極不經濟合算,錯誤;C、利用太陽能使大氣中的CO2與海底開采的CH4合成合成氣(CO、H2)是合理的,正確;選C。


科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.增大壓強,化學反應速率增加
B.降低壓強,化學反應速率降低
C.改變壓強,化學反應速率可能不變
D.改變壓強引起了速率改變,平衡就會移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將標準狀況下的![]() LHCl(g)溶于1000g水中,得到的鹽酸密度為bg·cm-3,則該鹽酸的物質的量濃度是( )
LHCl(g)溶于1000g水中,得到的鹽酸密度為bg·cm-3,則該鹽酸的物質的量濃度是( )
A.![]() mo1·L-1 B.
mo1·L-1 B.![]() mol·L-1
mol·L-1
C.![]() mol·L-1 D.
mol·L-1 D.![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】標準狀況下有:①6.72L CH4,②3.01×1023個HCl分子,③13.6g H2S,④0. 2molNH3。下列對這四種氣體相關量的比較不正確的是
A. 體積:②>③>①>④ B. 密度:②>③>④>①
C. 質量:②>③>①>④ D. 氫原子數:①>④>③>②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】相同質量的烷烴、單烯烴、單炔烴,在空氣中完全燃燒生成二氧化碳和水,所需空氣量的比較中正確的是( )
A. 烷烴最少 B. 烯烴最少 C. 炔烴最少 D. 三者一樣多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在10mL 0.05mol/L的某金屬硫酸鹽M2(SO4)x溶液中,滴加15mL 0.10mol/L的BaCl2溶液,恰好完全反應生成硫酸鋇沉淀,該金屬的化合價為
A. +1 B. +2 C. +3 D. 不能確定
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com