
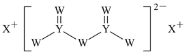
【題目】短周期主族元素W、X、Y、Z的原子序數(shù)依次增大,X的原子半徑是所有短周期主族元素中最大的,W的核外電子數(shù)與X、Z的最外層電子數(shù)之和相等,Y的原子序數(shù)是Z的最外層電子數(shù)的2倍,由W、X、Y三種元素形成的化合物M的結構如圖所示。下列敘述正確的是( )
A.元素非金屬性強弱的順序為W>Y>Z
B.Y單質(zhì)的熔點高于X單質(zhì)
C.W分別與X、Y、Z形成的二元化合物均只有一種
D.化合物M中W不都滿足8電子穩(wěn)定結構
【答案】B
【解析】
短周期主族元素W、X、Y、Z的原子序數(shù)依次增大,X的原子半徑是所有短周期主族元素中最大的,則X為Na元素;根據(jù)結構,W最外層有6個電子,原子序數(shù)小于11,則W為O元素;Y最外層有4個電子,原子序數(shù)大于11,則Y為Si元素;W的核外電子數(shù)為8,與X、Z的最外層電子數(shù)之和相等,則Z最外層有7個電子,只能為Cl元素;Y的原子序數(shù)是Z的最外層電子數(shù)的2倍,符合題意,據(jù)此分析解答。
根據(jù)上述分析,W為O元素,X為Na元素,Y為Si元素,Z為Cl元素。
A、同一周期,從左向右,非金屬性增強,同一主族,從上到下,非金屬性減弱,則元素非金屬性強弱的順序為Cl>Si,即Z>Y,故A錯誤;
B、硅為原子晶體,熔點高于鈉,即Y單質(zhì)的熔點高于X單質(zhì),故B正確;
C、O與Na能夠形成氧化鈉和過氧化鈉2種,故C錯誤;
D、根據(jù) ,陰離子帶2個單位負電荷,其中O都滿足8電子穩(wěn)定結構,故D錯誤;
,陰離子帶2個單位負電荷,其中O都滿足8電子穩(wěn)定結構,故D錯誤;
故選B。


科目:高中化學 來源: 題型:
【題目】已知:pKa=-lgKa。25℃時,幾種弱酸的pKa值如下表所示。下列說法正確的是
弱酸的化學式 | CH3COOH | HCOOH | H2SO3 |
pKa | 4.74 | 3.74 | 1.90 7.20 |
A. 向Na2SO3溶液中加入過量乙酸,反應生成SO2
B. 25℃時,pH=8的甲酸鈉溶液中,c( HCOOH)=9.9×10-7mol·L-1
C. 25℃時,某乙酸溶液pH=a,則等濃度的甲酸pH=a-1
D. 相同溫度下,等濃度的 HCOONa溶液比Na2SO3溶液的pH大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作能達到實驗目的的是
選項 | 實驗目的 | 實驗操作 |
A | 檢驗KIO3中的碘元素 | 取少量KIO3晶體溶于適量的蒸餾水,再加入硝酸酸化的AgNO3溶液 |
B | 檢驗石油裂解氣中的乙烯 | 將混合氣體通入足量酸性KMnO4溶液中 |
C | 比較HClO和CH3COOH的酸性強弱 | 室溫下,用pH計測定飽和的NaClO溶液和飽和的 |
D | 硅酸膠體的制備 | 向 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組為探究銅跟濃硫酸的反應,用如圖所示裝置進行有關實驗。請回答:

(1)寫出銅和濃硫酸反應的化學方程式:_____________。
(2)裝置D中試管口放置的棉花中浸有NaOH溶液,其作用是______。
(3)裝置B的作用是貯存多余的氣體。當D處有明顯的現(xiàn)象后,關閉旋塞K,移去酒精燈,但由于余熱的作用,A處仍有氣體產(chǎn)生,此時B中的現(xiàn)象是__,B中應放置的液體是____(填序號)。
A.水 B.酸性KMnO4溶液 C.濃溴水 D.飽和NaHSO3溶液
(4)取一定質(zhì)量的銅片和一定體積濃度為18.4 mol·L-1的濃硫酸放在圓底燒瓶中共熱,直到反應完畢,發(fā)現(xiàn)燒瓶中銅和硫酸都有剩余。若想使燒瓶中剩余的銅片溶解,可向燒瓶中加入下列試劑中的____(填序號)。
A.HNO3 B.NaNO3 C.NaHCO3 D.Na2CO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】數(shù)10億年來,地球上的物質(zhì)不斷變化,大氣的成分也發(fā)生了很大的變化。下表是原始大氣和目前空氣的主要成分:

用上表所涉及的分子填寫下列空白。
(1)含有10個電子的分子有(填化學式,下同)______________;
(2)由極性鍵構成的非極性分子有____________________;
(3)與H+可直接形成配位鍵的分子有________;
(4)沸點最高的物質(zhì)是________,用所學的知識解釋其沸點最高的原因________;
(5)分子中不含孤電子對的分子(稀有氣體除外)有________,它的立體構型為________;
(6)極易溶于水、且水溶液呈堿性的物質(zhì)的分子是________,它之所以極易溶于水是因為它的分子和水分子之間形成________;
(7)CO的結構可表示為O![]() C,與CO結構最相似的分子是________,這兩種結構相似的分子中,分子的極性________(填“相同”或“不相同”),CO分子中有一個鍵的形成與另外兩個鍵不同,它叫________。
C,與CO結構最相似的分子是________,這兩種結構相似的分子中,分子的極性________(填“相同”或“不相同”),CO分子中有一個鍵的形成與另外兩個鍵不同,它叫________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據(jù)雜化軌道理論和價電子對互斥模型判斷,下列分子或者離子的中心原子雜化方式及空間構型正確的是( )
選項 | 分子或離子 | 中心原子雜化方式 | 價電子對互斥模型 | 分子或離子的立體構型 |
A. | SO2 | sp | 直線形 | 直線形 |
B. | HCHO | sp2 | 平面三角形 | 三角錐形 |
C. | NF3 | sp2 | 四面體形 | 平面三角形 |
D. |
| sp3 | 正四面體形 | 正四面體形 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化氯(ClO2)是一種優(yōu)良的消毒劑,熔點為-59 ℃,沸點為 11 ℃,濃度過高時易發(fā)生分解,甚至爆炸。二氧化氯具有強刺激性和腐蝕性。某課外興趣小組通過氯氣與 NaClO2溶液反應來制取少量ClO2,裝置如圖所示:
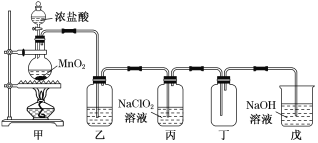
(1)甲裝置中圓底燒瓶內(nèi)發(fā)生反應的化學方程式是______________________________________。
(2)Cl-存在時會催化 ClO2的生成,若無乙裝置,則丙裝置內(nèi)產(chǎn)生 ClO2的速率明顯加快。乙裝置中試劑瓶內(nèi)的液體是__________。實驗過程中常需通入適量的 N2稀釋 ClO2,其目的是_____________________________________________。
(3)丙裝置中發(fā)生的反應為:Cl2+2NaClO2===2ClO2↑+2NaCl 。
下列有關該實驗的說法正確的是________________
A. 可用微熱法檢查實驗裝置的氣密性
B. 如果乙裝置是盛有濃硫酸,更有利于實驗安全
C. 若甲中足量MnO2與含0.4 molHCl的濃鹽酸反應,則丙中可制得0.2molClO2
D. 實驗過程甲裝置要緩緩加熱,不宜強熱
(4)戊裝置燒杯中NaOH 溶液,其作用是_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用含碳化合物合成燃料是解決能源危機的重要方法,已知CO(g)+2H2(g)![]() CH3OH(g)反應過程中的能量變化情況如圖所示,曲線Ⅰ和曲線Ⅱ分別表示不使用催化劑和使用催化劑的兩種情況。下列判斷正確的是 ( )
CH3OH(g)反應過程中的能量變化情況如圖所示,曲線Ⅰ和曲線Ⅱ分別表示不使用催化劑和使用催化劑的兩種情況。下列判斷正確的是 ( )

A. 該反應的ΔH=+91 kJ·mol-1
B. 加入催化劑,該反應的ΔH變小
C. 反應物的總能量小于生成物的總能量
D. 如果該反應生成液態(tài)CH3OH,則ΔH減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖甲表示葉綠體的結構,圖乙表示暗反應過程。請據(jù)圖回答下列問題:

(l)葉綠體中的色素分布于圖甲中的____ (填序號);四種色素能在濾紙條上分離,是因為____。
(2)葉綠體進行光合作用時,ATP的移動方向是從____到____(填序號),合成ATP所需的能量來自____。
(3)在光照強度、溫度和CO2濃度三種環(huán)境因素中,能直接影響圖乙所示過程的是 _________。若突然降低光照強度,則在短時間內(nèi)葉綠體中C3和C5的含量變化分別是 _________、________。
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com