
【題目】在2 L容器中發生3A+B=2C的反應,最初加入的A、B都是4 mol,10 s 內A的反應速率為0.12 mol/(L·s),10 s后容器內B的物質的量濃度為 ( )
A. 1.6 mol/L B. 1.4 mol/L C. 3.2 mol/L D. 1.8 mol/L
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】對于可逆反應mA(g)十nB(g)![]() pC(g)十qD(g),若其它條件都不變,探究催化劑對反應的影響,可得到如下兩種v-t圖象。下列判斷正確的是
pC(g)十qD(g),若其它條件都不變,探究催化劑對反應的影響,可得到如下兩種v-t圖象。下列判斷正確的是

A.b1>b2 ,t1>t2
B.兩圖中陰影部分面積一定相等
C.A的平衡轉化率(II)大于(Ⅰ)中A的轉化率
D.若m+n<p+q,則壓強變化對正反應速率的影響程度比逆反應速率影響程度大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有Na2CO3和NaHCO3兩種白色固體物質欲探究Na2CO3和NaHCO3穩定性的相對強弱,兩同學分別設計了以下兩組裝置:
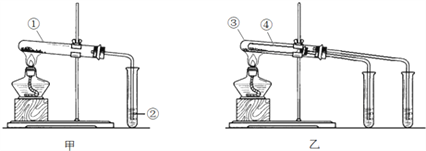
請回答:
(1)如甲圖所示,分別用Na2CO3和NaHCO3做實驗,試管②中的試劑是______________(填字母).
a.稀HSO4 b.NaOH溶液 c.Ca(OH)2溶液
(2)如乙圖所示,試管④中裝入的固體應該是_________(填化學式).
(3)通過上述實驗,得出的結論是:Na2CO3比NaHCO3的穩定性_______(填“強”或“弱”).
(4)欲鑒別兩種物質的溶液可選用的試劑是________________
(5)等物質的量濃度兩種物質的溶液與同濃度的鹽酸反應,反應速率快的是_________(填化學式)
(6)除去碳酸鈉粉末中混入的碳酸氫鈉雜質用______方法,化學方程式_____________________________
(7)除去碳酸氫鈉溶液中混入的硅酸鈉雜質的試劑是______,所采用的分離方法______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列電離方程式正確的是 ( )
A. NaHS 溶于水: NaHS=Na+ + HS- HS- + H2O![]() H3O+ + S2-
H3O+ + S2-
B. (NH4)2SO4溶于水: (NH4)2SO4![]() 2NH4+ + SO42-
2NH4+ + SO42-
C. 磷酸溶于水中: H3PO4![]() 3H+ + PO43-
3H+ + PO43-
D. Al(OH)3的電離: Al(OH)3![]() Al3+ + 3OH-
Al3+ + 3OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】萜類化合物廣泛存在于動植物體內,關于下列萜類化合物的說法正確的是

A. a和b都屬于芳香族化合物
B. a、b和c均能使酸性KMnO4溶液褪色
C. a和c分子中所有碳原子均處于同一平面上
D. b和c均能與新制的Cu(OH)2反應生成紅色沉淀
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[化學—選修3:物質結構與性質]目前半導體生產正在進行一場“銅芯片”革命:在硅芯片上用銅代替鋁布線。古老的金屬銅在現代科技應用上取得了突破。用黃銅礦(主要成分為CuFeS2)生產粗銅,其反應原理如下:
![]()
(1)基態銅原子的價電子排布式為____________,硫、氧元素相比,第一電離能較大的元素是________(填元素符號)。
(2)反應①、②中均生成有相同的氣體分子,該分子的中心原子雜化類型是_________,其立體結構是________,與該分子互為等電子體的單質氣體的化學式是 。
(3)某學生用硫酸銅溶液與氨水做了一組實驗:CuSO4溶液![]() 藍色沉淀
藍色沉淀![]() 沉淀溶解,得到深藍色透明溶液。生成藍色沉淀溶于氨水的離子方程式為 ;
沉淀溶解,得到深藍色透明溶液。生成藍色沉淀溶于氨水的離子方程式為 ;
(4)銅是第四周期最重要的過渡元素之一,其單質及化合物具有廣泛用途。銅晶體中銅原子堆積模型為________;銅的某種氧化物晶胞結構如圖所示,若該晶體的密度為d g/cm3,阿伏加德羅常數的值為NA,則該晶胞中銅原子與氧原子之間的距離為________pm。(用含d和NA的式子表示)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以NA 表示阿伏加德羅常數,下列說法正確的是
A. T℃時,1LpH=6純水中,含10-8NA個OH-
B. 15.6gNa2O2 與過量CO2反應時,轉移的電子數為0.4NA
C. pH=1的H3PO4溶液中含有0.1NA個H+
D. 1molCO和N2混合氣體中含有的質子數是14NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在4個容積均為1 L的恒容容器中分別進行反應(各容器中A都足量)A(s)+B(g)![]() C(g)+D(g) ΔH =+100 kJ·mol-1,某時刻測得部分數據如下表:
C(g)+D(g) ΔH =+100 kJ·mol-1,某時刻測得部分數據如下表:
容器編號 | n(B)/mol | n(C)/mol | n(D)/mol | 反應時間/min | 反應速率 |
Ⅰ | 0.06 | 0.60 | 0.10 | t1 | v(正)=v(逆) |
Ⅱ | 0.12 | 1.20 | 0.20 | t2 | |
Ⅲ | 0.32 | 1.0 | 0 | 0 | |
Ⅳ | 0.12 | 0.30 | v(正)=v(逆) |
下列說法正確的是
A.容器Ⅰ中平均反應速率v(B)=0.04/t1 mol·L-1·min-1
B.t2時容器Ⅱ中v(正)>v(逆)
C.容器Ⅲ
D.容器Ⅳ中c(D)= 0.4 mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質中,所含原子數最多的是( )
A.8g O2
B.0.3mol NaCl
C.標準狀況下4.48L CH4
D.含有3.01×1022個氧原子的H2SO4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com