
【題目】可以將反應Zn+Br2= ZnBr2設計成蓄電池,下列4個電極反應:
①Br2+ 2e-= 2Br- ②2Br-- 2e-= Br2③Zn – 2e-= Zn2+④Zn2++ 2e-= Zn
其中表示充電時的陽極反應和放電時的負極反應的分別是
A.④和①B.②和①C.③和①D.②和③
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】下列內容與結論不對應的是
選項 | 內容 | 結論 |
A | H2O(g)變成H2O(l) | 該過程的ΔS<0 |
B | 硝酸銨溶于水可自發進行 | 因為ΔS>0 |
C | 一個反應的ΔH>0、ΔS>0 | 該反應一定不能自發進行 |
D | H2(g)+F2(g)=2HF(g) ΔH=-271 kJ·mol-1、 ΔS=8 J·mol-1·K-1 | 該反應在任何溫度下均可自發進行 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下一系列反應,最終產物為草酸(乙二酸)。
B![]() C
C![]() D
D![]() E
E![]() F
F![]()
![]()
已知B為某一溴代物。
(1)推測用字母代表的化合物的結構式:C_______________。
(2)E→F的化學方程式是______________________。
(3)寫出E和草酸在一定條件下生成高分子化合物的化學方程式_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知土壤膠體帶負電,在土壤里施用含氮量相等的下列肥料,肥效較差的是( )
A.(NH4)2SO4
B.NH4HCO3
C.NH4NO3
D.NH4Cl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列由事實得出的結論錯誤的是( )
A.維勒用無機物合成尿素,突破了無機物與有機物的界限
B.門捷列夫在前人工作的基礎上總結出了元素周期律,表明科學研究既要繼承又要創新
C.C60是英國和美國化學家共同發現的,體現了國際科技合作的重要性
D.科恩和波普爾因理論化學方面的貢獻獲諾貝爾化學獎,意味著化學已成為以理論研究為主的學科
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】R,X,Y,Z,A是短周期主族元素,它們在元素周期表中的相對位置如圖所示.X原子最外層電子數等于電子層數的3倍.下列推斷正確的是( ) 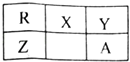
A.最簡單氣態氫化物的熱穩定性由強到弱的排序:Z,R,X,Y
B.原子半徑由小到大的排序:Z,A,Y,X
C.最高價氧化物的水化物酸性由弱到強的排Z,R,A
D.RY3 , A2X,ZA5分子中每個原子最外層都達到8 電子結構
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溴及其化合物在生活和生產中都有重要應用,自然界中的溴絕大多數都分布在海洋中,從海水中提取溴是溴的最主要來源.
(1)海水中溴的主要存在形式是(填字母代號).
A.Br﹣
B.Br2
C.BrO﹣
D.BrO3﹣
(2)實驗室若要直接濃縮海水時,下列儀器肯定不需要的是 . 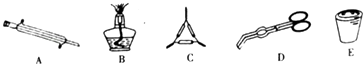
(3)工業上常將海水中的溴轉化為單質,再用熱空氣吹出溴,采用以下兩種方式吸收:
方法I、二氧化硫水溶液吸收,該方法中二氧化硫是(填“氧化劑”或“還原劑”).
方法II、純堿溶液吸收法,生成物之一是NaBrO3 , 寫出反應的化學方程式 .
(4)現有一份吸收了溴的無色溶液X,假定吸收劑和溴完全反應,通過下列實驗可探究X是采用哪種方法吸收溴的(已知pH試紙遇酸變紅,遇堿變藍).
①用玻璃棒蘸取少量X點在pH試紙上,試紙呈色,證明X是采用方法I吸收的;另取少量X,依次加入稀硫酸和四氯化碳,充分振蕩后靜置,觀察到溶液分層,(填“上”或“下”)層呈橙紅色,有關反應的離子方程式為 , 證明X是采用方法II吸收的.
②請再設計一個實驗驗證X是采用方法I吸收溴所得的溶液 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是氧族部分元素的相關性質。
元素 性質 | 8O | 16S | 34Se | 52Te |
主要化合價 | -2 | -2、+4、+6 | -2、+4、+6 | |
原子半徑 | 逐漸增大 | |||
單質與H2 反應情況 | 點燃時 易化合 | 加熱 化合 | 加熱 難化合 | 不能 直接化合 |
請回答下列問題:
(1)硒在周期表中位置____。
(2)碲的化合價可能有____。
(3)硫、硒、碲的氫化物水溶液的酸性由強至弱的順序是__________(填化學式)。
(4)氫硒酸有較強的____(填“氧化性”或“還原性”),因此放在空氣中易變質,其可能發生的化學方程式為_____________。
(5)氧族元素單質與H2反應過程中的焓變如圖所示,其中a、b、c、d分別表示氧族中某一元素的單質。則b代表___,d代表___(均寫單質名稱)。
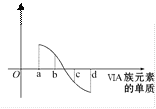
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以玉米淀粉為原料生產燃料乙醇的生產過程可由下圖表示:
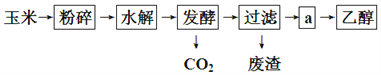
(1)乙醇分子中所含的官能團的名稱為:__________________;
(2)過濾后得到a的主要成分為葡萄糖和乙醇,步驟a的操作是__________;
A.蒸發 B.萃取 C.蒸餾 D.分液
(3)生產過程中為了檢驗水解是否開始,可使用的試劑是______________;
(4)已知1g乙醇完全燃燒放出的熱量為29.7kJ,請據此寫出乙醇燃燒的熱化學方程式:_______。
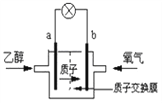
(5)為了充分利用乙醇的能量,科學家還把乙醇設計成燃料電池,如圖,用磺酸類質子溶劑,在高溫供電時,乙醇電池效率高且更安全。請判斷,該電池的a極為電池的_______極(填“正”或“負”),b極的電極反應式為:____________________________,電池工作時,若有1mol乙醇被氧化,則轉移的電子為____________mol。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com