

 BaCO3(s)+SO42ŻŁ(aq)
BaCO3(s)+SO42ŻŁ(aq) BaCO3Ż©sŻ®+SO42ŻŁ
BaCO3Ż©sŻ®+SO42ŻŁ =
= =4.0Ī┴10ŻŁ2 Ż©2ĘųŻ¼Ųõųą┴ą╩ĮĪó┤·╚ļöĄųĄĖ„1ĘųŻ®
=4.0Ī┴10ŻŁ2 Ż©2ĘųŻ¼Ųõųą┴ą╩ĮĪó┤·╚ļöĄųĄĖ„1ĘųŻ® Ba2+(aq) + SO42ŻŁ(aq) Ż©1ĘųŻ®Ż¼╝ė╚ļ’¢║═╠╝╦ßŌc╚▄ę║Ż¼CO32ŻŁØŌČ╚į÷┤¾Ż¼╩╣Qc(BaCO3)=c(Ba2+)Ī┴c(CO32ŻŁ)ŻŠKsp(BaCO3) Ż¼ą╬│╔╠╝╦ßõ^Ą─▀^’¢║═╚▄ę║Ż¼ę“┤╦╬÷│÷BaCO3│┴ĄĒŻ©1ĘųŻ®Ż¼c(Ba2+)£pąĪŻ¼╩╣BaSO4│┴ĄĒŽ“╚▄ĮŌĘĮŽ“ęŲäėŻ¼BaSO4▐D╗»×ķBaCO3Ż©1ĘųŻ®ĪŻŻ©║Ž└Ē╝┤ĮoĘųŻ®
Ba2+(aq) + SO42ŻŁ(aq) Ż©1ĘųŻ®Ż¼╝ė╚ļ’¢║═╠╝╦ßŌc╚▄ę║Ż¼CO32ŻŁØŌČ╚į÷┤¾Ż¼╩╣Qc(BaCO3)=c(Ba2+)Ī┴c(CO32ŻŁ)ŻŠKsp(BaCO3) Ż¼ą╬│╔╠╝╦ßõ^Ą─▀^’¢║═╚▄ę║Ż¼ę“┤╦╬÷│÷BaCO3│┴ĄĒŻ©1ĘųŻ®Ż¼c(Ba2+)£pąĪŻ¼╩╣BaSO4│┴ĄĒŽ“╚▄ĮŌĘĮŽ“ęŲäėŻ¼BaSO4▐D╗»×ķBaCO3Ż©1ĘųŻ®ĪŻŻ©║Ž└Ē╝┤ĮoĘųŻ® BaCO3Ż©sŻ®+SO42ŻŁ
BaCO3Ż©sŻ®+SO42ŻŁ =
=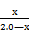 =4.0Ī┴10ŻŁ2 Ż©2ĘųŻ¼Ųõųą┴ą╩ĮĪó┤·╚ļöĄųĄĖ„1ĘųŻ®
=4.0Ī┴10ŻŁ2 Ż©2ĘųŻ¼Ųõųą┴ą╩ĮĪó┤·╚ļöĄųĄĖ„1ĘųŻ® Ba2+(aq) + SO42ŻŁ(aq)Ż¼╝ė╚ļ’¢║═╠╝╦ßŌc╚▄ę║─▄į÷┤¾CO32ŻŁØŌČ╚Ż¼╩╣Qc(BaCO3)=c(Ba2+)Ī┴c(CO32ŻŁ)ŻŠKsp(BaCO3) Ż¼ą╬│╔╠╝╦ßõ^Ą─▀^’¢║═╚▄ę║Ż¼ę“┤╦╬÷│÷BaCO3│┴ĄĒŻ¼įņ│╔c(Ba2+)£pąĪŻ¼╩╣BaSO4│┴ĄĒŽ“╚▄ĮŌĘĮŽ“ęŲäėŻ¼BaSO4▐D╗»×ķBaCO3ĪŻ
Ba2+(aq) + SO42ŻŁ(aq)Ż¼╝ė╚ļ’¢║═╠╝╦ßŌc╚▄ę║─▄į÷┤¾CO32ŻŁØŌČ╚Ż¼╩╣Qc(BaCO3)=c(Ba2+)Ī┴c(CO32ŻŁ)ŻŠKsp(BaCO3) Ż¼ą╬│╔╠╝╦ßõ^Ą─▀^’¢║═╚▄ę║Ż¼ę“┤╦╬÷│÷BaCO3│┴ĄĒŻ¼įņ│╔c(Ba2+)£pąĪŻ¼╩╣BaSO4│┴ĄĒŽ“╚▄ĮŌĘĮŽ“ęŲäėŻ¼BaSO4▐D╗»×ķBaCO3ĪŻ

 ┐┌╦ŃŅ}┐©╝ėæ¬ė├Ņ}╝»ė¢ŽĄ┴ą┤░Ė
┐┌╦ŃŅ}┐©╝ėæ¬ė├Ņ}╝»ė¢ŽĄ┴ą┤░Ė ŠC║Žūį£yŽĄ┴ą┤░Ė
ŠC║Žūį£yŽĄ┴ą┤░Ė
| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║╠Ņ┐šŅ}
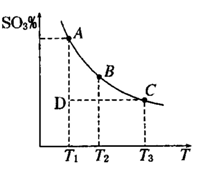
 2SO3Ż©gŻ®Ż¼╗ņ║Ž¾wŽĄųąSO3 Ą─░┘Ęų║¼┴┐║═£žČ╚Ą─ĻPŽĄ╚ńŽ┬łD╦∙╩ŠŻ©Ū·ŠĆ╔Ž╚╬║╬ę╗³cČ╝▒Ē╩ŠŲĮ║ŌĀŅæBŻ®Ż«Ė∙ō■łD╩Š╗ž┤Ž┬┴ąå¢Ņ}Ż¼
2SO3Ż©gŻ®Ż¼╗ņ║Ž¾wŽĄųąSO3 Ą─░┘Ęų║¼┴┐║═£žČ╚Ą─ĻPŽĄ╚ńŽ┬łD╦∙╩ŠŻ©Ū·ŠĆ╔Ž╚╬║╬ę╗³cČ╝▒Ē╩ŠŲĮ║ŌĀŅæBŻ®Ż«Ė∙ō■łD╩Š╗ž┤Ž┬┴ąå¢Ņ}Ż¼ 2SO3Ż©gŻ®Ą─Ī„H 0
2SO3Ż©gŻ®Ą─Ī„H 0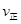
 Ż©╠ŅĪ░>Ī▒Ī░<Ī▒╗“Ī░=Ī▒Ż®
Ż©╠ŅĪ░>Ī▒Ī░<Ī▒╗“Ī░=Ī▒Ż®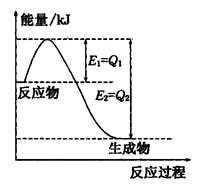
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║ėŗ╦ŃŅ}

 CH3OH(g) Ī„HŻĮQkJ/mol
CH3OH(g) Ī„HŻĮQkJ/mol ( CH3OH)┼cĘ┤欣žČ╚TĄ─ĻPŽĄŪ·ŠĆ╚ńłD2╦∙╩ŠŻ¼ät╔Ž╩÷Ę┤æ¬Ą─Q_____0Ż©╠ŅĪ░ŻŠĪ▒Ī░Ż╝Ī▒╗“Ī░ŻĮĪ▒Ż®Ż╗
( CH3OH)┼cĘ┤欣žČ╚TĄ─ĻPŽĄŪ·ŠĆ╚ńłD2╦∙╩ŠŻ¼ät╔Ž╩÷Ę┤æ¬Ą─Q_____0Ż©╠ŅĪ░ŻŠĪ▒Ī░Ż╝Ī▒╗“Ī░ŻĮĪ▒Ż®Ż╗▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║╠Ņ┐šŅ}
 2FeŻ©sŻ®+3CO2Ż©gŻ® Ī„H= ŻŁ28Ż«5 kJĪżŻ©molŻŁ1
2FeŻ©sŻ®+3CO2Ż©gŻ® Ī„H= ŻŁ28Ż«5 kJĪżŻ©molŻŁ1 2COŻ©gŻ® Ī„H=" +" 172Ż«5 kJĪżmolŻŁ1
2COŻ©gŻ® Ī„H=" +" 172Ż«5 kJĪżmolŻŁ1 2FeŻ©sŻ®+3COŻ©gŻ® Ī„H= kJĪżmolŻŁ1
2FeŻ©sŻ®+3COŻ©gŻ® Ī„H= kJĪżmolŻŁ1 2FeŻ©sŻ®+3CO2Ż©gŻ® Ī„H=ŻŁ28Ż«5 kJĪżmolŻŁ1Ą─ŲĮ║Ō│ŻöĄ▒Ē▀_╩ĮK= Ż¼£žČ╚ĮĄĄ═║¾Ż¼KųĄ Ż«Ż©╠ŅĪ░į÷┤¾Ī▒ĪóĪ░▓╗ūāĪ▒╗“Ī░£pąĪĪ▒Ż®ĪŻ
2FeŻ©sŻ®+3CO2Ż©gŻ® Ī„H=ŻŁ28Ż«5 kJĪżmolŻŁ1Ą─ŲĮ║Ō│ŻöĄ▒Ē▀_╩ĮK= Ż¼£žČ╚ĮĄĄ═║¾Ż¼KųĄ Ż«Ż©╠ŅĪ░į÷┤¾Ī▒ĪóĪ░▓╗ūāĪ▒╗“Ī░£pąĪĪ▒Ż®ĪŻ| | Fe2 O3 | CO | Fe | CO2 |
| ╝ū╚▌Ų„ | 1Ż«0 mol | 1Ż«0 mol | 1Ż«0 mol | 1Ż«0 mol |
| ęę╚▌Ų„ | 1Ż«0 mol | 2Ż«0 mol | 1Ż«0 mol | 1Ż«0 mol |

▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║╠Ņ┐šŅ}
 2SO3(g) ?H=-196Ż«6 kJĪżmol-1
2SO3(g) ?H=-196Ż«6 kJĪżmol-1 2NO2(g) ?H=-113Ż«0 kJĪżmol-1
2NO2(g) ?H=-113Ż«0 kJĪżmol-1  SO3(g)+NO(g)Ą─?H= kJĪżmol-1ĪŻ
SO3(g)+NO(g)Ą─?H= kJĪżmol-1ĪŻ

 CH3OH(g)ĪŻCOį┌▓╗═¼£žČ╚Ž┬Ą─ŲĮ║Ō▐D╗»┬╩┼cē║ÅŖĄ─ĻPŽĄ╚ń╔ŽłDŻ©ė꯮╦∙╩ŠĪŻįōĘ┤æ¬?H 0Ż©╠ŅĪ░>Ī▒╗“Ī░ <Ī▒Ż®ĪŻ
CH3OH(g)ĪŻCOį┌▓╗═¼£žČ╚Ž┬Ą─ŲĮ║Ō▐D╗»┬╩┼cē║ÅŖĄ─ĻPŽĄ╚ń╔ŽłDŻ©ė꯮╦∙╩ŠĪŻįōĘ┤æ¬?H 0Ż©╠ŅĪ░>Ī▒╗“Ī░ <Ī▒Ż®ĪŻ ▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║ėŗ╦ŃŅ}
 2FeŻ©sŻ®+3CO2Ż©gŻ®Ż¼šł╗ž┤Ž┬┴ąå¢Ņ}Ż║
2FeŻ©sŻ®+3CO2Ż©gŻ®Ż¼šł╗ž┤Ž┬┴ąå¢Ņ}Ż║| AŻ«├▄ķ]╚▌Ų„ųą┐éē║ÅŖ▓╗ūā |
| BŻ«├▄ķ]╚▌Ų„ųą╗ņ║ŽÜŌ¾wĄ─ŲĮŠ∙─”Ā¢┘|┴┐▓╗ūā |
| CŻ«├▄ķ]╚▌Ų„ųą╗ņ║ŽÜŌ¾wĄ─├▄Č╚▓╗ūā |
| DŻ«cŻ©COŻ®= cŻ©CO2Ż® |
 2Fe3O4Ż©sŻ®+CO2Ż©gŻ® Ī„H="©C47" kJ/mol
2Fe3O4Ż©sŻ®+CO2Ż©gŻ® Ī„H="©C47" kJ/mol 3FeOŻ©sŻ®+CO2Ż©gŻ® Ī„H=" +19" kJ/mol
3FeOŻ©sŻ®+CO2Ż©gŻ® Ī„H=" +19" kJ/mol FeŻ©sŻ®+CO2Ż©gŻ® Ī„H="©C11" kJ/mol
FeŻ©sŻ®+CO2Ż©gŻ® Ī„H="©C11" kJ/mol 2FeŻ©sŻ®+3CO2Ż©gŻ®Ą─Ī„H= ĪŻ
2FeŻ©sŻ®+3CO2Ż©gŻ®Ą─Ī„H= ĪŻ| £žČ╚ | 250Īµ Ī½ 600Īµ Ī½ 1000Īµ Ī½ 2000Īµ |
| ų„ę¬│╔Ęų | Fe2O3 Fe3O4 FeO Fe |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║ėŗ╦ŃŅ}
 CH3CH2OH(g) + H2O(g) Ī„H =" Ī¬256.1" kJĪżmolŻŁ1
CH3CH2OH(g) + H2O(g) Ī„H =" Ī¬256.1" kJĪżmolŻŁ1 CO2(g)+H2(g) Ī„H=" Ī¬41.2" kJĪżmolŻŁ1
CO2(g)+H2(g) Ī„H=" Ī¬41.2" kJĪżmolŻŁ1 CH3CH2OH(g) +3H2O(g) Ī„H = ĪŻ
CH3CH2OH(g) +3H2O(g) Ī„H = ĪŻ
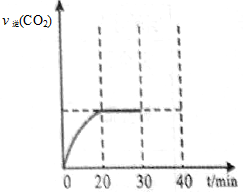
 N2 (g) + CO2 (g)ĪŻ─│蹊┐ąĪĮMŽ“─│├▄ķ]╚▌Ų„ųą╝ė╚╦ūŃ┴┐Ą─╗Ņąį╠┐║═NOŻ¼║Ń£ž( T1Īµ)Śl╝■Ž┬Ę┤æ¬Ż¼Ę┤æ¬▀MąąĄĮ▓╗═¼Ģrķg£yĄ├Ė„╬’┘|Ą─ØŌČ╚╚ńŽ┬Ż║
N2 (g) + CO2 (g)ĪŻ─│蹊┐ąĪĮMŽ“─│├▄ķ]╚▌Ų„ųą╝ė╚╦ūŃ┴┐Ą─╗Ņąį╠┐║═NOŻ¼║Ń£ž( T1Īµ)Śl╝■Ž┬Ę┤æ¬Ż¼Ę┤æ¬▀MąąĄĮ▓╗═¼Ģrķg£yĄ├Ė„╬’┘|Ą─ØŌČ╚╚ńŽ┬Ż║| ĪĪ ØŌČ╚/mol?LŻŁ1 Ģrķg/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║╠Ņ┐šŅ}


| ╚▌ Ų„ | ╝ū | ęę | ▒¹ |
| Ę┤æ¬╬’═Č╚ļ┴┐ | 1 mol NO2 1 mol CO | 2 mol NO 2 mol CO2 | 1 mol NO2Īó1 mol CO 1 mol NOĪó1 mol CO2 |
| ŲĮ║ŌĢrc(NO) /molĪżL-1 | 1.5 | 3 | m |
| ─▄┴┐ūā╗» | Ę┼│÷a kJ | ╬³╩šb kJ | Ę┼│÷c kJ |
| CO╗“NOĄ─▐D╗»┬╩ | ”┴1 | ”┴2 | ”┴3 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║▓╗įö Ņ}ą═Ż║å╬▀xŅ}
| AŻ«N2H4Ż©gŻ®+2H2O2Ż©lŻ®= N2Ż©gŻ®+4H2OŻ©lŻ®”żHŻĮŻ½817.63 kJĪżmolŻŁ1 |
| BŻ«N2H4Ż©gŻ®+2H2O2Ż©lŻ®= N2Ż©gŻ®+4H2OŻ©gŻ®”żHŻĮŻŁ641.63 kJĪżmolŻŁ1 |
| CŻ«N2H4Ż©gŻ®+2H2O2Ż©lŻ®= N2Ż©gŻ®+4H2OŻ©lŻ®”żHŻĮŻŁ641.63 kJĪżmolŻŁ1 |
| DŻ«N2H4Ż©gŻ®+2H2O2Ż©lŻ®= N2Ż©gŻ®+4H2OŻ©gŻ®”żHŻĮŻŁ817.63 kJĪżmolŻŁ1 |
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com