
下列實驗不能達到預期實驗目的的是( )
| 序號 | 實驗內容 | 實驗目的 |
| A | 向盛有10滴0.1 mol·L-1 AgNO3溶液的試管中滴加0.1 mol·L-1 NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol·L-1 Na2S溶液 | 證明AgCl能轉化為溶解度更小的Ag2S |
| B | 向2 mL甲苯中加入3滴酸性KMnO4溶液,振蕩;向2 mL苯中加入3滴酸性KMnO4溶液,振蕩 | 證明與苯環相連的甲基易被 氧化 |
| C | 向Na2SiO3溶液中通入CO2 | 證明碳酸的酸性比硅酸強 |
| D | 向淀粉溶液中加入稀硫酸,水浴加熱,一段時間后,再加入新制的氫氧化銅懸濁液并加熱 | 驗證淀粉已水解 |
 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案科目:高中化學 來源: 題型:實驗題
某研究性學習小組為測定NH3分子中氮、氫原子個數比,設計如下實驗流程:
實驗時,先用制得的氨氣排盡洗氣瓶前所有裝置中的空氣,再連接洗氣瓶和氣體收集裝置,立即加熱氧化銅。
下圖A、B、C為該小組制取氨氣時可能用到的裝置,D為盛有濃硫酸的洗氣瓶。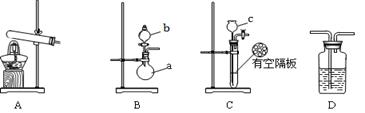
請回答下列問題:
(1)寫出儀器的名稱:a ,b 。
(2)硬質玻璃管中發生的反應方程式是 ,反應過程中硬質玻璃管的現象是 。
(3)請判斷制取氨氣可能用到的裝置,在下表中你認為可行的裝置中填寫對應的實驗藥品(寫出化學式)。
| 裝置 | 實驗藥品 |
| A | |
| B | b: a: |
| C | c: 隔板: |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
醫用氯化鈣可用于補鈣、抗過敏和消炎等,以工業碳酸鈣(含少量Na+、Al3+、Fe3+等雜質)生產醫用二水合氯化鈣工藝流程為: 
已知:查閱資料得知氫氧化物沉淀時的pH為:
| 氫氧化物 | Fe(OH)3 | Al(OH)3 | |
| 開始沉淀時的pH | 2.3 | 4.0 | 開始溶解:7.8 |
| 完全沉淀時的pH | 3.7 | 5.2 | 完全溶解:10.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下表中的實驗操作能達到實驗目的或能得出相應結論的是
| 選項 | 實驗內容 | 實驗目的或實驗結論 |
| A | 向盛有2 mL 0.1 mol/L AgNO3溶液的試管中滴加5滴0.1 mol/L NaCl溶液,有白色沉淀生成,再向其中滴加5滴0.1 mol/L KI溶液 | 說明一種沉淀能轉化為溶解度更小的沉淀 |
| B | 向1 mL 20% 的蔗糖溶液中加入3~5滴稀硫酸,水浴加熱5 min,冷卻后再加入新制Cu(OH)2懸濁液,加熱 | 證明蔗糖能發生水解反應 |
| C | 水浴加熱濃硝酸、濃硫酸和苯的混合物后,直接蒸餾分液后得到的粗產品 | 制備純硝基苯 |
| D | 室溫下,分別向2支試管中加入相同體積、相同濃度的Na2S2O3溶液,再分別加入等體積不同濃度的稀硫酸 | 研究濃度對反應速率的影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用下列實驗裝置進行的實驗中,不能達到相應實驗目的的是 ( )
| A.裝置甲:氣體從b口進入,收集CO2 | B.裝置乙:可制得金屬錳 |
| C.裝置丙:實驗室制取乙酸乙酯 | D.裝置丁:驗證HCl氣體在水中的溶解性 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關實驗的表述中,錯誤的是( )
| A.除去乙醇的水:加新制生石灰,蒸餾,收集餾出物 |
| B.檢驗淀粉的水解產物:在用酸作催化劑的水解液中直接加入新制Cu(OH)2溶液,然后加熱,觀察是否有紅色沉淀生成 |
| C.除去乙酸乙酯中的乙酸:加飽和碳酸鈉溶液,充分振蕩,分液,棄水層 |
| D.銀氨溶液的配制:在潔凈的試管中加2% AgNO3溶液1~2 mL,逐滴加入2%稀氨水,邊滴邊振蕩,至沉淀恰好溶解時為止 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列根據實驗操作和現象所得出的結論正確的是
| 選項 | 實驗操作 | 實驗現象 | 結論 |
| A | 取等物質的量的兩種金屬單質X、Y,分別與足量的鹽酸反應 | X產生氫氣的體積比Y多 | 金屬性:X>Y |
| B | 等體積pH=3的HA和HB兩種酸分別與足量的鋅反應,排水法收集氣體 | HA放出的氫氣多且反應速率快 | HA酸性比HB強 |
| C | 在CuSO4溶液中加入KI溶液,再加入苯,振蕩 | 有白色沉淀生成,苯層呈紫色 | 白色沉淀可能為CuI |
| D | 取久置的Na2O2粉末,向其中滴加過量的鹽酸 | 產生無色氣體 | Na2O2沒有變質 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下述實驗能達到預期實驗目的的是( )
| 序號 | 實驗內容 | 實驗目的 |
| A | 室溫下,用pH試紙測定濃度為0.1 mol·L-1NaClO溶液和0.1 mol·L-1 CH3COONa溶液的pH | 比較HClO和CH3COOH的酸性強弱 |
| B | 向盛有1 mL硝酸銀溶液的試管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 說明一種沉淀能轉化為另一種溶解度更小的沉淀 |
| C | 向NaAlO2溶液中滴加飽和NaHCO3溶液,有白色沉淀產生 | 驗證兩者都發生了水解反應,且相互促進 |
| D | 室溫下,分別向2支試管中加入相同體積、相同濃度的Na2S2O3溶液,再分別加入不同濃度的稀硫酸 | 研究濃度對反應速率的影響 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com