
【題目】設NA表示阿伏加德羅常數值,下列敘述正確的是
A.NA個氧氣分子和NA個氫氣分子的質量比為16∶1
B.標準狀況下,22.4LH2O含有的分子數為NA
C.11.2L 氯氣中含有的原子數為NA個
D.2L 1mol/L Na2SO4溶液中Na+離子數為2NA個
科目:高中化學 來源: 題型:
【題目】某白色粉末由兩種物質組成,為鑒別其成分進行如下實驗:
①取少量樣品加入足量水仍有部分固體未溶解;再加入足量稀鹽酸,有氣泡產生,固體全部溶解;
②取少量樣品加入足量稀硫酸有氣泡產生,振蕩后仍有固體存在。
該白色粉末可能為( )
A. ![]() 、
、![]() B. AgCl、
B. AgCl、![]()
C. ![]() 、
、![]() D.
D. ![]() 、
、![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有四種不同堆積方式的金屬晶體的晶胞如圖所示,有關說法正確的是( )

A.①為簡單立方堆積②為六方最密堆積③為體心立方堆積④為面心立方最密堆積
B.每個晶胞含有的原子數分別為:①1個,②2個,③2個,④4個
C.晶胞中原子的配位數分別為:①6,②8,③8,④12
D.空間利用率的大小關系為:①<②<③<④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠礬(![]() )是治療缺鐵性貧血的特效藥。某化學興趣小組對綠礬進行了如下的探究:
)是治療缺鐵性貧血的特效藥。某化學興趣小組對綠礬進行了如下的探究:
I .【制備產品】
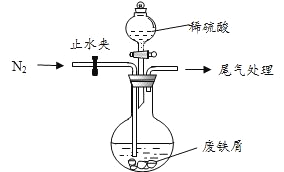
該小組由廢鐵屑(含少量氧化銅、氧化鐵等雜質),用上圖所示裝置制備![]() 晶體,步驟如下:
晶體,步驟如下:
(1)預處理:先將廢鐵屑加入到飽和![]() 溶液中洗滌,目的是_____,然后將廢鐵屑用水洗滌2~3 遍。
溶液中洗滌,目的是_____,然后將廢鐵屑用水洗滌2~3 遍。
(2)將洗滌后的廢鐵屑加入到圓底燒瓶中,并持續通入![]() ,
,![]() 的作用是________。
的作用是________。
(3)再加入足量稀硫酸,控制溫度 50℃~80℃之間,充分反應后,圓底燒瓶中剩余的固體為_____________。
(4)獲取產品:先向步驟(3)中反應后的混合物中加入少許蒸餾水,趁熱過濾, ____________。
濾出晶體,用少量冰水洗滌 2~3 次,再用濾紙將晶體吸干,密閉保存。
II.【測定![]() 含量】
含量】
(1)稱取上述樣品 10.0g,溶于適量的稀硫酸中,配成 100mL 溶液,需要的儀器除天平、膠頭滴管、 燒杯、量筒外,還需要的儀器有(填儀器名稱)____________________、_______________________。
(2)準確量取 25mL 該液體于錐形瓶中,用 0.1000mol/L ![]() 標準溶液滴定,則滴定終點的判斷方法是________________________。
標準溶液滴定,則滴定終點的判斷方法是________________________。
(3)用同樣的方法滴定 3 次,平均消耗 10.00mL 標準液,該樣品中![]() 的質量分數為____________。(已知 Mr(
的質量分數為____________。(已知 Mr(![]() )=278)
)=278)
(4)若測量結果偏小,則可能是在定容時_________________(填“俯視”或“仰視”)讀數。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有屬于前四周期的A、B、C、D、E、F、G七種元素,原子序數依次增大。A元素的價電子構型為nsnnpn+1;C元素為最活潑的非金屬元素,D元素核外有三個電子層,最外層電子數是核外電子總數的1/6;E元素正三價離子的3d軌道為半充滿狀態,F元素基態原子的M層全充滿,N層沒有成對電子,只有一個未成對電子;G元素與A元素位于同一主族,其某種氧化物有劇毒。
(1)A元素的第一電離能 B元素的第一電離能(填“<”“>”或“=”),A、B、C三種元素電負性由小到大的順序為 (用元素符號表示)。
(2)D元素原子的價電子排布式是 。
(3)C元素的電子排布圖為 ;E3+的離子符號為 。
(4)F元素位于元素周期表的 區,其基態原子的電子排布式為 。
(5)G元素可能的性質 。
A.其單質可作為半導體材料
B.其電負性大于磷
C.最高價氧化物對應的水化物是強酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com