
【題目】按要求回答下列問題:
(1)在標準狀況下,CO和CO2混合氣體的質量為32g,體積為22.4L,則其中CO與CO2物質的量之比為_____________,所含O原子的數目為_____________;將其中的CO2與足量的過氧化鈉反應,反應中轉移電子的物質的量為_____________。
(2)在實驗室將16.8g固體NaHCO3加熱一段時間后,測得剩余固體的質量變為13.7g。則減少的為_______物質的質量,有______gNaHCO3發生了分解反應。
【答案】 3:1 1.25×6.02×1023 0.25mol CO2和H2O 8.4
【解析】(1)標準狀況下,CO和CO2混合氣體的質量為32g,體積為22.4L,混合氣體的物質的量是1mol,則混合物的平均相對分子質量是32,根據十字交叉法可知CO與CO2物質的量之比為![]() ,其中CO和CO2的物質的量分別是0.75mol、0.25mol,因此所含O原子的物質的量是1.25mol,數目為1.25×6.02×1023;0.25molCO2與足量的過氧化鈉反應,反應中轉移電子的物質的量為0.25mol。(2)反應后固體質量減少了16.8g-13.7g=3.1g,根據方程式可知
,其中CO和CO2的物質的量分別是0.75mol、0.25mol,因此所含O原子的物質的量是1.25mol,數目為1.25×6.02×1023;0.25molCO2與足量的過氧化鈉反應,反應中轉移電子的物質的量為0.25mol。(2)反應后固體質量減少了16.8g-13.7g=3.1g,根據方程式可知
2NaHCO3![]() Na2CO3+H2O+CO2↑ 固體質量減少
Na2CO3+H2O+CO2↑ 固體質量減少
168 106 18 44 62
8.4g 3.1g
所以減少的為CO2和H2O的質量,有8.4gNaHCO3發生了分解反應。


 新活力總動員暑系列答案
新活力總動員暑系列答案 龍人圖書快樂假期暑假作業鄭州大學出版社系列答案
龍人圖書快樂假期暑假作業鄭州大學出版社系列答案科目:高中化學 來源: 題型:
【題目】將14g銅銀合金與足量的HNO3反應,放出的氣體與標準狀況下體積為1.12L的O2 混合后再通入水中,恰好全部吸收,則合金中銅的質量為
A. 4.8g B. 3.2g C. 6.4g D. 10.8g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】霉酚酸酯(MMF)是器官移植中抑制細胞增殖最常用的藥物.下列說法正確的是( ) 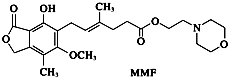
A.MMF能溶于水
B.1 mol MMF能與含3 mol NaOH的水溶液完全反應
C.1 mol MMF能與6 mol氫氣發生加成反應
D.MMF能發生取代反應和消去反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組采用類似制乙酸乙酯的裝置(如圖1),以環己醇制備環己烯.
已知: ![]()
密度(g/cm3) | 熔點(℃) | 沸點(℃) | 溶解性 | |
環己醇 | 0.96 | 25 | 161 | 能溶于水 |
環己烯 | 0.81 | ﹣103 | 83 | 難溶于水 |
(1)制備粗品將12.5mL環己醇加入試管A中,再加入1mL濃硫酸,搖勻后放入碎瓷片,緩慢加熱至反應完全,在試管C內得到環己烯粗品.
①A中碎瓷片的作用是 , 導管B除了導氣外還具有的作用是 .
②試管C置于冰水浴中的目的是 .
(2)制備精品①環己烯粗品中含有環己醇和少量酸性雜質等.加入飽和食鹽水,振蕩、靜置、分層,環己烯在層(填“上”或“下”),分液后用(填選項字母)洗滌.
a.KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再將環己烯按如圖2裝置蒸餾,冷卻水從進入.蒸餾時要加入生石灰,目的是 .
③收集產品時,控制的溫度應在左右,實驗制得的環己烯精品質量低于理論產量,可能的原因是(填選項字母).
a.蒸餾時從70℃開始收集產品
b.環己醇實際用量多了
c.制備粗品時環己醇隨產品一起蒸出
(3)以下區分環己烯精品和粗品的方法,合理的是(填選項字母).a.用酸性高錳酸鉀溶液 b.用金屬鈉 c.用溴水 d.測定沸點.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用硫酸廠燒渣(含鐵的氧化物和少量FeS及SiO2)制堿式硫酸鐵的流程如下:

(1)SO2與過量NaOH溶液反應的離子方程式為_____________。
(2)濾渣的主要成分為_________(填化學式)。
(3)反應1中加雙氧水的目的是將Fe2+氧化為Fe3+,該反應的離子方程式為________。
(4)堿式硫酸鐵的化學式為Fex(OH)y(SO4)z·nH2O,為確定其組成進行如下實驗:
①稱取1.6920g樣品溶于足量的稀鹽酸中;
②加足量的BaCl2溶液,過濾、洗滌、干燥、稱重,得固體質量為2.3300g;
③向步驟②的濾液中加過量的NaOH溶液,過濾、洗滌、灼燒、稱重,得固體質量為0.6400g。
根據以上實驗數據確定該堿式硫酸鐵的化學式_________(寫出計算過程)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述中正確的是( )
A. 2g氫氣所含原子數目為1mol
B. 1molO2的質量是32g
C. 硫酸的摩爾質量是98g
D. 鐵的摩爾質量在數值上等于鐵原子的相對原子質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,H2(g)+CO2(g)H2O(g)+CO(g)的平衡常數K= ![]() .該溫度下在甲、乙、丙三個恒容密閉容器中,投入H2(g)和CO2(g),其起始濃度如表所示.下列判斷不正確的是( )
.該溫度下在甲、乙、丙三個恒容密閉容器中,投入H2(g)和CO2(g),其起始濃度如表所示.下列判斷不正確的是( )
起始濃度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
A.平衡時,乙中CO2的轉化率大于60%
B.平衡時,甲中和丙中H2的轉化率均是60%
C.平衡時,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反應開始時,丙中的反應速率最快,甲中的反應速率最慢
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列描述中,不正確的是( )
A. 14N與15N具有相同的質子數 B. 18O和17O具有相同的電子數
C. 18O與19F具有相同的中子數 D. 12C與13C具有相同的質量數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】酸堿中和反應的本質是:H+ + OH- = H2O,下列物質間的反應可以用上述離子方程式表示的是( )
A. 氫氧化鐵和稀鹽酸反應 B. Ba(OH)2溶液滴入稀硫酸中
C. 澄清石灰水和稀硝酸反應 D. 氨水與鹽酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com