
���}Ŀ��![]() �ڲ������I(y��)�г��������儩��Óɫ�������I(y��)�ϲ������Ըߝ�Ⱥ���Uˮ
�ڲ������I(y��)�г��������儩��Óɫ�������I(y��)�ϲ������Ըߝ�Ⱥ���Uˮ![]() ��Ҫ��
��Ҫ��![]() ��ʽ����
��ʽ����![]() ��ȡ
��ȡ![]() �Ĺ�ˇ�������£�
�Ĺ�ˇ�������£�
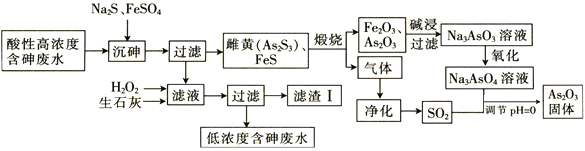
�ش����І��}��
![]() �������̵�__________�^�������ڗl����ԭ������������л���
�������̵�__________�^�������ڗl����ԭ������������л���![]() �����C��
�����C��![]() �Ĵ��ڣ�������
�Ĵ��ڣ�������![]() ����____________�Ե��@һ�������|(zh��)��
����____________�Ե��@һ�������|(zh��)��
![]() �{(di��o)��(ji��)
�{(di��o)��(ji��)![]() �r(sh��)����
�r(sh��)����![]() �Ƃ�
�Ƃ�![]() ���x�ӷ���ʽ��_____________________________��
���x�ӷ���ʽ��_____________________________��
![]() �����£���NaOH��Һ�ζ�
�����£���NaOH��Һ�ζ�![]() �r(sh��)�����N�������|(zh��)������?j��n)?sh��)�SpH��׃��������D��ʾ��
�r(sh��)�����N�������|(zh��)������?j��n)?sh��)�SpH��׃��������D��ʾ��
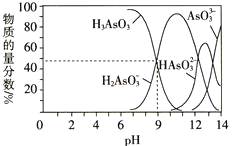
![]() AsO
AsO![]() ��________Ԫ________
��________Ԫ________![]() ������(qi��ng)����������
������(qi��ng)����������![]() �ᡣ
�ᡣ
![]() ��7�{(di��o)��(ji��)��10���^���аl(f��)������(y��ng)���x�ӷ���ʽ��____________________________��
��7�{(di��o)��(ji��)��10���^���аl(f��)������(y��ng)���x�ӷ���ʽ��____________________________�� ![]() ��һ����xƽ�ⳣ��(sh��)
��һ����xƽ�ⳣ��(sh��)![]() _______��
_______��
![]() �V�������
�V�������![]() ��
��![]() ��
��![]() ��_______________
��_______________![]() ��W(xu��)ʽ
��W(xu��)ʽ![]() ����֪
����֪
![]() ��������Ⱦ�����S�ŷŘ�(bi��o)��(zh��n)�鲻����
��������Ⱦ�����S�ŷŘ�(bi��o)��(zh��n)�鲻����![]() �����͝�Ⱥ���Uˮ
�����͝�Ⱥ���Uˮ![]() ���O(sh��)�����
���O(sh��)�����![]() ��ʽ����
��ʽ����![]() ��
��![]() �ĝ�Ȟ�
�ĝ�Ȟ�![]() ���t�͝�Ⱥ���Uˮ��
���t�͝�Ⱥ���Uˮ��![]() �ĝ�Ȟ�_________
�ĝ�Ȟ�_________![]() ��________
��________![]() ����������������������
����������������������![]() �ŷŘ�(bi��o)��(zh��n)��
�ŷŘ�(bi��o)��(zh��n)��
���𰸡��џ� �� ![]() �� ��
�� �� ![]()
![]()
![]()
![]() ����
����
��������
���Ըߝ�Ⱥ���Uˮ�������c�����၆�F���������၆�F�ɳ�ȥ�^�������x�ӣ��^�V�õ�As2S3��FeS���VҺ���Ё��F�x���Լ���������ȣ������^�������������F�x�ӣ�����������}������FeAsO4��Fe(OH)3��Ca3(AsO4)2���Լ������}�ȣ�As2S3��FeS������������As2O3�������F������������c��Һ����Na3AsO3����������Na3AsO4�����ɵĚ��w����������cNa3AsO4�����ԗl���°l(f��)������߀ԭ����(y��ng)����As2O3���Դ˽��ԓ�}��
![]() �������̵��џ��^�������ڗl����ԭ������������л���
�������̵��џ��^�������ڗl����ԭ������������л���![]() �����C��
�����C��![]() �Ĵ��ڣ�������
�Ĵ��ڣ�������![]() ���д��Ե��@һ�������|(zh��)��
���д��Ե��@һ�������|(zh��)��
�ʴ𰸞飺�џ����ţ�
![]() �{(di��o)��(ji��)
�{(di��o)��(ji��)![]() �r(sh��)����
�r(sh��)����![]() �Ƃ�
�Ƃ�![]() ���x�ӷ���ʽ��
���x�ӷ���ʽ��![]() ��
��
�ʴ𰸞飺![]() ��
��
![]() ����(j��)�}�������D��֪��
����(j��)�}�������D��֪��![]() ����Ԫ���
����Ԫ���
�ʴ𰸞飺��������
![]() ����(j��)�����D��֪��pH��7�{(di��o)��(ji��)��10���^���У�H3AsO3�����|(zh��)������?j��n)?sh��)�ڜp�٣�H2AsO3-�����|(zh��)������?j��n)?sh��)�����ӣ����l(f��)������(y��ng)���x�ӷ���ʽ�飺
����(j��)�����D��֪��pH��7�{(di��o)��(ji��)��10���^���У�H3AsO3�����|(zh��)������?j��n)?sh��)�ڜp�٣�H2AsO3-�����|(zh��)������?j��n)?sh��)�����ӣ����l(f��)������(y��ng)���x�ӷ���ʽ�飺![]() ��
��
�ʴ𰸞飺![]() ��
��
![]() ��һ����xƽ�ⳣ��(sh��)
��һ����xƽ�ⳣ��(sh��)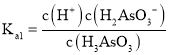 ����(d��ng)
����(d��ng)![]() �r(sh��)��
�r(sh��)��![]() ������
������![]() ��
��
�ʴ𰸞飺![]() ��
��
![]() ���������}����ˮ���V�����к���
���������}����ˮ���V�����к���![]() ��
��![]() ��
��![]() ���⣬߀����
���⣬߀����![]() ��
��
�ʴ𰸞飺![]() ��
��
![]() ��
��![]() �ĝ�Ȟ�
�ĝ�Ȟ�![]() ������
������![]() ���t�͝�Ⱥ���Uˮ��
���t�͝�Ⱥ���Uˮ��![]() �ĝ�Ȟ飺
�ĝ�Ȟ飺![]() ��208g/mol��103mg/g =
��208g/mol��103mg/g =![]() ����
��С��![]() �������ŷŘ�(bi��o)��(zh��n)��
�������ŷŘ�(bi��o)��(zh��n)��
�ʴ𰸞飺![]() ��
��![]() �����ϡ�
�����ϡ�



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ������(j��)����߀ԭ����(y��ng)��2Ag��(aq)��Cu(s)=Cu2��(aq)��2Ag(s)�O(sh��)Ӌ(j��)��ԭ늳أ���D��ʾ��
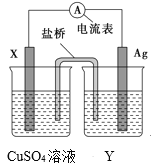
Ո�ش����І��}��
��1��늘OX�IJ�����___��늽��|(zh��)��ҺY��___��
��2���y늘O��늳ص�___�O���l(f��)����늘O����(y��ng)��___��X늘O�ϰl(f��)����늘O����(y��ng)��___��
��3�����·�е�����Ǐ�____�O����___�O��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����ij��غ��ݵ����]������(n��i)�l(f��)������(y��ng)��2A��g��+B��g��![]() C��g����H��0���_ʼ����2mol A��2mol B�����_(d��)��ƽ���B(t��i)�������f�����_����
C��g����H��0���_ʼ����2mol A��2mol B�����_(d��)��ƽ���B(t��i)�������f�����_����
A. �ٳ���2mol A��ƽ�����ƣ�A���D(zhu��n)��������
B. ������ߜضȣ�C���w�e��?j��n)?sh��)����
C. �������(qi��ng)�����W(xu��)ƽ��һ����������(y��ng)�����Ƅ�(d��ng)��B���w�e��?j��n)?sh��)�pС
D. �ٳ���1mol C��C�����|(zh��)������Ȍ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��![]() ��һ�N��Ч�����������Á����������ЙC(j��)��ζ�Ҳ�����cˮ�е��s�|(zh��)����r(ji��)�F���i�����衢�ӵȷ���(y��ng)����(sh��)�(y��n)�ҳ���
��һ�N��Ч�����������Á����������ЙC(j��)��ζ�Ҳ�����cˮ�е��s�|(zh��)����r(ji��)�F���i�����衢�ӵȷ���(y��ng)����(sh��)�(y��n)�ҳ���![]() ��(bi��o)��(zh��n)��Һ��(bi��o)��δ֪��ȵ�
��(bi��o)��(zh��n)��Һ��(bi��o)��δ֪��ȵ�![]() ��Һ���l(f��)������(y��ng)
��Һ���l(f��)������(y��ng)![]() ����
����
����(j��)������Ϣ��������І��}��
��1��������Ų�Kλ��Ԫ�����ڱ���________�^(q��)�����B(t��i)![]() �ĺ�������Ų�ʽ�ɱ�ʾ��________��
�ĺ�������Ų�ʽ�ɱ�ʾ��________��
��2��![]() �������еĹ��r(ji��)�I��(sh��)Ŀ��________��
�������еĹ��r(ji��)�I��(sh��)Ŀ��________��
��3�����B(t��i)Cԭ�ӵĺ��������ռ��(j��)����ܼ��������݆���D��________��![]() ��̼ԭ�ӵ�܉���s�������________��
��̼ԭ�ӵ�܉���s�������________��
��4��ͬ����Ԫ��������������(y��ng)��Κ仯��ķ��c(di��n)��![]() ��ԭ����________��
��ԭ����________��
��5��![]() �ĽY(ji��)��(g��u)��Se�������������ܶѷe�������Y(ji��)��(g��u)��D��ʾ��
�ĽY(ji��)��(g��u)��Se�������������ܶѷe�������Y(ji��)��(g��u)��D��ʾ��
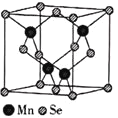
![]() ��Mn�����(sh��)��________��
��Mn�����(sh��)��________��
![]() ��ԓ���w�ľ�������(sh��)��apm�������ӵ��_����(sh��)��ֵ��
��ԓ���w�ľ�������(sh��)��apm�������ӵ��_����(sh��)��ֵ��![]() �t���x����ăɂ�(g��)�iԭ��֮�g�ľ��x��________pm��
�t���x����ăɂ�(g��)�iԭ��֮�g�ľ��x��________pm��![]() ���ܶ�
���ܶ�![]() ________
________![]() �г����_(d��)ʽ
�г����_(d��)ʽ![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���±��Ԫ�����ڱ��е������ڵIJ���Ԫ��![]() �����Ұ�ԭ����(sh��)�f������
�����Ұ�ԭ����(sh��)�f������![]() ������(j��)Ҫ��ش����І��}��
������(j��)Ҫ��ش����І��}��
K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
��1������Ԫ�صĻ��B(t��i)ԭ�ӵ�����Ų��У�4s܉����ֻ��1��(g��)��ӵ�Ԫ����______![]() ��Ԫ�����Q
��Ԫ�����Q![]() ��
��
��2������Ԫ���У�����s�^(q��)��Ԫ����_________�N������d�^(q��)��Ԫ����______�N��
��3����һ��x��![]() ________
________![]() ����
����![]() ������
������![]() ������
������![]() ������ͬ
������ͬ![]() ��
��
��4���F(xi��n)�к�⁵ăɷN�ɫ�ľ��w��![]() ����λ��(sh��)����6��һ�N����ɫ��һ�N��Gɫ�����P(gu��n)��(sh��)�(y��n)�C�����ɷN���w�ĽM�ɽԞ�
����λ��(sh��)����6��һ�N����ɫ��һ�N��Gɫ�����P(gu��n)��(sh��)�(y��n)�C�����ɷN���w�ĽM�ɽԞ�![]() ����y���@�ɷN���w�Ļ��W(xu��)ʽ���O(sh��)Ӌ(j��)������(sh��)�(y��n)��
����y���@�ɷN���w�Ļ��W(xu��)ʽ���O(sh��)Ӌ(j��)������(sh��)�(y��n)��
![]() �քeȡ���|(zh��)���ăɷN����ᄃ�w�Ę�Ʒ��ɴ��y��Һ��
�քeȡ���|(zh��)���ăɷN����ᄃ�w�Ę�Ʒ��ɴ��y��Һ��
![]() �քe�����y��Һ�е���
�քe�����y��Һ�е���![]() ��Һ�����a(ch��n)����ɫ������
��Һ�����a(ch��n)����ɫ������
![]() ��Һ����(y��ng)�õ��İ�ɫ�����|(zh��)������ɫ���w��ˮ��Һ����(y��ng)�õ������|(zh��)����
��Һ����(y��ng)�õ��İ�ɫ�����|(zh��)������ɫ���w��ˮ��Һ����(y��ng)�õ������|(zh��)����![]() ��ԇ�Ɣ���ɫ���w�Ļ��W(xu��)ʽ��_________��
��ԇ�Ɣ���ɫ���w�Ļ��W(xu��)ʽ��_________��
��5������Ԫ��K���}����ɫ����(y��ng)��__________ɫ���S������}�����l(f��)����ɫ����(y��ng)����ԭ����____________��
��6�������������w![]() ����һ�N��Ӳ���ϣ��Ѓ�(y��u)������ĥ�ԣ��侧����D��ʾ��
����һ�N��Ӳ���ϣ��Ѓ�(y��u)������ĥ�ԣ��侧����D��ʾ��
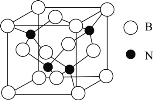
��������������߅�L��![]() ���t������������ܶȞ�________g/cm3
���t������������ܶȞ�________g/cm3![]() ֻҪ������ʽ������Ӌ(j��)�����(sh��)ֵ�������ӵ��_����(sh��)��ֵ��NA)��
ֻҪ������ʽ������Ӌ(j��)�����(sh��)ֵ�������ӵ��_����(sh��)��ֵ��NA)��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���Ҝ��£���![]() ��
��![]() ��Һ�ζ�
��Һ�ζ�![]()
![]() ��
��![]() ��Һ��ˮ����x�̶��S
��Һ��ˮ����x�̶��S![]() ��Һ�w�e��׃��������D��ʾ�������f�����_����( )
��Һ�w�e��׃��������D��ʾ�������f�����_����( )

A.ԓ�ζ��^�̑�(y��ng)ԓ�x���������ָʾ��
B.��![]() �c(di��n)��
�c(di��n)��![]() �c(di��n)����Һ��ˮ����x�̶���u����
�c(di��n)����Һ��ˮ����x�̶���u����
C.![]() �c(di��n)��Һ��
�c(di��n)��Һ��![]()
D.![]() �c(di��n)����(y��ng)��
�c(di��n)����(y��ng)��![]() ��Һ���w�e��
��Һ���w�e��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ������(j��)����߀ԭ����(y��ng)��2Ag+(aq)+ Cu(s) = Cu2+(aq)+ 2Ag(s) �O(sh��)Ӌ(j��)��ԭ늳����D��ʾ�������}��?y��n)魂֬�C�KNO3�}��Ո�ش����І��}��
(1)늘OX�IJ����� ___________��늽��|(zh��)��ҺY�� ____________________��
(2)�y늘O��늳ص� __________ �O����늘O����(y��ng)ʽ�飺___________________________________ ��
(3)�}������CuSO4��Һ���w�Ƶ��x���� ___________��

A��K+ B��NO3�D C��Ag+ D��SO42�D
�������\�i��늳���һ�Nһ��늳أ��⚤������\�����g��̼�������܇���̼�ۡ�MnO2��ZnCl2��NH4Cl�ȽM�ɵĺ�������ԓ늳��ڷ���^�̮a(ch��n)��MnOOH������̎��ԓ�U늳ؿɵõ���N����ԭ�ϡ��ش����І��}��
(1)ԓ늳ص����O����(y��ng)ʽ�� ________________________��늳ط���(y��ng)���x�ӷ���ʽ��________________________________________
(2)�U늳غ���������ˮ̎�����^�V���VҺ����Ҫ��ZnCl2��NH4Cl�����߿�ͨ�^ ___________________________________ ���x���ա�
(3)�V������Ҫ�ɷ���MnO2��̼�ۺ�MnOOH�������еõ��^����MnO2�����ķ�����_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�������£���һ����ȵĴ�����Һ�м���NaOH��Һ��������Һ![]() ��ʾ
��ʾ![]() ��
��![]() ��pX��ʾ����(y��ng)�����|(zh��)������ȵ�ؓ(f��)����(sh��)
��pX��ʾ����(y��ng)�����|(zh��)������ȵ�ؓ(f��)����(sh��)![]() �cpH���P(gu��n)ϵ��D��ʾ�������f���e(cu��)�`����
�cpH���P(gu��n)ϵ��D��ʾ�������f���e(cu��)�`����![]()

A.����A����![]() ��ʾ
��ʾ![]() �cpH���P(gu��n)ϵ
�cpH���P(gu��n)ϵ
B.�����£�![]() �Ĕ�(sh��)������
�Ĕ�(sh��)������![]()
C.ˮ����x�̶ȣ�![]()
D.Y�c(di��n)����(y��ng)��Һ������|(zh��)������ȵ�![]() ��
��![]() �Ļ����Һ
�Ļ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�������Ќ�(sh��)�(y��n)���F(xi��n)��ó��ĽY(ji��)Փ�����_���ǣ� ��
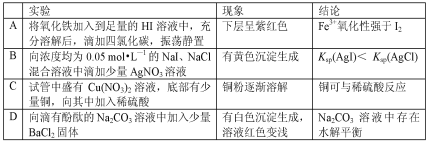
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_ | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com