
【題目】乙烯是重要有機化工原料。結合以下路線回答:
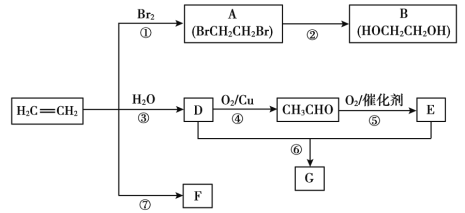
已知:2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
(1)反應①的化學方程式是__。
(2)B的官能團是__。
(3)F是一種高分子,可用于制作食品袋,其結構簡式為__。
(4)G是一種油狀、有香味的物質,有以下兩種制法。
制法一:實驗室用D和E反應制取G,某學習小組在實驗室制取乙酸乙酯的主要步驟如下:
i.配制2mL濃硫酸、3mLD(含18O)和2mLE的混合溶液。
ii.按如圖連接好裝置并加入混合液,用小火均勻加熱3~5min。
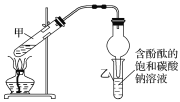
iii.待試管乙收集到一定量產物后停止加熱,撤出試管乙用力振蕩,然后靜置待分層。
iv.分離出乙酸乙酯,洗滌、干燥。
回答問題:
①裝置中球形干燥管,除起冷凝作用外,另一重要作用是___。
②步驟②安裝好實驗裝置,加入藥品前還應檢查__。
③反應中濃硫酸的作用是__;寫出能表示18O位置的制取乙酸乙酯的化學方程式:__。
④上述實驗中飽和碳酸鈉溶液的作用是__(填字母)。
a.中和乙酸并吸收乙醇
b.中和乙酸和乙醇
c.降低乙酸乙酯的溶解度
d.加速酯的生成,提高其產率
⑤步驟③所觀察到的現象是__;從試管乙中分離出乙酸乙酯的實驗操作名稱是___。
制法二:工業上用CH2=CH2和E直接反應獲得G。
a.反應類型是__。
b.與制法一相比,制法二的優點是__。
【答案】H2C=CH2+ Br2→BrCH2CH2Br 羥基(或—OH) ![]() 防止倒吸 裝置的氣密性 催化劑、吸水劑 CH3COOH+C2H518OH
防止倒吸 裝置的氣密性 催化劑、吸水劑 CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O ac 試管乙中的液體分成上下兩層,上層無色油狀,下層液體的紅色變淺 分液 加成反應 原子利用率高
CH3CO18OC2H5+H2O ac 試管乙中的液體分成上下兩層,上層無色油狀,下層液體的紅色變淺 分液 加成反應 原子利用率高
【解析】
(1)反應①為H2C=CH2與Br2發生加成反應,生成BrCH2CH2Br。
(2)B的官能團是-OH。
(3)F是一種高分子,可用于制作食品袋,則其為聚乙烯。
(4)G是一種油狀、有香味的物質,有以下兩種制法。
制法一:實驗室用D和E反應制取G,某學習小組在實驗室制取乙酸乙酯的主要步驟如下:
①裝置中球形干燥管,除起冷凝作用外,還能防止試管內液體進入反應試管內。
②制取氣體時,第一步操作通常為檢查裝置的氣密性。
③反應中濃硫酸的作用是催化劑和吸水劑;乙酸與乙醇發生酯化反應時,酸脫羥基醇脫氫。
④上述實驗中飽和碳酸鈉溶液的作用是中和乙酸并吸收乙醇、降低乙酸乙酯的溶解度。
⑤步驟③所得的溶液中,乙酸乙酯與水不互溶,由此可判斷反應產生的現象;試管乙中,乙酸乙酯與水分層。
制法二:工業上用CH2=CH2和E直接反應獲得G。
a.發生反應為CH2=CH2+CH3COOH→CH3COOCH2CH3,由此可確定反應類型。
b.與制法一相比,制法二中,CH3COOCH2CH3是唯一產物。
(1)反應①為H2C=CH2與Br2發生加成反應,生成BrCH2CH2Br,反應方程式為H2C=CH2+ Br2→BrCH2CH2Br。答案為:H2C=CH2+ Br2→BrCH2CH2Br;
(2)B的官能團是羥基(或-OH)。答案為:羥基(或-OH);
(3)F是一種高分子,可用于制作食品袋,則其為聚乙烯其結構簡式為![]() 。答案為:
。答案為:![]() ;
;
(4)G是一種油狀、有香味的物質,有以下兩種制法。
制法一:實驗室用D和E反應制取G,某學習小組在實驗室制取乙酸乙酯的主要步驟如下:
①裝置中球形干燥管,除起冷凝作用外,還能防止倒吸。答案為:防止倒吸;
②步驟②安裝好實驗裝置,加入藥品前還應檢查裝置的氣密性。答案為:裝置的氣密性;
③反應中濃硫酸的作用是催化劑和吸水劑;乙酸與乙醇發生酯化反應時,酸脫羥基醇脫氫,反應方程式為CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O。答案為:催化劑、吸水劑;CH3COOH+C2H518OH
CH3CO18OC2H5+H2O。答案為:催化劑、吸水劑;CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O;
CH3CO18OC2H5+H2O;
④上述實驗中飽和碳酸鈉溶液的作用是中和乙酸并吸收乙醇、降低乙酸乙酯的溶解度。答案為:ac;
⑤步驟③所得的溶液中,乙酸乙酯與水不互溶,由此可判斷反應產生的現象為試管乙中的液體分成上下兩層,上層無色油狀,下層液體的紅色變淺;試管乙中,乙酸乙酯與水分層,采用分液法分離。答案為:試管乙中的液體分成上下兩層,上層無色油狀,下層液體的紅色變淺;分液;
制法二:工業上用CH2=CH2和E直接反應獲得G。
a.發生反應為CH2=CH2+CH3COOH→CH3COOCH2CH3,反應類型為加成反應。答案為:加成反應;
b.與制法一相比,制法二中原子利用率高。答案為:原子利用率高。


 53隨堂測系列答案
53隨堂測系列答案科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A.標準狀況下,22.4 L水中所含的分子數約為6.02×1023個
B.1 mol Cl2中含有的原子數為NA
C.標準狀況下,aL氧氣和氮氣的混合物含有的分子數約為![]() ×6.02×1023個
×6.02×1023個
D.常溫常壓下,11.2 L CO分子數是0.5NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四種短周期元素X、Y、Z和W在周期表中的位置如圖所示,已知Y原子的最外層電子數是內層電子數的3倍,下列說法正確的是( )
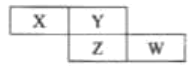
A.X、Y、Z和W均可以與氫元素形成18電子的共價化合物
B.簡單離子半徑:W<Z<Y<X
C.氧化物對應水化物的酸性:W>Z
D.Y與Z均為非金屬,兩者不能形成化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖表示在20mL![]() 溶液中逐滴加入
溶液中逐滴加入![]() 的NaOH溶液的pH變化曲線,下列說法不正確的是( )
的NaOH溶液的pH變化曲線,下列說法不正確的是( )

A.A點溶液存在的關系:![]()
B.C點溶液中各微粒濃度的大小關系為:![]()
C.在D點溶液中:![]()
D.當滴到20mL![]() 溶液時,反應達到終點,滴定過程中此時水的電離程度最大
溶液時,反應達到終點,滴定過程中此時水的電離程度最大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海洋中有豐富的資源,如圖為海水資源利用的部分過程。
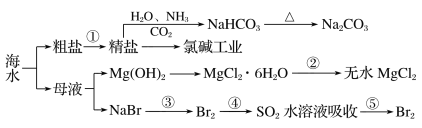
下列有關說法正確的是( )
A.用澄清石灰水可鑒別NaHCO3和Na2CO3
B.第③步和第⑤步均發生了氧化還原反應
C.在第③④⑤步中溴元素均被氧化
D.工業上通過電解飽和MgCl2溶液制取金屬鎂
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、M、Q、R是6種短周期元素,其原子半徑及主要化合價如下:
元素代號 | X | Y | Z | M | Q | R |
原子半徑/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
主要化合價 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(1)Y在元素周期表中的位置是___。
(2)元素Q和R形成的化合物A是果實催熟劑,用A制備乙醇的化學方程式是___。
(3)單質銅和元素M的最高價氧化物對應水化物的稀溶液發生反應的離子方程式為___。
(4)元素X的金屬性比元素Y___(填“強”或“弱”),用原子結構的知識解釋原因___。
(5)元素Q、元素Z的含量影響鋼鐵性能,采用如圖裝置A在高溫下將鋼樣中元素Q、元素Z轉化為QO2、ZO2。
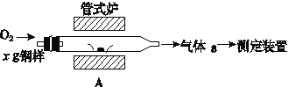
①氣體a的成分是__(填化學式)。
②若鋼樣中元素Z以FeZ的形式存在,在A中反應生成ZO2和穩定的黑色氧化物,則反應的化學方程式是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是常溫下幾種常見弱酸的電離平衡常數:
弱酸 | 電離方程式 | 電離平衡常數K |
CH3COOH | CH3COOH | K=1.6×10-5 |
H2C2O4 | H2C2O4 HC2O4- | K1=5.9×10-2 K2=6.4×10-5 |
H2CO3 | H2CO3 HCO3- | K1=4.4×10-7 K2=5.6×10-11 |
H2S | H2S HS- | K1=9.1×10-8 K2=1.1×10-15 |
回答下列問題:
(1)某溫度下,純水中的c(H+)=2.0×10-7mol·L-1,若溫度不變,滴入稀硫酸使c(H+)=5.0×10-6mol/L,則由水電離出的c(H+)為___mol·L-1。
(2)下列四種離子結合H+能力最強的是___。
A.HCO3- B.C2O42- C.S2- D.CH3COO-
(3)常溫下1.0mol·L-1的CH3COOH溶液中的c(H+)=___mol·L-1。
(4)常溫下,加水稀釋0.1mol·L-1的H2C2O4溶液,下列說法正確的是___。
A.溶液中n(H+)·n(OH-)保持不變
B.溶液中水電離的c(H+)·c(OH-)保持不變
C.溶液中![]() 保持不變
保持不變
D.溶液中c(OH-)增大
(5)將CH3COOH溶液加入少量Na2CO3溶液中,反應的離子方程式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】儲氫納米碳管的研制成功體現了科技的進步。用電弧法合成的碳納米管常伴有大量的雜質——碳納米顆粒。這種碳納米顆粒可用氧化氣化法提純。其反應中的反應物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七種。
(1)請用上述物質填空(不用配平):C+________+H2SO4——________+______+Cr2(SO4)3+H2O。
(2)上述反應中氧化劑是(填化學式)________,被氧化的元素是(填元素符號)________。
(3)H2SO4在上述反應中表現出來的性質是(填選項序號)________。
A.氧化性 B.氧化性和酸性 C.酸性 D.還原性和酸性
(4)若反應中電子轉移了0.8 mol,則產生的氣體在標準狀況下的體積為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數,則下列敘述中正確的是( )
A.同溫同壓下,NA個NO氣體與NA個N2和O2的混合氣體的體積相等
B.標準狀況下,22.4LCCl4所含分子數為NA
C.4℃時,9mL水和標準狀況下11.2L氮氣含有相同的原子數
D.1.7gH2O2中含有的電子數為NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com