
空氣質量與我們的健康息息相關,目前我國通過監測6項污染物的質量濃度來計算空氣質量指數(AQI),SO2、NO2和CO是其中3項中的污染物。
(1)上述3種氣體直接排入空氣后會引起酸雨的氣體有 (填化學式)。
(2)早期人們曾經使用鉛室法生產硫酸,其主要反應為:
SO2(g)+NO2(g) SO3(g)+NO(g)
SO3(g)+NO(g)
①若已知2SO2(g)+O2(g) 2SO3(g) ΔH=a kJ·mol-1
2SO3(g) ΔH=a kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=b kJ·mol-1
2NO2(g) ΔH=b kJ·mol-1
則SO2(g)+NO2(g) SO3(g)+NO(g) ΔH= kJ·mol-1。
SO3(g)+NO(g) ΔH= kJ·mol-1。
②一定溫度下,向固定體積為2 L的密閉容器中充入SO2和NO2各1 mol,發生反應:SO2(g)+NO2(g) SO3(g)+NO(g)。下列事實中不能說明該反應達到平衡狀態的是 (選填序號)。
SO3(g)+NO(g)。下列事實中不能說明該反應達到平衡狀態的是 (選填序號)。
a.體系壓強保持不變 b.混合氣體的顏色保持不變
c.NO的物質的量保持不變 d.每生成1 mol SO3的同時消耗1 mol NO2
③測得②中反應5 min末到達平衡,此時容器中NO與NO2的體積比為3︰1,則這段時間內SO2的反應速率υ(SO2)= ,此反應在該溫度下的平衡常數K= 。
(3)甲醇日趨成為重要的有機燃料,通常利用CO和H2合成甲醇,其反應的化學方程式為CO(g)+2H2(g) CH3OH(g)。今在一容積可變的密閉容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡轉化率(α)與溫度(T)、壓強(P)的關系如圖所示:
CH3OH(g)。今在一容積可變的密閉容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡轉化率(α)與溫度(T)、壓強(P)的關系如圖所示:
①上述合成甲醇的反應為 反應(填“放熱”或“吸熱”)。
②A、B、C三點的平衡常數KA、KB、KC的大小關系為 。
③若將達到平衡狀態A時生成的甲醇用于構成甲醇一氧氣燃料電池,電解質溶液為KOH濃溶液,則該電池工作時正極的電極反應式為 ,理論上通過外電路的電子最多為 mol。
(1)(2分) SO2、NO2 (2)(8分)① ②ad ③0.075mol/(L?min) 9
②ad ③0.075mol/(L?min) 9
(3)(6分)①放熱(1分) ②Ka=Kb>KC(1分) ③O2 + 2H2O + 4e-=4OH-(2分) 30(2分)
解析試題分析:(1)SO2和NO2排入大氣中最終分別變為硫酸和硝酸,從而形成酸雨。CO不能形成酸雨。
(2)①若已知2SO2(g)+O2(g)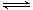 2SO3(g) ΔH=a kJ·mol-1、2NO(g)+O2(g)
2SO3(g) ΔH=a kJ·mol-1、2NO(g)+O2(g)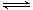 2NO2(g) ΔH=b kJ·mol-1,則根據蓋斯定律可知前者減去后者即得到反應2SO2(g)+2NO2(g)
2NO2(g) ΔH=b kJ·mol-1,則根據蓋斯定律可知前者減去后者即得到反應2SO2(g)+2NO2(g)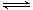 2SO3(g)+
2SO3(g)+
2NO(g),因此反應SO2(g)+NO2(g)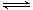 SO3(g)+NO(g) ΔH=
SO3(g)+NO(g) ΔH= kJ·mol-1。
kJ·mol-1。
②在一定條件下,當可逆反應的正反應速率和逆反應速率相等時(但不為0),反應體系中各種物質的濃度或含量不再發生變化的狀態,稱為化學平衡狀態,據此可以判斷。A、根據反應式可知,反應前后氣體的體積不變,因此壓強始終是不變,則體系壓強保持不變不能說明反應達到平衡狀態;b、顏色的深淺與NO2的濃度有關系,所以當混合氣體的顏色保持不變時,則說明NO2的濃度不再發生變化,因此反應達到平衡狀態;c、NO的物質的量保持不變說明正逆反應速率相等,達到平衡狀態;d、每生成1 mol SO3的同時,一定消耗1 molNO2,因此該關系是始終成立的,不能說明反應達到平衡狀態,答案選ad。
③ SO2(g)+NO2(g)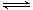 SO3(g)+NO(g)
SO3(g)+NO(g)
起始量(mol) 1 1 0 0
轉化量(mol) x x x x
平衡量(mol) 1-x 1-x x x
由于平衡時容器中NO與NO2的體積比為3︰1
則3-3x=x
解得x=0.75mol
所以平衡時消耗SO2的濃度是0.75mol÷2L=0.375mol/L
則這段時間內SO2的反應速率υ(SO2)=0.375mol/L÷5min=0.075mol/(L?min)
由于反應前后體積不變,所以可以用物質的量代替濃度計算平衡常數
則此反應在該溫度下的平衡常數K=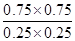 =9
=9
(3)①根據圖像可知,在壓強不變的條件下,隨著溫度的升高,CO的轉化率降低。這說明升高溫度平衡向逆反應方向移動,因此正方應是放熱反應。
②平衡常數只與溫度有關系,A和B兩點溫度相同,則平衡常數相等。升高溫度平衡向逆反應方向移動,平衡常數減小,所以三點平衡常數的大小關系是Ka=Kb>KC。
③原電池中負極失去電子,發生氧化反應。正極得到電子,發生還原反應。所以在燃料電池中燃料在負極通入,氧氣或空氣在正極通入。由于電解質是氫氧化鉀溶液,顯堿性,所以正極電極反應式為O2 + 2H2O + 4e-=4OH-;根據圖像可知A點CO的轉化率是0.5,則平衡常數生成甲醇的物質的量是10mol×0.5=5mol。甲醇中碳元素的化合價是-2價,反應后被氧化為+4價,失去6個電子,所以5mol甲醇反應轉移電子的物質的量是5mol×6=30mol。
考點:考查酸雨的形成、蓋斯定律、反應速率和平衡常數計算、平衡狀態判斷、外界條件對平衡狀態的影響以及電化學原理的應用與計算


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
甲醇是一種重要的化工原料。甲醇與水蒸氣催化重整可獲得清潔能源,具有廣泛的應用前景。現有如下實驗,在體積為1 L的密閉容器中,充入1mol CH3OH和1molH2O,一定條件下發生反應:CH3OH (g)+ H2O (g) CO2(g) +3 H2 (g),測得CO2和CH3OH(g)的濃度隨時間變化如下表所示。
CO2(g) +3 H2 (g),測得CO2和CH3OH(g)的濃度隨時間變化如下表所示。
| 時間 物質 | 0 min | 10 min | 30 min | 60 min | 70 min |
| CO2(mol/L) | 0 | 0.2 | 0.6 | 0.8 | 0.8 |
| CH3OH(mol/L) | 1.0 | 0.8 | 0.4 | 0.2 | 0.2 |
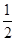 O2 (g)
O2 (g) CO2(g) + 2H2 (g) ?H1= —192.9kJ/mol
CO2(g) + 2H2 (g) ?H1= —192.9kJ/mol 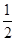 O2 (g)
O2 (g) H2 O(g) ?H2= —120.9kJ/mol
H2 O(g) ?H2= —120.9kJ/mol 
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
銅單質及其化合物在工業生產和科研中有重要作用。
(1)已知:2Cu2O(s) + O2(g) = 4CuO(s)△H=-292kJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
請寫出用足量炭粉還原CuO(s)制備Cu2O(s)的熱化學方程式: ;
(2)現用氯化銅晶體(CuCl2·2H2O,含氯化亞鐵雜質)制取純凈的CuCl2·2H2O。先將其制成水溶液,后按如圖步驟進行提純: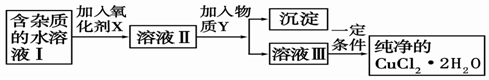
已知Cu2+、Fe3+和Fe2+的氫氧化物開始沉淀和沉淀完全時的pH見下表
| 金屬離子 | Fe3+ | Fe2+ | Cu2+ |
| 氫氧化物開始沉淀時的pH | 1.9 | 7.0 | 4.7 |
| 氫氧化物完全沉淀時的pH | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氨有著廣泛的用途,可用于化肥、硝酸、合成纖維等工業生產。
(1)根據最新“人工固氮”的研究報道,在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發生反應可生成氨氣: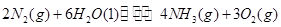
該反應在固定體積的密閉容器中進行,有關說法正確的是_____________(填序號字母)。
A.反應處于平衡狀態時,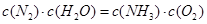 |
B.反應達到平衡后,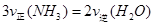 |
| C.體系的總壓強不變,說明反應已達平衡 |
| D.混合氣體的密度保持不變,說明反應已達平衡 |
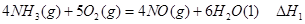 ①
①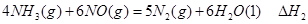 ②
②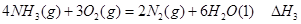 ③
③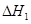 、
、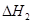 、
、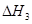 三者之間關系的表達式,
三者之間關系的表達式,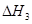 =_________。
=_________。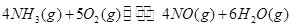
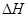 =
=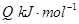


| 時間/濃度 |   | 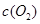  | 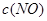  | 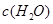  |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | a | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化學反應中既有物質變化,又有能量變化,釋放或吸收熱量是化學反應中能量變化的主要形式之一。已知C(石墨)、H2(g)燃燒的熱化學方程式分別為:
① C(石墨)+ O2(g)=CO(g)
O2(g)=CO(g)  ="-111.0" KJ·mol-1
="-111.0" KJ·mol-1
② H2(g)+  O2(g) =H20(g)
O2(g) =H20(g)  ="-242.0" kJ·mol-1
="-242.0" kJ·mol-1
③ C(石墨)+O2(g)=CO2(g)  ="-394.0" kJ·mol-1
="-394.0" kJ·mol-1
請解答下列問題:
(1)化學反應中有能量變化的本質原因是反應過程中有 的斷裂和形成。上述三個反應都是 (填“吸熱”或“放熱”)反應。
(2)在熱化學方程式中,需要標明反應物及生成物的狀態的原因是 ;在①中,02的化學計量數“1/2”是表示 (填字母)。
a.分子個數 b.物質的量 c.氣體的體積
(3)反應2H20(g)=2H2(g)+02(g)的 = KJ·mol-1。
= KJ·mol-1。
(4)若C(金剛石)+02(g)=C02(g)的 ="-395.0" kJ·mol-1,則穩定性:金剛石 (填“>”、“<”或“=”)石墨。
="-395.0" kJ·mol-1,則穩定性:金剛石 (填“>”、“<”或“=”)石墨。
(5)已知形成H20(g)中的2 mol H-O鍵能放出926.0 kJ的能量,形成1 mol 02(g)中的共價鍵能放出498.0 kJ的能量,則斷裂1 mol H2(g)中的H-H鍵需要的能量 KJ。
(6)工業制氫氣的一個重要途徑是用CO(g)與H2O(g)反應生成C02(g)和H2(g),則該反應的熱化學方程式是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氨在國民經濟中占有重要地位。
(1)工業合成氨時,合成塔中每產生1 mol NH3,放出46.1 kJ的熱量。
① 工業合成氨的熱化學方程式是 。
② 已知:
N2 (g)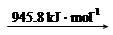 2N (g)
2N (g)
H2 (g)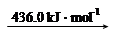 2H (g)
2H (g)
則斷開1 mol N-H鍵所需的能量是_______kJ。
(2)下表是當反應器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反應達到平衡時,混合物中NH3的物質的量分數隨壓強的變化曲線。
① 曲線a對應的溫度是 。
② 關于工業合成氨的反應,下列敘述正確的是 (填字母)。
A. 及時分離出NH3可以提高H2的平衡轉化率
B. 加催化劑能加快反應速率且提高H2的平衡轉化率
C. 上圖中M、N、Q點平衡常數K的大小關系是K(M)=" K(Q)" >K(N)
③ M點對應的H2轉化率是 。 (3)氨是一種潛在的清潔能源,可用作堿性燃料電池的燃料。電池的總反應為:
(3)氨是一種潛在的清潔能源,可用作堿性燃料電池的燃料。電池的總反應為:
4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g)。
則該燃料電池的負極反應式是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
以下是一些物質的熔沸點數據(常壓):
| | 鉀 | 鈉 | Na2CO3 | 金剛石 | 石墨 |
| 熔點(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
| 沸點(℃) | 774 | 882.9 | 1850(分解產生CO2) | ---- | 4250 |
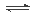 2 Na2CO3(l)+ C(s,金剛石) △H=-1080.9kJ/mol
2 Na2CO3(l)+ C(s,金剛石) △H=-1080.9kJ/mol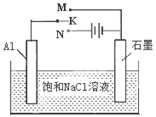
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
汽車尾氣里含有的NO氣體是由于內燃機燃燒的高溫引起氮氣和氧氣反應所致:
N2(g)+O2(g)  2NO(g) ΔH,已知該反應在 T ℃時,平衡常數K=9.0。
2NO(g) ΔH,已知該反應在 T ℃時,平衡常數K=9.0。
請回答:
(1)已知:N2(g)+2O2(g)  2NO2(g) ΔH1 2NO2(g)
2NO2(g) ΔH1 2NO2(g)  O2+2NO(g) ΔH2 ΔH= (用含ΔH1、ΔH2的表達式表示);
O2+2NO(g) ΔH2 ΔH= (用含ΔH1、ΔH2的表達式表示);
(2)某溫度下,向2 L的密閉容器中充入N2和O2各1 mol,5分鐘后O2的物質的量為0.5 mol,則NO的反應速率 ;
(3)假定該反應是在恒容條件下進行,下列能判斷該反應已達到平衡的是________;
| A.消耗1 mol N2同時生成1 mol O2 |
| B.混合氣體密度不變 |
| C.混合氣體平均相對分子質量不變 |
| D.2v正(N2)=v逆(NO) |
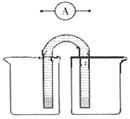
 2NO(g)的“K-T”、“c(NO)-t”圖,由圖A可以推知該反應為 反應(填“吸熱”或“放熱”)。由圖B可知,與a對應的條件相比,b改變的條件可以是 ;
2NO(g)的“K-T”、“c(NO)-t”圖,由圖A可以推知該反應為 反應(填“吸熱”或“放熱”)。由圖B可知,與a對應的條件相比,b改變的條件可以是 ;
 2NO(g)________________(填“處于化學平衡狀態”、“向正反應方向進行”或“向逆反應方向進行”),平衡時,N2在混合氣體的體積百分數為多少?(在答題卡上寫出具體計算過程,結果保留2位有效數字)
2NO(g)________________(填“處于化學平衡狀態”、“向正反應方向進行”或“向逆反應方向進行”),平衡時,N2在混合氣體的體積百分數為多少?(在答題卡上寫出具體計算過程,結果保留2位有效數字)查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2012年始,霧霾天氣無數次肆虐家鄉邯鄲。其中,燃煤和汽車尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為:2NO(g) + 2CO(g)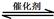 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
①該反應平衡常數表達式
②若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是 (填代號)。
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。
已知:Ⅰ CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
Ⅱ 2NO2(g)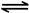 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
Ⅲ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式: 。
(3)甲烷燃料電池可以提升能量利用率。下圖是利用甲烷燃料電池電解100mL1mol/L食鹽水,電解一段時間后,收集到標準狀況下的氫氣2.24L(設電解后溶液體積不變).
①甲烷燃料電池的負極反應式: 。
②電解后溶液的pH= (忽略氯氣與氫氧化鈉溶液反應)
③陽極產生氣體的體積在標準狀況下是 L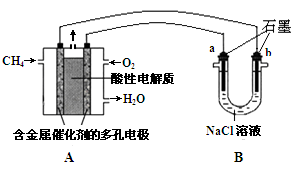
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com