
(14分)2014年10月初,霧霾天氣多次肆虐河北、天津、北京等地區。其中,燃煤和汽車尾氣是造成空氣污染的原因之一。
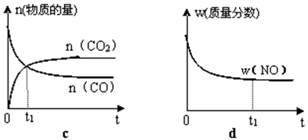
(1)汽車尾氣凈化的主要原理為:2NO(g) + 2CO(g) 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
①該反應的平衡常數表達式 。
②若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是 (填代號)。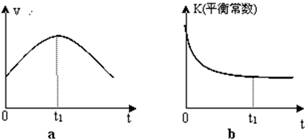
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g)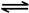 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式: 。
(3)在一定條件下,也可以用NH3處理NOx。已知NO與NH3發生反應生成N2和H2O,現有NO和NH3的混合物1mol,充分反應后得到的還原產物比氧化產物多1.4 g,則原反應混合物中NO的物質的量可能是_____________。
(4)以甲烷為原料制取氫氣是工業上常用的制氫方法。則2 molCH4與足量H2O(g)反應最多可生成_______mol H2,寫出該反應的化學方程式_________________________________________________。
(5)上述方法制得的H2可以和CO在一定條件下合成甲醇和二甲醚(CH3OCH3)及許多烴類物質。當兩者以物質的量1:1催化反應,其原子利用率達100%,合成的物質可能是 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
(1)①K=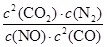 (2分) ②bd (2分)
(2分) ②bd (2分)
(2)CH4(g)+N2O4(g)=N2(g) +2H2O(l) + CO2(g) △H=—898.1kJ/mol (2分)
(3)0.3mol或0.8mol(2分)
(4)8 mol (2分) CH4(g)+2 H2O(g)= CO2(g)+4H2(g)(2分) (5)c(2分)
解析試題分析:(1)①化學平衡常數是在一定條件下,當可逆反應達到平衡狀態時,生成物濃度的冪之積和反應物濃度的冪之積的比值,因此根據反應式2NO(g) + 2CO(g)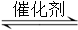 2CO2(g)+ N2(g)可知,該反應的平衡常數表達式K=
2CO2(g)+ N2(g)可知,該反應的平衡常數表達式K=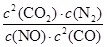 。
。
②a、到達平衡后正、逆速率相等,不再變化,t1時刻V正最大,之后隨反應進行速率發生變化,未到達平衡,故a錯誤;b、該反應正反應為放熱反應,隨反應進行溫度升高,化學平衡常數減小,到達平衡后,溫度為定值,達最高,平衡常數不變,為最小,圖象與實際符合,故b正確;c、t1時刻后二氧化碳、NO的物質的量發生變化,t1時刻未到達平衡狀態,故c錯誤;d、隨著反應的進行,NO的質量分數逐漸減小。t1時刻NO的質量分數為定值,不再發生變化,說明反應處于平衡狀態,故d正確,答案選bd。
(2)根據反應①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol、
②2NO2(g) N2O4(g) △H=-56.9 kJ/mol、③H2O(g) = H2O(l) △H = -44.0 kJ/mol并依據蓋斯定律可知,①-②+③×2即得到反應CH4(g)+N2O4(g)=N2(g) +2H2O(g) + CO2(l) ,所以該反應的反應熱△H=-867 kJ/mol+56.9 kJ/mol-44.0 kJ/mol×2=—898.1kJ/mol。
N2O4(g) △H=-56.9 kJ/mol、③H2O(g) = H2O(l) △H = -44.0 kJ/mol并依據蓋斯定律可知,①-②+③×2即得到反應CH4(g)+N2O4(g)=N2(g) +2H2O(g) + CO2(l) ,所以該反應的反應熱△H=-867 kJ/mol+56.9 kJ/mol-44.0 kJ/mol×2=—898.1kJ/mol。
(3)氨氣與NO反應的化學方程式為6NO+4NH3=5N2+6H2O,其中氨氣是還原劑,NO是氧化劑,則氮氣既是氧化產物,也是還原產物,還原產物比氧化產物多1mol,質量是28g,則
6NO+4NH3=5N2+6H2O 還原產物比氧化產物多
6mol 4mol 28g
0.3mol 0.2mol 1.4g
所以如果NO過量,則原反應混合物中NO的物質的量是1.0mol-0.2mol=0.8mol
如果氨氣過量,則原反應混合物中NO的物質的量是0.3mol
(4)CH4與足量H2O(g)反應要產生最多的氫氣,則為生成物應該是氫氣和CO2,反應的化學方程式為CH4(g)+2 H2O(g)= CO2(g)+4H2(g),.所以2mol甲烷與足量水蒸氣反應最多生成8mol氫氣。
(5)當H2和CO以物質的量1:1催化反應,其原子利用率達100%時,根據原子守恒可知生成物的化學式應該是CH2O,該物質是甲醛,答案選c。
考點:考查平衡常數、平衡狀態的判斷;蓋斯定律的應用;氧化還原反應的有關計算;綠色化學的應用


 快樂5加2金卷系列答案
快樂5加2金卷系列答案科目:高中化學 來源: 題型:填空題
“節能減排”,減少全球溫室氣體排放,意義十分重大。二氧化碳的捕捉與封存是實現溫室氣體減排的重要途徑之一,科學家利用 溶液噴淋“捕捉”空氣中的
溶液噴淋“捕捉”空氣中的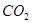 。
。
(1)使用過量 溶液吸收
溶液吸收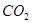 ,反應的離子方程式為________;若含有3molNaOH的溶液“捕捉”了22.4L
,反應的離子方程式為________;若含有3molNaOH的溶液“捕捉”了22.4L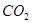 氣體(標準狀況),則所得溶液中鈉與碳元素的物料守恒關系式為__________(用離子濃度的關系式表示)。
氣體(標準狀況),則所得溶液中鈉與碳元素的物料守恒關系式為__________(用離子濃度的關系式表示)。
(2)①以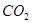 和
和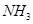 為原料可合成化肥尿素[
為原料可合成化肥尿素[ ]。已知:
]。已知:
 ①
①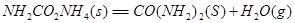
 ②
②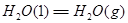
 ③
③
試寫出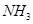 和
和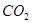 合成尿素和液態水的熱化學方程式__________。
合成尿素和液態水的熱化學方程式__________。
②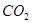 通過反應可轉化為
通過反應可轉化為 ,在催化劑作用下CO和
,在催化劑作用下CO和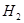 反應生成甲醇:
反應生成甲醇: 某容積可變的密閉容器中充有10molCO與20mol
某容積可變的密閉容器中充有10molCO與20mol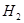 ,CO的平衡轉化率(a)與溫度、壓強的關系如下圖所示。
,CO的平衡轉化率(a)與溫度、壓強的關系如下圖所示。
A.若A點表示在某時刻達到的平衡狀態,此時容器的容積為VL,則該溫度下的平衡常數K=__________;平衡狀態B點時容器的容積 _______VL。(填“大于”、“小于”或“等于”)
_______VL。(填“大于”、“小于”或“等于”)
B.若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間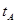 _______
_______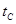 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
C.在不改變反應物用量的情況下,為提高CO的轉化率可采取的措施是________(寫出一種即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氫氧兩種元素形成的常見物質有H2O與H2O2,在一定條件下均可分解。
(1)已知:
| 化學鍵 | 斷開1mol化學鍵所需的能量(kJ) |
| H—H | 436 |
| O—H | 463 |
| O=O | 498 |
| 實驗編號 | 反應物 | 催化劑 | |
| a | 50 mL 5% H2O2溶液 | | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| b | 50 mL 5% H2O2溶液 | 少量濃鹽酸 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| c | 50 mL 5% H2O2溶液 | 少量濃NaOH溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| d | 50 mL 5% H2O2溶液 | | MnO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
金屬鎢用途廣泛,主要用于制造硬質或耐高溫的合金,以及燈泡的燈絲。高溫下,在密閉容器中用H2還原WO3可得到金屬鎢,其總反應為:
WO3 (s) + 3H2 (g) W (s) + 3H2O (g)
W (s) + 3H2O (g)
請回答下列問題:
⑴上述反應的化學平衡常數表達式為___________________________。
⑵某溫度下反應達平衡時,H2與水蒸氣的體積比為2:3,則H2的平衡轉化率為_____________________;隨溫度的升高,H2與水蒸氣的體積比減小,則該反應為反應_____________________(填“吸熱”或“放熱”)。
⑶上述總反應過程大致分為三個階段,各階段主要成分與溫度的關系如下表所示:
| 溫度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
 W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1  W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1  WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。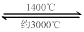 WI4 (g)。下列說法正確的有____________。
WI4 (g)。下列說法正確的有____________。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義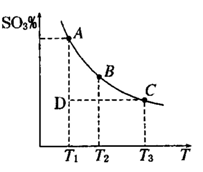
(1)硫酸生產中,SO2催化氧化生成SO3; 2SO2(g)+O2(g)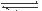 2SO3(g),混合體系中SO3 的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態).根據圖示回答下列問題,
2SO3(g),混合體系中SO3 的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態).根據圖示回答下列問題,
①2SO2(g)+O2(g)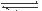 2SO3(g)的△H 0
2SO3(g)的△H 0
(填“>”或“<”):若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,平衡 移動(填“向左”“向右”或“不”)
②若溫度為T1、T2,反應的平衡常數分別為K1,K2,則K1 K2;反應進行到狀態D時, 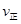
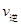 (填“>”“<”或“=”)
(填“>”“<”或“=”)
(2)氮是地球上含量豐富的一種元素,氮及其化合物在工農 業生產、生活中有著重要作用,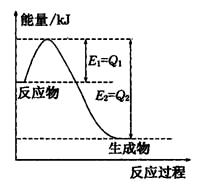
①如圖是一定的溫度和壓強下N2和H2反應生成lmolNH3過程中能量變化示意圖,請寫出工業合成氨的熱化學方程式:
(△H的數值用含字母Q1、Q2的代數式表示)
②氨氣溶于水得到氨水,在25℃下,將a mol·L-1的氨水與b mol·L-1的鹽酸等體積混合,反應后溶液顯中性,則c(NH4+) c(Cl-)(填“>”、“<”或“=”);用含a和b的代數式表示出該混合溶液中氨水的電離平衡常數 .
(3)海水中含有大量的元素,常量元素如氯,微量元素如碘,其在海水中均以化合態存在,在25℃下,向0.1L0.002mol·L-l的NaCl溶液中逐滴加入適量的0.1L0.002mol·L-l硝酸銀溶液,有白色沉淀生成,從沉淀溶解平衡的角度解釋產生沉淀的原因是 ,向反應后的濁液中繼續加入0.1L0.002mol·L-1的NaI溶液,看到的現象是 ,產生該現象的原因是(用離子方程式表示) 。
(已知:25℃時KSP(AgCl)=1.6×l0-10 KSP(AgI)=1.5×l0-16)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
尿素(H2NCONH2)是一種非常重要的高氮化肥,在工農業生產中有著非常重要的地位。
(1)工業上合成尿素的反應如下:
2NH3(l)+CO2(g) H2O(l)+H2NCONH2(l) △H=-103.7 kJ·mol-1
H2O(l)+H2NCONH2(l) △H=-103.7 kJ·mol-1
下列措施中有利于提高尿素的生成速率的是
| A.采用高溫 |
| B.采用高壓 |
| C.尋找更高效的催化劑 |
| D.減小體系內CO2濃度 |
 H2NCOONH4(氨基甲酸銨)(l) △H1
H2NCOONH4(氨基甲酸銨)(l) △H1 H2O(l)+H2NCONH2(l) △H2.
H2O(l)+H2NCONH2(l) △H2.
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)、①用肼(N2H4)為燃料,四氧化二氮做氧化劑,兩者反應生成氮氣和氣態水。
已知:N2(g)+2O2(g)=N2O4(g) ΔH=+10.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543kJ·mol-1
寫出氣態肼和N2O4反應的熱化學方程式: 。
②已知四氧化二氮在大氣中或在較高溫度下很難穩定存在,其很容易轉化為二氧化氮。試推斷由二氧化氮制取四氧化二氮的反應條件(或措施): 。
(2)科學家制造出一種使用固體電解質的燃料電池,其效率更高,可用于航天航空。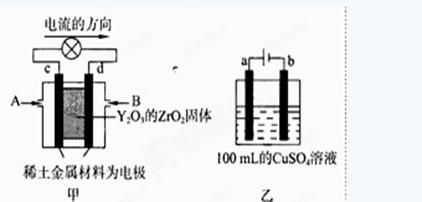
圖甲所示裝置中,以稀土金屬材料為惰性電極,在兩極上分別通入CH4和空氣,其中固體電解質是摻雜了Y2O3的ZrO2固體,它在高溫下能傳導陽極生成的O2-(O2+4e →2O2-)
①c電極為 ,d電極上的電極反應式為 。
②圖乙是電解100mL 0.5mol·L-1 CuSO4溶液,a電極上的電極反應式為 。若a電極產生56mL(標準狀況)氣體,則所得溶液的pH= (不考慮溶液體積變化),若要使電解質溶液恢復到電解前的狀態,可加入 (選填字母序號)
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
完成下列熱化學方程式(化學方程式、電極反應式、表達式等)的書寫:
(1)已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H = -169kJ·mol-1,
C(s)+1/2O2(g)=CO(g);△H = -110.5kJ·mol-1,
Cu(s)+1/2O2(g)=CuO(s);△H = -157kJ·mol-1
用炭粉在高溫條件下還原CuO生成Cu2O的熱化學方程式是:
(2)在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2(g) 2SO3(g),寫出該反應的化學平衡常數表達式:
2SO3(g),寫出該反應的化學平衡常數表達式:
(3)以甲烷、空氣為反應物,KOH溶液作電解質溶液構成燃料電池,則負極反應式為: 。
(4)無水AlCl3瓶蓋打開有白霧,其反應的化學方程式為 。
(5)“鎂—次氯酸鹽”燃料電池,其裝置示意圖如圖,該電池反應的總反應方程式為_____________________。
(6)工業上電解飽和食鹽水的離子方程式為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(15分)A、B、C、D、E、F是中學化學中常見的六種短周期元素,有關位置及信息如下:A的最高價氧化物對應的水化物與其氫化物反應生成離子化合物;C單質一般保存在煤油中;F的最高價氧化物對應的水化物既能與酸反應又能與堿反應,G單質是日常生活中用量最大的金屬,易被腐蝕或損壞。請回答下列問題: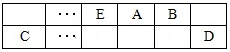
(1)A元素的氫化物水溶液能使酚酞變紅的原因用電離方程式解釋為 。
(2)同溫同壓下,將a L A氫化物的氣體和b L D的氫化物氣體通入水中,若所得溶液的pH=7,則a b(填“>"或“<”或“=”)
(3)常溫下,相同濃度F、G簡單離子的溶液中滴加NaOH溶液,F、G兩元素先后沉淀,F (OH)n完全沉淀的pH是4.7,G (OH)n完全沉淀的pH是2.8,則ksp較大的是: (填化學式)
(4)A與B可組成質量比為7:16的三原子分子,該分子釋放在空氣中其化學作用可能引發的后果有: 。
①酸雨 ②溫室效應 ③光化學煙霧 ④臭氧層破壞
(5)A和C組成的一種離子化合物,能與水反應生成兩種堿,該反應的化學方程式是 。
(6)已知一定量的E單質能在B2 (g)中燃燒,其可能的產物及能量關系如下左圖所示:請寫出一定條件下EB2(g) 與E(s)反應生成EB(g)的熱化學方程式 。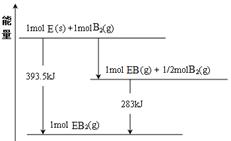
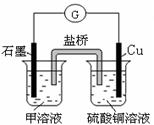
(7)若在D與G組成的某種化合物的溶液甲中,加入銅片,溶液會慢慢變為藍色,依據產生該現象的反應原理,所設計的原電池如上右圖所示,其反應中正極反應式為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com