
下列說法中,不正確的是
| A.利用鐵加入硫酸銅溶液中的反應不可以比較Cu、Fe2+的還原性: |
| B.足量的銅跟一定量的濃硝酸反應只產(chǎn)生一種氣體 |
| C.氮的固定不一定只有在高溫、高壓、催化劑的條件下才能實現(xiàn) |
| D.用苯萃取溴水中的Br2時,有機層從分液漏斗的下端放出 |
 發(fā)散思維新課堂系列答案
發(fā)散思維新課堂系列答案科目:高中化學 來源: 題型:單選題
將磁性氧化鐵放入稀HNO3中可發(fā)生如下反應:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O,下列判斷合理的是
| A.Fe(NO3)x中的x為2 |
| B.磁性氧化鐵中的鐵元素全部被氧化 |
| C.稀HNO3在反應中只作氧化劑 |
| D.反應中每生成0.4 mol還原產(chǎn)物,就有1.2 mol電子轉移 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
科學家發(fā)現(xiàn),食用蝦類等水生甲殼類動物的同時服用維生素C容易中毒,這是因為對人體無害的+5價砷類物質(zhì)在維生素C的作用下,能夠轉化為有毒的+3價砷類化合物。下列說法中不正確的是
| A.維生素C具有還原性 |
| B.上述過程中砷元素發(fā)生還原反應 |
| C.上述過程中+5價砷類物質(zhì)作氧化劑 |
| D.1 mol+5價砷完全轉化為+3價砷,共失去2 mol電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在反應2Na2O2+2H2O=4NaOH+O2↑中氧化劑和還原劑的質(zhì)量比為( )
| A.1 :1 | B.2 :1 | C.1 :2 | D.3 :1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一定溫度下,1 mol金屬銅與足量某濃度的硝酸完全反應,生成NO2和NO的物質(zhì)的量之比為1:3,則反應過程中轉移的電子為
| A.2 mol | B.3 mol | C.4mol | D.5 mo1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
對于反應3Br2+6NaOH=5NaBr+NaBrO3+3H2O,以下敘述正確的是
| A.Br2是氧化劑,NaOH是還原劑 |
| B.氧化產(chǎn)物與還原產(chǎn)物的物質(zhì)的量的比為5∶1 |
| C.Br2既是氧化劑又是還原劑 |
| D.每生成1mol的NaBrO3轉移6mol的電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在某100 mL的混合液中,硝酸和硫酸的物質(zhì)的量濃度分別是0.4 mol/L、
0.1 mol/L,向該混合液中加入1.92 g銅粉,加熱,待充分反應后,所得溶液中銅離子物質(zhì)的量濃度是( )
| A.0.15 mol/L | B.0.225 mol/L |
| C.0.30 mol/L | D.0.45 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用CH4催化還原NOx可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH="-574" kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH="-1" 160 kJ·mol-1
下列說法不正確的是( )
| A.由反應①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)ΔH="-Q" ,Q>574 kJ·mol-1 |
| B.等物質(zhì)的量的甲烷分別參加反應①、②,則反應轉移的電子數(shù)不同 |
| C.若用標準狀況下4.48 L CH4還原NO2至N2,放出的熱量為173.4 kJ |
| D.若用標準狀況下4.48 L CH4還原NO2至N2,整個過程中轉移的電子總數(shù)為1.6 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
如圖所示,兩圓圈相交的陰影部分表示圓圈內(nèi)物質(zhì)相互發(fā)生的反應,其中屬于氧化還原反應,但水既不作氧化劑也不作還原劑的是( )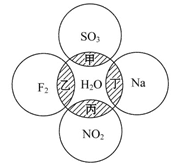
| A.甲 | B.乙 | C.丙 | D.丁 |
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com