
下圖為銅鋅原電池示意圖,下列說法正確的是
| A.電子由銅片通過導(dǎo)線流向鋅片 |
| B.燒杯中溶液逐漸呈藍(lán)色 |
| C.鋅片逐漸溶解 |
| D.該裝置能將電能轉(zhuǎn)變?yōu)榛瘜W(xué)能 |
C
解析試題分析:原電池中較活潑的金屬是負(fù)極,失去電子,發(fā)生氧化反應(yīng)。電子經(jīng)導(dǎo)線傳遞到正極,所以溶液中的陽離子向正極移動,正極得到電子,發(fā)生還原反應(yīng)。鋅比銅活潑,則根據(jù)裝置圖可知,鋅是負(fù)極,失去電子;銅是正極,溶液中的氫離子在正極得到電子,發(fā)生還原反應(yīng)生成氫氣。原電池是將化學(xué)能轉(zhuǎn)化為電能的裝置,所以正確的答案選C。
考點:考查原電池原理的有關(guān)判斷和應(yīng)用
點評:該題是高考中的常見考點,屬于基礎(chǔ)性試題的考查。該題的關(guān)鍵是明確原電池的工作原理,然后結(jié)合題意和裝置圖靈活運用即可,有利于培養(yǎng)學(xué)生的邏輯推理能力。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學(xué) 來源: 題型:單選題
下圖是電解CuCl2溶液的裝置,其中c、d為石墨電極。則下列有關(guān)的判斷正確的是( )
| A.a(chǎn)為陽極、b為陰極 | B.a(chǎn)為負(fù)極、b為正極 |
| C.電解過程中,氯離子濃度不變 | D.電解過程中,d電極質(zhì)量增加 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
在理論上可用來設(shè)計原電池的反應(yīng)是
| A.Fe +2HCl =" Fe" Cl2+ H2 |
| B.NaOH +HCl="NaCl+" H2O |
| C.Cu SO4 +2NaOH= Cu(OH)2+Na2 SO4 |
| D.Ca CO3+2HCl=" Ca" Cl2+ H2O+ CO2 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
下圖所示裝置中,觀察到電流計指針偏轉(zhuǎn),M棒變粗,N棒變細(xì),由此判斷下表中所列M、N、P物質(zhì),其中可以成立的是( )
| | M | N | P |
| A | 鋅 | 銅 | 稀硫酸溶液 |
| B | 銅 | 鐵 | 稀鹽酸溶液 |
| C | 銀 | 鋅 | 硝酸銀溶液 |
| D | 鋅 | 鐵 | 硝酸鐵溶液 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
在化學(xué)能與電能的轉(zhuǎn)化過程中,下列敘述正確的是 ( )
| A.電解飽和食鹽水時,陽極得到Cl2 和NaOH(aq) |
| B.教材所示的銅-鋅原電池在工作時,Zn2+ 向銅片附近遷移 |
| C.電鍍時,電鍍槽里的負(fù)極材料發(fā)生氧化反應(yīng) |
| D.原電池與電解池連接后,電子從原電池負(fù)極流向電解池陽極 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:單選題
如圖所示是Zn和Cu形成的原電池,某實驗興趣小組做完實驗后,在讀書卡上的記錄如下,則卡片上的描述合理的是 ( )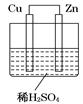
| 實驗后的記錄: ①Cu為負(fù)極,Zn為正極 ②Cu極上有氣泡產(chǎn)生,發(fā)生還原反應(yīng) ③ 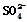 向Cu極移動 向Cu極移動④若有0.5mol電子流經(jīng)導(dǎo)線,則可產(chǎn)生0.25mol氣體 ⑤電子的流向是:Cu―→Zn ⑥正極反應(yīng)式:Cu—2e-===Cu2+,發(fā)生氧化反應(yīng) |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(13分)(1)將鋅、銅用導(dǎo)線連接后浸入2mol/L的稀硫酸中,正極電極反應(yīng)式為_________________,發(fā)生 反應(yīng)(填氧化或還原);電子從 經(jīng)外電路到 (填鋅或銅),溶液中H+ 向 移動(填正極或負(fù)極)。
(2)根據(jù)反應(yīng)2Fe3+ + Cu = 2Fe2++Cu2+ 設(shè)計原電池,所需負(fù)極材料為 ,溶液中Fe3+向 (填“負(fù)極”或“正極”)遷移,負(fù)極反應(yīng)式為 ;正極反應(yīng)式為 。
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com