
Na、Mg、Al三種金屬各2mol分別跟1L1mol?L-1的鹽酸反應時,相同條件下放出氫氣體積最大的是
| A.Al | B.Mg | C.Na | D.三者產生的氫氣一樣多 |
C
解析試題分析:n(HCl)=1mol.n(金屬)="2mol." A.2Al+6HCl=2AlCl3+3H2↑。HCl不足量。完全反應,Al過量,反應產生的氫氣按照HCl來計算。n(H2)=0.5mol。Mg+2HCl=MgCl2+ H2↑。HCl不足量。完全反應,Mg過量,反應產生的氫氣按照HCl來計算。n(H2)=0.5mol。C.2Na+2HCl="2NaCl+" H2↑。HCl不足量。完全反應,Mg過量,反應產生的氫氣按照HCl來計算, n(H2)=0.5mol。過量的Na會與水繼續反應2Na+2H2O=" 2NaOH+" H2↑。又產生氫氣的物質的量為0.5mol。所以一共產生的氫氣的物質的量為1mol。綜上所述相同條件下放出氫氣體積最大的是Na。選項為C。
考點:考查Na、Mg、Al與酸及水反應的知識。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:單選題
設NA為阿伏加德羅常數的數值,下列說法正確的是
| A.室溫下H2O2分解得到16 g O2,轉移的電子數為2NA |
| B.含1mol H2SO4的濃硫酸與足量銅反應轉移的電子總數為NA |
| C.標準狀況下11.2 L CO和H2的混合氣體完全燃燒消耗O2的量為0.25NA |
| D.相同物質的量OH-和CH3+含有相同數目的電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
設NA代表阿伏加德羅常數的數值,下列說法中正確的是( )
| A.1.8 g重水(D2O)中含有的質子數和電子數均為1.0NA |
| B.0℃、1個標準大氣壓下,22.4L NO 和22.4L O2混合后所得氣體中分子總數為1.5NA |
| C.含4mol Si-O鍵的二氧化硅晶體中,氧原子數為2NA |
| D.將11.2 L Cl2通入足量的石灰乳中制備漂白粉,轉移的電子數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列說法不正確的是
| A.炔烴的官能團為-C≡C- | B.乙烯的結構簡式為CH2CH2 |
| C.在鐵制品上鍍銅時用金屬銅作陽極 | D.用Na2S做沉淀劑除去廢水中的Cu2+和Hg2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關化學用語的說法中不正確的是( )
A.-OH與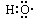 都表示羥基 都表示羥基 |
| B.次氯酸的結構式為:H—Cl—O |
C.CH4分子的球棍模型: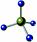 |
D.苯分子的比例模型: |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用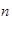 A表示阿伏加德羅常數的值。下列說法正確的是
A表示阿伏加德羅常數的值。下列說法正確的是
A.1 mol Cl-離子中含有的電子數為8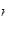 A A |
B.標準狀況下,2.24 L H20中含有的分子數為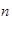 A A |
C.27g鋁與足量的氧氣反應,轉移的電子數為3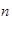 A A |
D.0.2 mo1·L-1 Ca(NO3)2溶液中含有的N03-離子數為0.4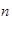 A A |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
有Na2CO3、NaHCO3、CaO和NaOH組成的混合物28.2g,把它們溶于足量的水,充分反應后,溶液中Ca2+、CO32—、HCO3—均轉化為沉淀,將容器中的水分蒸干,最后得到白色固體物質共30g。則下列有關敘述錯誤的是
| A.原混合物中含Na2CO3 0.1 mol |
| B.原混合物中n(Na2CO3)+n(NaHCO3)=n(CaO) |
| C.30g固體中一定存在n(CaCO3)<n(NaOH) |
| D.不能確定原混合物中NaOH的質量 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com