向34g10%的硝酸銀溶液中先加入14g氯化鋇溶液,氯化鋇完全反應后,把沉淀過濾后除去,然后再向濾液中加入足量氯化鈉溶液,完全反應后,將產生的沉淀充分干燥,稱得質量為1.435g,求原氯化鋇溶液中溶質的質量分數.(保留至0.1%)
【答案】
分析:根據化學方程式有加入氯化鈉生成沉淀的質量計算出與氯化鈉溶液反應的硝酸銀質量,然后根據氯化鋇溶液反應的硝酸銀質量從而求出原氯化鋇的質量,就可以計算出樣品中氯化鋇的質量分數.
解答:解:設與氯化鈉溶液反應的硝酸銀質量為x
AgNO
3+NaCl═AgCl↓+NaNO
3 170 143.5
x 1.435g
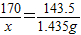
x=1.7g
則與氯化鋇溶液反應的硝酸銀質量為34g×10%-1.7g=1.7g
設與硝酸銀溶液反應的氯化鋇質量為y
BaCl
2+2AgNO
3═2AgCl↓+Ba(NO
3)
2 208 340
y 1.7g
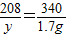
y=1.04g
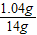
×100%=7.4%
答:原氯化鋇溶液中溶質的質量分數為7.4%.
故答案為:7.4%.
點評:本題主要考查含雜質物質的化學方程式的計算和溶質質量分數的計算,難度較大.

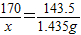
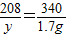
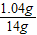 ×100%=7.4%
×100%=7.4% 

 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案